В лимфоциты субпопуляции в лимфоцитов функция
Исследование включает в себя определение абсолютного и относительного количества CD19+ B-лимфоцитов (B-клетки) и углубленный анализ малых популяций В-лимфоцитов. Это В1-клетки (популяция, связанная с продукцией аутоантител), В-клетки памяти. Рекомендуется к назначению для контроля показателей клеточного звена иммунной системы в динамике после комплексного иммунологического обследования.
Синонимы русские
Иммунофенотипирование, клеточный иммунитет, многоцветный клеточный анализ методом проточной цитометрии, В-клетки, В-лимфоциты, В1-клетки.
Синонимы английские
Human Immune System, Immunophenotyping, Multicolor Flow Cytometry Cell Analysis, Human Leukocyte Differentiation Antigens, Human B cells, B lymphocytes.
Метод исследования
Проточная цитометрия.
Какой биоматериал можно использовать для исследования?
Венозную кровь.
Как правильно подготовиться к исследованию?
- Исключить из рациона алкоголь в течение 24 часов до исследования.
- Детям в возрасте до 1 года не принимать пищу в течение 30-40 минут до исследования.
- Детям в возрасте от 1 до 5 лет не принимать пищу в течение 2-3 часов до исследования.
- Не принимать пищу в течение 12 часов до исследования, можно пить чистую негазированную воду.
- Полностью исключить (по согласованию с врачом) прием лекарственных препаратов в течение 24 часов перед исследованием.
- Исключить физическое и эмоциональное перенапряжение в течение 24 часов до исследования.
- Не курить в течение 30 минут до исследования.
Общая информация об исследовании
Оценка клеточного состава (иммунофенотипирование) лимфоцитов крови человека – основной компонент в оценке иммунного статуса – выполняется методом проточной цитофлуориметрии.
Иммунофенотипирование – характеристика клеток при помощи моноклональных антител или каких-либо других зондов, позволяющих судить об их типе и функциональном состоянии по наличию того или иного набора клеточных маркеров.
Иммунофенотипирование лейкоцитов заключается в обнаружении на их поверхности маркеров дифференциации, или CD антигенов. Лейкоциты экспрессируют ряд поверхностных и цитоплазматических антигенов, уникальных для своей субпопуляции и стадии развития. CD антигены (англ. cluster of differentiation antigens) – это антигены на поверхности клеток, маркеры, отличающие одни типы клеток от других. Дифференциации этих антигенов изучены и стандартизованы, им присвоены определенные номера. CD могут быть распознаны с помощью соответствующих моноклональных антител. Используя флюоресцентно-меченые моноклональные антитела, связывающиеся с определенными CD, можно с помощью метода проточной цитометрии произвести подсчёт содержания лимфоцитов, относящихся к различным по функции или стадии развития субпопуляциям.
В основе проточной цитофлуориметрии лежит проведение фотометрических и флюоресцентных измерений отдельных клеток, пересекающих одна за другой вместе с потоком жидкости луч монохроматического света, обычно света лазера.
CD19
СD19 является ключевой молекулой трансдукции сигналов, регулирующих развитие, активацию и дифференцировку В-лимфоцитов. Этот антиген экспрессируется практически на всех клетках В-ряда и не обнаруживается на лимфоидных клетках других типов, данный маркер рекомендуется для количественной характеристики общей популяции В-лимфоцитов.
Клиническая значимость характеристики определения количества СD19+ лимфоцитов:
– бактериальные и паразитарные инфекционные заболевания;
– агаммаглобулинемия и дисгаммаглобулинемия;
– злокачественные опухоли;
– злокачественные новообразования В-лимфоцитов (лимфолейкозы, лимфомы, миеломная болезнь и т.д.);
– аутоиммунные заболевания (системная красная волчанка, ревматоидный артрит и др.; ценность особенно возрастает при дополнительном включении анализа на CD5-фенотип);
– контроль эффективности проведенной вакцинации (в особенности противобактериальными вакцинами).
Функциональной пробой является постановка реакции бласттрансформации с использованием В-клеточных митогенов: липополисахарида (ЛПС) и митогена лаконоса.
Следует иметь в виду, что с превращением В-лимфоцитов в плазматические клетки на последних происходит утрата CD19-рецепторов. Важным является также то, что помимо В-клеток высокая экспрессия CD19 характерна и для фолликулярных дендритных клеток.
CD5
Молекулы CD5, экспрессированные на Т- или В-лимфоцитах, принимают непосредственное участие в модулировании сигнала, проводимого через антигенспецифический рецепторный комплекс (TCR и BCR). Помимо своей двойной экспрессии, CD5 может быть двойным рецептором, обеспечивающим стимулирующие или ингибирующие сигналы, в зависимости как от типа несущих его клеток, так и от стадии клеточного развития.
Клиническая значимость включения дополнительного анализа CD5-маркера состоит в следующем: после трансплантации костного мозга существенным образом уменьшается количество CD3+ Т-клеток, на которых не экспрессированы молекулы CD5. Чем выраженнее это уменьшение, тем тяжелее течение развивающейся болезни “3трансплантат против хозяина”. У человека герпес-вирусные инфекции индуцируют утрату экспрессии CD5 (а также и других костимуляторных молекул, например CD28 и CD6) в популяции CD8+ Т-клеток, которая после инфицирования значительно возрастает. Поскольку, как уже указывалось выше, CD5-маркер может быть экспрессирован на клетках В-клеточного ряда, то определенная клиническая значимость тестирования этого маркера характерна и при фенотипическом анализе В-лимфоцитов. СD5 представляет собой фенотипический маркер, обнаруживаемый при некоторых В-клеточных лимфопролиферативных расстройствах (В-ХЛЛ, лимфома маргинальной зоны селезенки, волосатоклеточный лейкоз и т.д.). Для ряда других аутоиммунных расстройств (ревматоидный артрит, синдром Шегрена, инсулинозависимый сахарный диабет, болезнь Грейвса и т.д.) характерна экспансия субпопуляции В1а-клеток (СD5+).
Метод позволяет определить количество популяции В-лимфоцитов:
- В-лимфоциты (CD19+CD3-);
и оценить малые клеточные популяции, а также изучить их функциональную активность:
- В-1-клетки (CD19+CD5+CD27-CD45+), связанные продукцией аутоантител;
- В-2-клетки (CD19+CD5-CD27-CD45+);
- В-клетки памяти (CD19+CD5-CD27+CD45+).
Когда назначается исследование?
Относительное количество общих В-лимфоцитов – важный диагностический признак. При воспалительных заболеваниях наблюдается значительное снижение процента В-лимфоцитов. Особенно ярко это выражено при остром панкреатите, хроническом пародонтите и тонзиллите, гнойном осложнении травм. Противоположный эффект наблюдается при острых и хронических гепатитах, у больных с тяжелым сепсисом с сочетанной патологией внутренних органов.
В настоящее время среди В-клеток выделяют три основные субпопуляции: В-1, В-2 и В-клетки памяти. Достаточно важная роль при данном делении отводится молекуле CD5. Молекула CD5 была расценена как возможный маркер B-клеток, позволяющий различать их субпопуляции: CD19+CD5+ B-клетки (также называемые B-1 клетки) и CD19+ CD5- B-клетки (или B-2 клетки).
B-1 клетки вызывают значительный интерес за счет того, что их ассоциируют с продукцией аутоантител и, как следствие, с аутоиммунными заболеваниями. Значительная роль B-1 клеток отмечена при ревматоидном артрите, системной красной волчанке и синдроме Шегрена. Увеличение количества CD5+ B-клеток наблюдали у пациентов, страдающих миастенией, инсулин-зависимым диабетом и тиреоидитом Хашимото. Значимость определения уровня циркулирующих В1-клеток показана также при первичных иммунодефицитах, например у пациентов с CVID (common variable immnodeficiency – общая вариабельная иммунная недостаточность). Доля CD5+ В-клеток может составлять треть и более от всех В-клеток при аутоиммунных заболеваниях.
Заболевания, при которых определение относительного количества В1-является диагностически значимым признаком (Зурочка А.В. и Хайдуков С.В., 2013).
Заболевания | Повышение относительного уровня В1-клеток |
Системная красная волчанка (СКВ) | ++++ |
Синдром Шегрена | ++++ |
Ревматоидный артрит | +++ |
Инсулинзависимый диабет | +++ |
Аутоиммунный тиреоидит | ++++ |
Миастения | +++ |
Неспецифический язвенный колит | +++ |
Аутоиммунные поражения при инфекционных заболеваниях (хламидиоз, синдром Рейтера, бруцеллез и др.) | +++ |
Рекомендовано для комплексного обследования пациентов, входящих в группу риска по четырем основным иммунопатологическим синдромам.
С аллергическим (атопическим) синдромом:
- атопический дерматит;
- нейродермит;
- экзема с инфекционным компонентом;
- тяжелая атопическая бронхиальная астма, поллиноз, хронический астматический бронхит.
С аутоиммунным синдромом:
- ревматоидный артрит;
- рассеянный склероз;
- диффузные заболевания соединительной ткани (системная красная волчанка, склеродермия, дерматомиозит);
- аутоиммунный тиреоидит;
- неспецифический язвенный колит.
Что означают результаты?
Изменения различных клеточных популяций лимфоцитов в сторону повышения или понижения развиваются при различных патологических процессах в организме, таких как инфекции, аутоиммунные и онкологические заболевания, иммунодефициты, в постоперационном периоде, при трансплантации органов.
Ниже представлена таблица с клиническими ситуациями, которые могут приводить к изменениям в субпопуляционном составе лимфоцитов.
Субпопуляция лимфоцитов | Повышение показателя | Снижение показателя |
В-лимфоциты (CD19+CD3-) |
|
|
B1-клетки (CD19+CD5+CD27-CD45+) |
| Не имеет диагностического значения. |
В совокупности с клиническими данными, симптоматикой, другими методами лабораторных исследований вышеуказанные изменения являются диагностическим признаком возникновения этих патологических процессов в организме человека.
Важные замечания
- Результаты данного исследования необходимо сопоставлять с клиническими данными и показателями других лабораторных анализов.
- Оценка показателей в динамике существенно повышает клиническую значимость исследования.
Литература
- Хаитов, Р.М. Аллергология и иммунология : национальное руководство / под ред. Р.М. Хаитова, Н.И. Ильиной. – М. : ГЭОТАР-Медиа, 2009. – 656 с.
- Хаитов, Р.М. Руководство по клинической иммунологии. Диагностика заболеваний иммунной системы : руководство для врачей / Р.М. Хаитов, Б.В. Пинегин, А.А. Ярилин. – М. : ГЭОТАР-Медиа, 2009. – 352 с.
- Зуева Е.Е. Иммунная система, иммунограмма : рекомендации по назначению и применению в лечебно диагностическом процессе /Е.Е Зуева, Е.Б. Русанова, А.В. Куртова, А.П. Рыжак, М.В. горчакова, О.В. Галкина – СПб. – Тверь: ООО «издательство «Триада», 2008. – 60 с.
- Кетлинский, С.А. Иммунология для врача / С.А. Кетлинский, Н.М. Калинина. СПб. : Гиппократ, 1998. – 156 с. Ярилин, А.А. Иммунология : учебник / А.А. Ярилин. – М. : ГЭОТАР-Медиа, 2010. – 752 с.
- Хаитов, Р.М. Иммунология : атлас / Р.М. Хаитов, А.А. Ярилин, Б.В. Пинегин.М. : ГЭОТАР-Медиа, 2011. – 624 с.
- Хаитов, Р.М. Иммунология : учебник / Р.М. Хаитов. – М. : ГЭОТАР-Медиа, 2009. – 320 с.
- Хаитов, Р.М. Оценка иммунного статуса человека в норме и при патологии / Р.М. Хаитов, Б.В. Пинегин // Иммунология. – 2001. – N4. – С. 4–6.
- Whiteside, T.L. Role of Human Natural Killer Cells in Health and disease / T.L. Whiteside, R.B. Herberman // Clinical and Diagnostic Laboratory Immunology. – 1994. – Vol. 1, №2. – P. 125–133.
- Ginadi, L. Differential expression of T-cell antigens in normal peripheral blood lymphocytes : a quantitative analysis by flow cytometry / L. Ginadi, N. Farahat, E. Matutes [et al.] // J. Clin. Pathol. – 1996. – Vol. 49, № 1. – P. 539–544.
- Merser, J.C. Natural killer T-cells : rapid responders controlling immunity and disease / J.C. Merser, M.J. Ragin, A. August // International J. Biochemistry & Cell Biology. – 2005. – № 37. – P. 1337–1343.
- Никитин, В.Ю. Маркеры активации на Т-хелперах и цитотокси ческих лимфоцитахна различных стадиях хронического вирусного гепатита С / В.Ю. Никитин, И.А. Сухина, В.Н. Цыган [и др.] // Вестн. Рос. Воен.-мед. акад. – 2007. – Т. 17, № 1. – С. 65–71.
- Boettler, T. T cells with CD4+CD25+ regulatory phenotype suppress in vitro proliferation of virus-specific CD8+ T cells during chronic hepatitis C virus infection / T. Boettler, H.C. Spangenberg, C. Neumann-Haefelin [et al.] // J. Virology. − 2005. − Vol. 79, N 12. −P. 7860–7867.
- Ormandy, L.A. Increased Populations of Regulatory T Cells in Peripheral Blood of Patients with Hepatocellular Carcinoma / L.A. Ormandy, T. Hillemann, H. Wedemeyer [et al.] // J. Cancer Res. − 2005. − Vol. 65, N 6. − P. 2457–2464.
- Sakaguchi, S. Naturally arising FoxP3-expressing CD4+CD25+ regulatory T cells in immunological tolerance to self- and non-self / S. Sakaguchi // Nature Immunol. − 2005. −Vol. 6, N 4. − P. 345–352.
- Romagnani, S. Regulation of the T cell response / S. Romagnani // Clin. Exp. Allergy. –2006. − Vol. 36. − P. 1357–1366.
- Хайдуков С.В., Основные и малые популяции лимфоцитов периферической крови человека и их нормативные значения (метод многоцветного цитометрического анализа) /Хайдуков С.В., Зурочка А.В., Тотолян А.А., Черешнев В.А. // Мед. иммунология. – 2009. -Т. 11 (2-3). – С. 227-238.
Источник
Оглавление темы “Иммунная система. Функции клеток иммунной системы. Т-лимфоциты. В-лимфоциты. Структура и функции органов иммунной системы.”: Функции В-лимфоцитов. Типы молекул на поверхности В-лимфоцитов.В-лимфоциты с помощью своих иммуноглобулиновых рецепторов могут распознавать не только пептиды, но и более крупные молекулы белков, нуклеиновых кислот, углеводов, липидов, полисахаридные и липопротеидные растворимые антигены. Зрелые В-лимфоциты способны самостоятельно распознавать растворимые антигены, в отличие от Т-лимфоцитов они не нуждаются в презентации чужеродных антигенов. Более того, В-лимфоциты сами могут выполнять функцию антигенпредставляющих клеток при взаимодействии с Ер2. Для этого В-лимфоциты имеют на своей поверхности адгезионные и костимулирующие молекулы, рецепторы для иммуноглобулинов, компонентов системы комплемента и для цитокинов (табл. 8.4). Таблица 8.4. Типы молекул на поверхности В-лимфоцитов
Распознавание антигена В-клеточным рецептором служит одним из сигналов активации В-лимфоцитов, которая проявляется их пролиферацией и дифференцировкой в продуцирующие иммуноглобулины плазматические клетки. Дополнительные сигналы активации В-клетки получают при взаимодействии с Th2, которые продуцируют и секретируют соответствующие цитокины: интерлейкины 4, 5, 6, 10. Синтез и секреция антител (иммуноглобулинов) В-лимфоцитами является завершающей стадией специфического гуморального иммунного ответа на конкретный антиген. В динамике иммунного ответа происходит переключение синтеза антител, который начинается с IgM, на другие изотипы: IgG, IgA или IgE. Переключение индуцируется разными цитокинами и взаимодействием костимулирующих молекул (CD40—CD40L), присутствующих на поверхности В-лимфоцитов и Th2. – Также рекомендуем “Антигенпредставляющие клетки. Структура и функции органов иммунной системы..” |
Источник
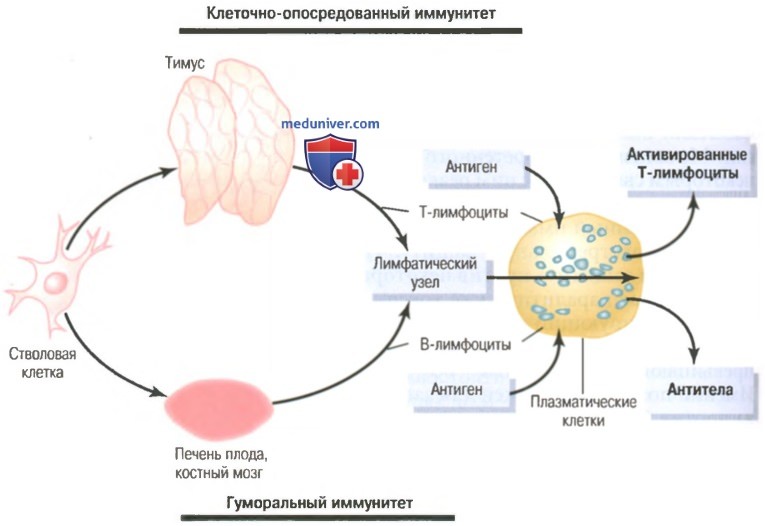
Т-лимфоциты и В-лимфоциты иммунитета. Предварительная обработка Т- и В-лимфоцитова) Клеточно-опосредованный и гуморальный иммунитеты обеспечивают два типа лимфоцитов – Т- и В-лимфоциты. Хотя при исследовании под микроскопом большинство лимфоцитов в нормальной лимфоидной ткани выглядят одинаковыми, эти клетки подразделяют на две основные популяции. Одна популяция — Т-лимфоциты — ответственна за формирование активированных лимфоцитов, обеспечивающих клеточно-опосредованный иммунитет. Другая популяция — В-лимфоциты — ответственна за формирование антител, обеспечивающих гуморальный иммунитет. Оба типа лимфоцитов образуются у эмбриона из полипотентных гемопоэтических стволовых клеток, формирующих лимфоциты как один из наиболее важных результатов их дифференцировки. Почти все сформированные лимфоциты в результате заселяют лимфоидную ткань, однако прежде чем это произойдет, они дополнительно дифференцируются или проходят предварительную обработку. Лимфоциты, которые в итоге станут активированными Т-лимфоцитами, сначала мигрируют к тимусу, где подвергаются предварительной обработке. Эти ответственные за клеточно-опо-средованный иммунитет лимфоциты называют Т-лимфоцитами, что подчеркивает роль тимуса. Другая популяция лимфоцитов, В-лимфоциты, предназначенные для формирования антител, проходят предварительную обработку в печени плода в середине периода внутриутробной жизни, а также в костном мозге в конце внутриутробной жизни плода и после рождения. Эта популяция клеток впервые была открыта у птиц, имеющих специальный орган для их предварительной обработки, который называют бурсой Фабриция (фабрициевой сумкой). Ответственные за гуморальный иммунитет лимфоциты называют В-лимфоцитами, что подчеркивает роль бурсы. На рисунке ниже показаны две лимфоцитарные системы для формирования: (1) активированных Т-лимфоцитов; (2) антител.
Предварительная обработка Т- и В-лимфоцитовВсе лимфоциты организма происходят от коммитированных в лимфоцитарном направлении стволовых клеток эмбриона, но эти клетки не могут непосредственно превратиться в активированные Т-лимфоциты или антитела. Прежде чем это станет возможным, клетки должны подвергнуться дальнейшей дифференцировке в соответствующих областях, где они проходят специфическую обработку. а) Т-лимфоциты проходят предварительную обработку в тимусе (вилочковой железе). После образования в костном мозге Т-лимфоциты сначала мигрируют к вилочковой железе. Здесь они быстро делятся, одновременно становясь чрезвычайно разнообразными, т.е. предназначенными для реакции против разных специфических антигенов. Это значит, что один лимфоцит, обработанный в тимусе, проявляет специфическую реактивность в отношении одного антигена. Следующий лимфоцит специфически реагирует на другой антиген. Это продолжается до тех пор, пока в тимусе не появятся тысячи разных типов лимфоцитов со специфической реактивностью в отношении тысяч разных антигенов. Эти разные типы предварительно обработанных Т-лимфоцитов оставляют тимус и распространяются кровью по всему телу, временно оседая в лимфоидной ткани. Кроме того, благодаря обработке в тимусе любой оставляющий его Т-лимфоцит не реагирует с белками или другими антигенами собственных тканей организма (иначе Т-лимфоциты погубили бы собственное тело человека в течение всего нескольких дней). Тимус выбирает, какие Т-лимфоциты могут его покинуть, сначала смешивая их практически со всеми специфическими аутоантигенами собственных тканей тела. Если Т-лимфоцит реагирует, он разрушается и фагоцитируется, вместо того, чтобы выделяться. Это происходит с основной частью клеток (вплоть до 90%). Таким образом, клетки, выделяющиеся из тимуса, не реагируют против собственных антигенов тела; они реагируют лишь на антигены внешних источников, например бактерий, токсинов или тканей, пересаженных от другого человека. Основная часть предобработки Т-лимфоцитов в тимусе происходит перед рождением ребенка и в течение нескольких месяцев после рождения. Удаление вилочковой железы после этого периода ослабляет (но не исключает) Т-лимфоцитарную иммунную систему. Однако удаление тимуса за несколько месяцев до рождения может нарушить развитие всего клеточно-опосредован-ного иммунитета. Поскольку именно клеточный тип иммунитета в основном отвечает за отторжение трансплантированных органов, например сердца или почек, органы можно пересаживать с меньшей вероятностью отторжения, если у животного в соответствующее время до его рождения удалить тимус. б) В-лимфоциты проходят предварительную обработку в печени и костном мозге. О деталях предварительной обработки В-лимфоцитов известно гораздо меньше, чем о предобработке Т-лимфоцитов. Известно, что у человека предварительная обработка В-лимфоцитов осуществляется в печени в середине внутриутробного периода развития, а также в костном мозге в конце внутриутробного периода и после рождения. Существуют два важных различия между В- и Т-лимфоцитами. Во-первых, В-лимфоциты активно секретируют реактивные агенты, называемые антителами, в отличие от Т-лимфоцитов, реагирующих с антигеном непосредственно. Антитела — это крупные белковые молекулы, способные соединяться с антигенной субстанцией и разрушать ее. Во-вторых, разнообразие В-лимфоцитов выражено больше, чем у Т-лимфоцитов, т.е. формируются миллионы типов В-лимфоцитарных антител с разными специфическими реактивностями. После предобработки В-лимфоциты, как и Т-лимфоциты, мигрируют к лимфоидной ткани по всему телу, где временно располагаются рядом, но несколько обособленно от областей локализации Т-лимфоцитов. – Также рекомендуем “Роль лимфоцитарных клонов. Происхождение клонов лимфоцитов” Оглавление темы “Клетки иммунитета. Виды иммунитета”: |
Источник