Транспорт липидов в лимфе
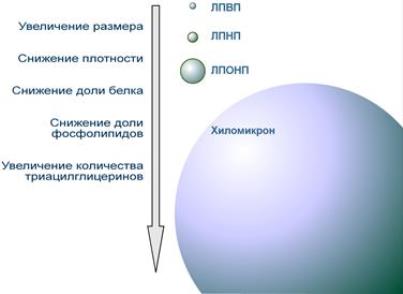
Поскольку липиды не растворимы в воде, для их переноса от слизистой кишечника в органы и ткани формируются особые транспортные формы: хиломикроны (ХМ), липопротеины очень низкой плотности (ЛПОНП), липопротеины низкой плотности (ЛПНП), липопротеины высокой плотности (ЛПВП). Непосредственно от слизистой тонкого кишечника транспорт всосавшихся и ресинтезированных липидов осуществляется в составе хиломикронов. ХМ – это белково-липидные комплексы диаметром от 100 до 500 нм, которые в связи с относительно большим размером не могут сразу проникать в кровь. Сначала они попадают в лимфу и в её составе попадают в грудной лимфатический проток, а затем – в верхнюю полую вену и с кровью разносятся по всему организму. Поэтому после приёма жирной пищи плазма крови становится мутной в течение 2 – 8 часов. Химический состав ХМ: Общее содержание липидов – 97-98%; в их составе преобладают ТАГ (до 90%), на содержание холестерина (Х), его эфиров (ЭХ) и фосфолипидов (ФЛ) суммарно приходится -7-8%. Содержание белка, стабилизирующего структуру ХМ – 2-3%. Т.о., ХМ – это транспортная форма «пищевого» или экзогенного жира. В капиллярах различных органов и тканей (жировой, печени, лёгких и др.) содержится липопротеидная липаза (ЛП-липаза), расщепляющая ТАГ хиломикронов до глицерина и жирных кислот. Плазма крови при этом просветвляется, т.е. перестаёт быть мутной, поэтому ЛП-липазу называют «просветвляющим фактором». Её активирует гепарин, который вырабатывается тучными клетками соединительной ткани в ответ на гиперлипидемию. Продукты расщепления ТАГ диффундируют в адипоциты, где они депонируются или поступают в другие ткани для покрытия энергозатрат. В жировых депо по мере необходимости организма в энергии происходит распад ТАГ до глицерина и жирных кислот, которые в комплексе с альбуминами крови транспортируются к периферическим клеткам органов и тканей.
Ремнантные ХМ (т.е. оставшиеся после расщепления ТАГ) поступают в гепатоциты и используются ими для построения других транспортных форм липидов: ЛПОНП, ЛПНП, ЛПВП. Их состав дополняется жирными кислотами ТАГ, фосфолипидами, холестерином, эфирами холестерина, сфингозинсодержащими липидами, синтезированными в печени «de novo». Размер ХМ и их химический состав изменяются по мере продвижения по сосудистому руслу. ХМ обладают наименьшей по сравнению с другими липопротеинами плотностью (0,94) и наиболее крупными размерами (их диаметр ~ 100нм). Чем выше плотность ЛП-частицы, тем меньше их размер. Диаметр ЛПВП наименьший (10 – 15нм), а плотность колеблется в диапазоне 1,063 – 1,21.
ЛПОНП формируются в печени, содержат в своём составе 55% ТАГ, поэтому они считаются транспортной формой эндогенного жира. ЛПОНП транспортируют ТАГ от клеток печени к клеткам сердца, скелетных мышц, лёгких и других органов, имеющим на своей поверхности фермент ЛП – липазу.
ЛП – липаза расщепляет ТАГ ЛПОНП до глицерина и жирных кислот, превращая ЛПОНП в ЛПНП (ЛПОНП – ТАГ = ЛПНП). ЛПНП могут также синтезироваться «de novo» в гепатоцитах. В их составе преобладает холестерин (~ 50%), их функция – транспорт холестерина и фосфолипидов к периферическим клеткам органов и тканей, имеющим на своей поверхности специфические рецепторы к ЛПНП. Холестерин и фосфолипиды, транспортируемые ЛПНП, используются для построения мембранных структур периферических клеток. Поглощаясь различными клетками, ЛПНП несут информацию о содержании холестерина в крови и определяют скорость его синтеза в клетках. ЛПВП синтезируются главным образом в клетках печени. Это наиболее устойчивые формы липопротеинов, т.к. содержат ~50% белка. Они отличаются высоким содержанием фосфолипидов (~20%) и низким содержанием ТАГ (~3%). ЛПВП (см. табл. №1) синтезируются гепатоцитами в виде плоских дисков. Циркулируя в крови, они поглощают избыток холестерина от различных клеток, стенок сосудов и, возвращаясь к печени, приобретают шаровидную форму. Т.О. , основная биологическая функция ЛПВП – транспорт холестерина от периферических клеток к печени. В печени избыток холестерина превращается в желчные кислоты.

Таблица №1. Химический состав транспортных липопротеинов (%).
| Химичесий состав | Хиломикроны | ЛПОНП | ЛПНП | ЛПВП |
| Белок | 2 -3 | |||
| ТАГ | ||||
| Холестерин | 3 -5 | |||
| Фосфолипиды | 3 – 4 |
ЛП – частицы крови: ХМ, ЛПОНП, ЛПНП, ЛПВП имеют общие закономерности строения. В центре располагаются неполярные (гидрофобные ) липиды: ТАГ и эфиры холестерина образуют гидрофобное ядро. В периферическом слое располагаются полярные липиды: глицерофосфолипиды, ганглиозиды и др., образуя гидрофильный слой ЛП-частицы. Свободный холестерин своей НО-группой обращён к поверхностному гидрофильному слою частицы. Белки липопротеидных частиц принято называть апопротеинами. Различают поверхностные, периферические и интегральные белки. Последние пронизывают гидрофильный слой частицы. Различают апопротеины А, В, С, которые делятся на подгруппы. В их составе ферменты, белки – рецепторы, активаторы ферментов, апо – белки. Они определяют растворимость ЛП – частиц, их устойчивость в кровеносном русле, связь с рецепторами клеточных мембран. Виды химических связей в ЛП- частицах, чаще всего, гидрофобные и ионные. Синтез различных апопротеинов происходит в гепатоцитах, в слизистой тонкого кишечника. Толщина гидрофильного слоя – 2,2 мкМ – одинакова у всех видов ЛП-частиц. Размер частиц определяется толщиной гидрофобного ядра.
Основными апопротеинами ХМ являются – апо В 48, ЛПОНП – апо В 100, ЛПНП – апо В 100, ЛПВП – апо А. Особую роль в составе ЛПВП выполняет фермент лецитинхолестеринацилтрансфераза (ЛХАТ), катализирующий реакцию: лецитин +свободный эфир холестерина + лизолецитин
Эфиры холестерина погружаются в гидрофобное ядро ЛП-частиц, при этом в поверхностном слое освобождается место для свободного холестерина. Забирая избыток свободного холестерина от клеток и стенок сосудов, ЛП-частицы постепенно приобретают шаровидную форму и возвращаются в печень. В печени избыток холестерина превращается в желчные кислоты. Ключевым ферментом этого процесса является 7-альфа гидроксилаза.
Источник
Поскольку липиды являются в основе своей гидрофобными молекулами, то они транспортируются в водной фазе крови в составе особых частиц – липопротеинов.
Структуру транспортных липопротеинов можно сравнить с орехом, у которых имеется скорлупа и ядро. “Скорлупа” липопротеина является гидрофильной, ядро – гидрофобное.
- поверхностный гидрофильный слой формируют фосфолипиды (их полярная часть), холестерол (его ОН-группа), белки. Гидрофильность липидов поверхностного слоя призвана обеспечить растворимость липопротеиновой частицы в плазме крови,
- “ядро” формируют неполярные эфиры холестерола (ХС) и триацилглицеролы (ТАГ), которые и являются транспортируемыми жирами. Их соотношение колеблется в разных типах липопротеинов. Также к центру обращены жирнокислотные остатки фосфолипидов и циклическая часть холестерола.
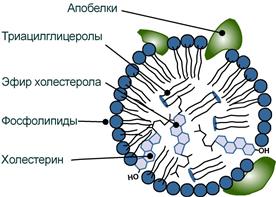
Схема строения любого транспортного липопротеина
Выделяют четыре основных класса липопротеинов:
- липопротеины высокой плотности (ЛПВП, α-липопротеины, α-ЛП),
- липопротеины низкой плотности (ЛПНП, β-липопротеины, β-ЛП),
- липопротеины очень низкой плотности (ЛПОНП, пре-β-липопротеины, пре-β-ЛП),
- хиломикроны (ХМ).
Свойства и функции липопротеинов разных классов зависят от их состава, т.е. от вида присутствующих белков и от соотношения триацилглицеролов, холестерола и его эфиров, фосфолипидов.
Подробно состав липопротеинов описан здесь

Cравнение размера и состава липопротеинов
Функции липопротеинов
Функциями липопротеинов крови являются
1. Перенос к клеткам тканей и органов
- насыщенных и мононенасыщенных жирных кислот в составе триацилглицеролов для последующего депонирования или использования в качестве энергетических субстратов,
- полиненасыщенных жирных кислот в составе эфиров холестерола для использования клетками в синтезе фосфолипидов или образования эйкозаноидов,
- холестерола в качестве мембранного материала,
- фосфолипидов в качестве мембранного материала,
Хиломикроны и ЛПОНП ответственны, в первую очередь, за транспорт жирных кислот в составе ТАГ. Липопротеины высокой и низкой плотности – за транспорт свободного холестерола и жирных кислот в составе его эфиров. ЛПВП способны также отдавать клеткам часть своей фосфолипидной оболочки.
2. Удаление избытка холестерола с мембран клеток.
3. Транспорт жирорастворимых витаминов.
4. Перенос стероидных гормонов (наряду со специфическими транспортными белками).
Апобелки липопротеинов
Белки в липопротеинах обычно называются апобелками, выделяют несколько их типов – А, В, С, D, Е. В каждом классе липопротеинов находятся соответствующие ему апобелки, выполняющие свою собственную функцию:
1. Структурная функция («стационарные» белки) – связывают липиды и формируют белок-липидные комплексы:
- апоВ-48 – присоединяет триациллицеролы,
- апоВ-100 – связывает как триацилглицеролы, так и эфиры холестерина,
- апоА-I – акцептирует фосфолипиды,
- апоА-IV – связывается с холестеролом.
2. Кофакторная функция («динамические» белки) – влияют на активность ферментов метаболизма липопротеинов в крови:
- апоС-II – кофактор гепаринзависимой липопротеинлипазы,
- апоС-III – кофактор печеночной ТАГ-липазы и ингибитор липопротеинлипазы,
- апоА-I, апоА-II и апоС-I – кофакторы лецитин-холестерол-ацилтрансферазы,
- апоЕ – ингибитор липопротеинлипазы.
3. Векторная функция (белки-маркеры, стационарные) – обеспечивают направленный транспорт липопротеинов:
- апоВ-48, апоВ-100 и апоА-I – связываются со своими рецепторами клеток-мишеней,
- апоЕ помогает взаимодействию векторных апобелков с рецепторами.
Названия апобелков B-48 и B-100 возникли не случайно. Длина мРНК гена апоВ равна 14 тысяч оснований и молекулярная масса “целого 100%-го” белка апоB-100 составляет 512 кДа. В мРНК имеется глутаминовый кодон СAA, который в результате процессинга мРНК превращается в терминирующий кодон UAA (стоп-кодон). В результате трансляции этой мРНК образуется укороченный апоB – апоВ-48 (241 кДа), который содержит N-концевые аминокислотные остатки апоВ-100.
Источник
Жирные
кислоты с длиной углеродной цепи менее
11 способны к самостоятельному всасыванию
через стенку кишечника в лимфу. Более
крупные молекулы усваиваются в комплексе
с желчными кислотами.
Глицерин
– трехатомный спирт, водорастворим и
легко всасывается из кишечника и по
воротной вене поступает в печень.
Комплекс
из 2-3 молекул желчных кислот и жирной
кислоты в стенке кишечника распадается.
После чего в стенке кишки происходит
синтез (ресинтез) триглицеридов.
Транспорт липидов в крови и лимфе.
Липиды
нерастворимы в воде, а, следовательно,
и в крови, поэтому весь транспорт липидов
в организме животных тесно связан с
белками. Транспорт липидов осуществляется
в комплексе с белками в виде липопротеинов.
Все
липопротеины имеют сходное строение.
В центре гидрофобное ядро (где и находится
триацилглицерол) и гидрофильный слой
на поверхности. Гидрофильный слой
представлен гидрофильными участками
белков (апопротеинов) и амфифильными
молекулами липидов (фосфолипидами и
холестеролом), гидрофобные части которых
погружены в гидрофобное ядро.
По
плотности и размеру частиц липопротеины
крови разделяют на хиломикроны (ХМ),
липопротеины очень низкой плотности (ЛПОНП),
липопротеины низкой плотности (ЛПНП),
липопротеины высокой плотности (ЛПВП).
Экзогенные
триглицеролы после всасывания в кишечнике
ресинтезируются. Синтезированные в
стенке кишечника триглицериды, ввиду
своих размеров попадают преимущественно
в лимфатическую систему, и лишь некоторое
количество поступает в портальный
кровоток. В лимфе и крови триглицериды
связываются с белком. Таким образом,
формируются мельчайшие капли –
хиломикроны. Хиломикроны – самые крупные
из липопротеинов крови, диаметр их более
120 нм. Однако при этом хиломикроны имеют
низкую плотность (0,92-0,98 г/мл).
Триацилглицеролы составляют до 85% всей
массы ХМ.
ЛПОНП
синтезируются в печени. Как и хиломикроны
обеспечивают транспорт триглицеридов,
которые составляют 50% массы ЛПОНП.
Под
действием мембранного фермента
эндотелиоцитов – липопротеинлипазы
из ХМ и ЛПОНП извлекаются триглицериды
на метаболические нужды тканей и
липопротеины увеличиваются по плотности.
Таким образом, формируются ЛПНП и ЛПВП.
Основная функция последних, транспорт
холестерола и фосфолипидов. ЛПНП и ЛПВП
поглощаются путем эндоцитоза клетками
печени, кишечника, жировой ткани, почек
и надпочечников. Следует отметить, что
ЛПНП обеспечивают транспорт холестерола
к тканям, а ЛПВП – от тканей к печени.
Синтез триглицеридов
Триглицериды
синтезируются в стенке кишечника, в
печени и жировой ткани (в адипоцитах).
Синтез
триглицеридов в стенке кишечника может
происходить из моноглицерида (из
2-моноацилглицерола) и двух молекул
активных жирных кислот (остатки жирных
кислот в комплексе с ацилпереносящим
энзимом – S-КоА),
или из глицерина и трех молекул активных
жирных кислот с участием АТФ, что более
характерно для процессов в печени и
жировой ткани.
Синтез
жира из глицерина и жирных кислот в
печени и жировой ткани происходит по
следующему пути. Глицерин фосфорилируется
с использованием АТФ до глицерофосфата
(фермент глицеролкиназа), затем под
действием фермента глицеролфосфатацилтрансферазы
взаимодействует с двумя молекулами
ацилкоэнзима-А (например, с пальмитил-КоА).
Образуется фосфатидная кислота
(3-фосфо-1,2-диацилглицерол). При
взаимодействии последней с ацилкоэнзимом-А
образуется триглицерид, свободныйHS-КоА
и остаток ортофосфорной кислоты.
Печень
– основной орган, где идет синтез жирных
кислот из продуктов гликолиза. Основной
путь синтеза триглицелидов в печени из
жирных кислот и глицерофосфата.
Глицерофосфат, в свою очередь, в печень
поступает из гидролиза жиров, а так же
при восстановлении диоксиацетонфосфата
(из гликолиза) при помощи восстановленного
НАДФ (НАДФ Н+Н).
Соседние файлы в папке Биохимия
- #
- #
- #
- #
- #
- #
- #
- #
- #
31.03.201521.5 Кб35Метионин.xls
- #
- #
Источник