Suv max для лимфоузлов
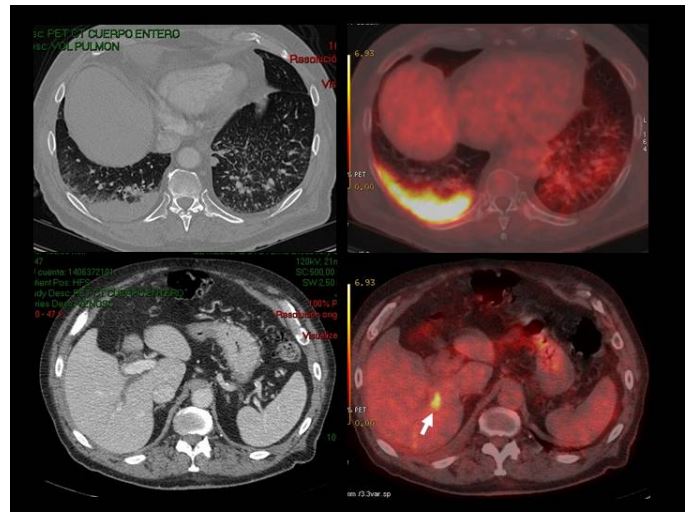
Показатели SUV MAX в ПЭТ/КТ исследовании
Как известно, работа ПЭТ/КТ томографа основывается на свойстве раковых клеток накапливать радиофармпрепарат в большом количестве. Метод позволяет не только визуализировать патологический процесс, но и произвести некоторые измерения. При ПЭТ/КТ в отличии от МРТ результативным показателем является не размер опухоли, а интенсивность накопления радиофармпрепарата в тканях организма.. Для количественного выражения уровня накопления ФДГ в диагностической практике используется коэффициент SUV MAX, сравнивающий уровень ФДГ в злокачественных тканях с накоплением его же в здоровых клетках.
SUV (стандартизированный уровень накопления радиофармпрепарата) — это коэффициент, используемый программным обеспечением любых современных томографов для полуколичественного анализа диагностических данных.
Интересно! Нормальные показатели SUV могут иметь разное цифровое значение. Дело в том, что в зависимости от томографа единицы измерения и сам параметр SUVmax могут меняться. Поэтому в протоколе исследования всегда имеется поясняющая ссылка, помогающая лечащему врачу верно интерпретировать SUV MAX ПЭТ/КТ.
Интерпретация результатов ПЭТ/КТ.
Для интерпретации диагностических данных ПЭТ/КТ, проведённого с фтордезоксиглюкозой, используют так называемую 4-уровневую шкалу интенсивности концентрации радиофармпрепарата:
- уровень — расслабленные мышцы и мягкие ткани;
- уровень — печень или выше (характерно для воспалительного процесса);
- уровень — между печенью и мозгом (характерно для метастаз или первичного очага, в редких указывает на хроническое воспаление);
- уровень — мозг и выше (характерно для метастаз или первичного очага).
Перед началом расшифровки ПЭТ/КТ-снимка необходимо установить базовую отсечку цветовой шкалы: фон — белый, мозг — черный.
Важно! Расшифровку SUV MAX и других диагностических данных, полученных при проведении ПЭТ/КТ должен проводить только опытный и высококвалифицированный специалист.
К неправильной интерпретации диагностических данных в том числе и коэффициента SUV может привести:
- наличие в организме пациента воспалительных процессов;
- физическая активность после введения радиофармпрепарата;
- присутствие на теле или одежде пациента металлических элементов гардероба или пирсинга;
- несоблюдение требований подготовительных мероприятий;
- некомпетентность врача;
- технические ошибки ПЭТ/КТ-томографа.
Почему SUV так важен?
SUV MAX по результатам ПЭТ/КТ — один из главных показателей, на который ориентируются врачи при расшифровке полученных в ходе проведения исследования данных. Важность показателя в диагностической практике сложно переоценить:
- во-первых, благодаря наличию пороговых значений нормы SUV при ПЭТ/КТ врач может различить патологические очаги и здоровые ткани;
- во-вторых, значение SUV до и после лечения позволяет сделать вывод о его эффективности и необходимости продолжения либо смене терапевтического курса;
- в-третьих, показатель имеет огромное прогностическое значение, позволяя наблюдать за развитием патологического процесса в динамике.
Полезная информация

ПЭТ/КТ после химиотерапии
Химиотерапия — основное «оружие» в сфере медикаментозного лечения злокачественных опухолей. По сути химиотерапия представляет собой лечение рака цитотоксическими средствами.
читать полностью

ПЭТ/КТ после операции
Хирургическое удаление опухоли — наиболее радикальный метод лечение онкологических заболеваний. Такая операция должна проводиться только при наличии показаний и только после всестороннего диагностического обследования.
читать полностью
все статьи
Источник
Здравствуйте, уважаемые консультанты!
У мужа первичная медиастинальная В-крупноклеточная лимфома с поражением переднего средостения, области яремной вырезки, надключичных лимфатических узлов слева, печени. Стадия IV.
Проведено 6 курсов про схеме R-EPOCH. После 5 курса по рекомендации врача сделали ПЭТ/КТ. Результат-остался очаг в средостении с некротическим аметаболическим центром (общий размер остаточного образования приблизительно 15 % от начальной массы (сама считала, по формуле S прямоугольного параллелепипеда) и крайне интенсивным свечением (наибольшее по передне-левому краю), max SUV = 30,75. С чем может быть связана такая высокая интенсивность поглощения глюкозы? Можно ли говорить о положительной динамике (после 2го курса осталось по результатам КТ около 30 % от начальной опухолевой массы в средостении, 1 очаг в печени (изначально по по УЗИ определялось 2 очага, по КТ-3), после 5го курса-только образование в средостении (около 15% от начального объема), но интенсивно поглощающее глюкозу)? Я разговаривала о SUV с онкологами, радиологами, никто в своей практике с такими цифрами не сталкивался. Если динамика недостаточная, какие варианты лечения можно использовать?
История болезни:
Сопутствующий диагноз: гепатит G (первично обнаружен 07.10.2014), синдром Жильбера в гетерозиготной форме.
Гистологическое заключение от 25.06.2014: Микроскопическое описание: в готовом препарате и препарате, изготовленном с блока в кусочке соединительной ткани разрастание лимфомы из крупных полиморфных клеток. Последние благодаря тонким, кольцевидным прослойкам местами формируют ячеистые структуры. Для уточнения морфологического варианта лимфомы на срезах с парафинового блока проведено иммуногистохимическое исследование с использованием антител к: CD3, CD5, CD10, CD20, CD23, CD30, CD43, BCL2, BCL6, MuM1, Ki67, панцитокератину. Опухолевые клетки экспрессируют CD20, CD23, MuM1 (до 50% опухолевых клеток), BCL2, BCL6. Маркер пролиферативной активности Ki67 экпрессируют 70-80% опухолевых клеток. С остальными маркерами реакции в опухолевых клетках негативные. В опухолевой ткани имеется умеренное количество дискретно лежащих реактивных CD3+, CD43+ Т-клеток.
Заключение: морфоиммуногистохимическая характеристика опухолевых клеток, с учетом локализации очага поражения, соответствует первичной медиастинальной (тимической) В-крупноклеточной лимфоме.
Миелограмма от 27.06.2014: пунктат клеточный. Показатели миелограммы в пределах нормальных значений. Мегакариоциты в достаточном количестве.
Трепанобиоптат от 27.06.2014: костный мозг представлен всеми ростками кроветворения составляет примерно 50% всех клеток. Данных за опухоль нет.
КТ ОГК от 20.06.2014 (с контрастным усилением): в верхнем и среднем этажах переднего средостения выявляется массивный опухолевый конгломерат, неоднородно накапливающий контрастное вещество, размером до 13,6х9,1 (на уровне передних отрезков 3х ребер), верхний полюс которого расположен на уровне яремной вырезки, нижний – на уровне переднего отрезка 4го ребра слева. Левая плечеголовая вена отчетливо не дифференцируется, вероятно, проходит в толще опухолевого конгломерата. Задняя поверхность опухоли тесно прилежит к сосудистым структурам средостения: верхней полой вене, плечеголовному стволу, левым общей сонной и подключичной артериям, восходящему отделу и дуге аорты, легочному стволу и к левой легочной артерии. Опухоль спускается вниз по передней и левой поверхности сердца, вероятно инфильтрируя перикард, в полости которого определяется жидкость слоем до 1,8 см, компремирует прилежащие отделы верхней доли левого легкого (на отдельных срезах нельзя исключить врастание опухоли в парамедиастинальные отделы легкого). Справа – без явных признаков инфильтрации легочной ткани. Передняя поверхность опухоли прилежит к внутренним отделам передней грудной стенки (без явных признаков инвазии в прилежащие отделы ребер и грудины). Верхушки легких фиброзно изменены. В С1 верхней доли левого легкого выявляется неправильной вытянутой формы участок уплотнения размером ~ до 0,7 см; ниже уплотнение размером до 0,6 см; в язычковых сегментах верхней доли левого легкого определяется очаговоподобное уплотнение размером до 0,4 см; субплеврально в С9 нижней доли-0,4 см; на границе междолевой плевры С6-4 правого легкого-очаговоподобное уплотнение размером до 0,6 см. В левой плевральной полости определяется выпот слоем до 1,0 см. Справа- выпота нет.
В левой надключичной области определяются отдельные лимфатические узлы размером до 1,0 см. Подмышечные, подключичные лимфоузлы с обеих сторон не увеличены. Костно-деструктивные изменения в зоне исследования не выявлены.
По данным КТ ОГК (без контрастного усиления) от 21.08.2014 (после 2 курса ПХТ): отмечается выраженное уменьшение размеров опухоли с 13,6х9,1 см до 6,2х3,8 см (на уровне передних отрезков 3х ребер). Вертикальный размер опухоли уменьшился ~ с 13,5 до 9,5 см, верхний край расположен на уровне рукоятки грудины (ранее на уровне яремной вырезки); нижний-на уровне хрящевого отрезка 3го ребра слева (ранее на 4м). Перестал определяться выпот в полости перекарда и в левой плевральной полости. В средостении стали прослеживаться отдельные лимфатические узлы: паратрахеально справа-до 0,6 см, аортопульмональные-до 0,4 см, бифуркационные-до 0,8 см. Левые надключичные лимфатические узлы уменьшились до 0,6 см.
Отмечается уменьшение количества и размеров очагов в легких: в С1 верхней доли левого легкого уменьшилось с 0,7 см до 0,5 см; субплеврально в С9 нижней доли с 0,4 см до 0,3 см. Остальные очаги в легких отчетливо не выявляются.
Заключение: лимфома с поражением переднего средостения, левых надключичных лимфатических узлов. Положительная динамика.
УЗИ от 26.06.2014
Печень: не увеличена, КВР правой доли 14,0, контуры четкие, ровные. В 1 сегменте определяется очаг 2,0х1,4 см. В 4 сегменте, кпереди от ворот, определяется очаг до 3,0х2,4 см. В других сегментах очаговые образования не определяются.
Селезенка: не увеличена, размером 10,0х4,5 см, контуры четкие, ровные, структура однородная, очаговые образования не определяются, в области ворот селезенки-без дополнительных образований.
УЗИ от 21.08.2014
Печень: не увеличена, КВР правой доли 14,0, контуры четкие, ровные. В 1 сегменте очаг не определяется. В 4 сегменте, кпереди от ворот, определяется нечеткий очаг до 1,4х0,8 см. В других сегментах очаговые образования не определяются.
УЗИ от 23.09.2014: Печень: не увеличена (КВР: 140 мм правая доля, 60 мм левая доля), умеренно повышенной эхогенности, диффузно неоднородной структуры, контуры ровные. Объемных образований не выявлено.
Желчный пузырь размерами 72х23х26 мм, стенки уплотнены, тонус снижен, деформирован неполной перетяжкой в воронке, содержимое с хлопьевидной взвесью. Холеход не расширен, до 3 мм, без включений в просвете. Ширина воротной вены 11 мм.
Поджелудочная железа: головка 24 мм, тело 12 мм, хвост 22 мм, повышенной эхогенности, диффузно неоднородной структуры, контуры ровные, частично размытые из-за метеоризма. Ворсунгов проток визуализируется в виде тонкой гиперэхогенной линии.
Почки: правая опущена на 3,5-4 см, левая расположена типично, размерами в пределах 112х50 мм, паренхима 16-18 мм, обычной структуры,контуры ровные. Синусы повышенной эхогенности, не расширены, сосуды визуализируются в виде линейных
гиперэхогенных включений без акустических теней. Конкрементов нет. Надпочечники не визуализируются.
Селезенка размерами 95х42 мм, обычной формы и структуры. Ширина селезеночной вены 6 мм. Лимфоузлы в воротах печени и селезенки, парааортальные и паракавальные размерами 6х4 мм (доступные исследованию), обычной структуры и эхогенности.
Заключение: УЗ-картина диффузных изменений печени и поджелудочной железы, нельзя исключить хронический холецистит, с явлениями ДЖВП. Эхопризнаки правостороннего нефроптоза, умеренных структурных изменений в синусах. Объемных образований не выявлено.
ПЭТ/КТ от 10.11.2014
На серии КТ и реконструированных ПЭТ (от основания черепа до середины бедра определяются очаги патологического накопления 18F-ФДГ в отдельных участках по периферии опухолевого конгломерата в переднем средостении с макс SUV 30,75 (наиболее выражено-в передне-левых отделах конгломерата). Образование размерами около 4,7х3,7х5,4 см, с аметаболическим центром, соответствующим центральной зоне некроза по КТ.
Другие очаги патологического накопления РФП не выявлены.
В средостении определяются единичные мелкие лимфоузлы до 0,5 см, без накопления РПФ. Лимфоузлы надключичных зон не визуализируются.
Правая и левая доли щитовидной железы, перешеек, а также слюнные железы (поднижнечелюстная и околоушные) с обеих сторон не увеличены. Увеличенных лимфоузлов в мягких тканях шеи не выявлено.
В легких определяются единичные очаги до 0,6 см, без накопления РПФ, без динамики при сравнении с КТ от 21.08.2014. Корни не расширены. Плевральные синусы свободны, жидкости нет.
Печень в размерах не увеличена, контуры ровные и четкие. Структура паренхимы однородная, без видимых патологических изменений. Селезенка не увеличена, контуры ровные и четкие, внутренняя структура однородная. Панкреатический проток не расшире. Надпочечники не увеличены, без явных узловых образований. Положение, форма и размеры почек не изменены. Контуры ровные, четкие структура однородная. Увеличенные лимфоузлы брюшной полости, забрюшинного пространства и малого таза не определяются.
Отмечается повышенное накопление РПФ в отдельных петлях тонкой кишки на уровне S1-2 позвонков.
Деструктивных изменений по КТ и очагов патологического накопления РПФ в костяхне выявлено. Отмечается повышенное накопление РПФ в костном мозге реактивного характера.
Отмечается физиологическое выведение РПФ по мочевыводящим путям, физиологическое накопление в миокарде, мышцах фонации, лимфоидной ткани ротоглотки.
Заключение: на момент исследования получены данные о наличии активной остаточной опухолевой ткани в конгломерате лимфоузлов в переднем средостении.
Спасибо!!!
Источник
Рак легкого является ведущей причиной смерти от рака во всем мире и обусловливает 1,59 миллионов смертей в год. Несмотря на прогресс, достигнутый в лечении пациентов, страдающих этой болезнью, пятилетняя выживаемость все еще остается невысокой, составляя приблизительно 15–16%. Основным фактором риска развития рака является табакокурение, повышающим вероятность его возникновения более чем в десять раз по сравнению с некурящими людьми. Другими состояниями, при которых повышен развития новообразования, являются идиопатический легочный фиброз и воздействие канцерогенов, например, асбеста.
Правильное определение стадии является крайне важным и необходимым моментом, позволяющим правильно спланировать лечение и оценить выживаемость. У больных раком легких является методом выбора при определении стадии опухоли, более эффективным, чем другие лучевые методы, такие как КТ или рентгенография. Благодаря возможности одновременной оценки анатомических и функциональных изменений, ПЭТ-КТ позволяет добиться большей точности по сравнению с ПЭТ и КТ в отдельности.
Этот метод диагностики позволяет более четко определить первичную опухоль, отличить опухолевую ткань от участков ателектаза и фиброзных изменений, расположенных рядом. Доказана высокая эффективность в оценке состояния лимфоузлов, а также обнаружения отдаленных метастазов. Также была подтверждена ценность этого метода как инструмента прогнозирования выживаемости путем оценки метаболизма в опухоли при первичном исследовании и в определении раннего (промежуточного) и завершающего ответа на химиотерапию. В последних литературных источниках этот метод был упомянут как рекомендуемый с экономической точки зрения.
Что такое ПЭТ-КТ?
ПЭТ-КТ является комбинированным методом визуализации, позволяющим совместить информацию об анатомических изменениях, полученную с помощью КТ, и данные об изменениях метаболизма, полученные при использовании ПЭТ; при этом исследовании существует возможность просмотра данных методов по отдельности, либо при наложении друг на друга на трехмерных реконструкциях или плоских (двухмерных) срезах. Чаще всего применяется радиофармпрепарат F18-фтордезоксиглюкова (ФДГ), использование которого позволяет обнаружить как первичную опухоль, так и метастазы. Это происходит потому, что большинство патологических очагов злокачественной природы в легких захватывают глюкозу, и видны на сканах в виде ярких участков. При ПЭТ-КТ обычно не используются йодсодержащие контрастные средства, в то же время возможно дополнительное КТ-сканирование с применением контрастных веществ. Использование йодсодержащего контрастного вещества улучшает визуализацию сосудов средостения и позволяет лучше определить их отношение к опухоли, помогает также оценить средостение и плевру, дает возможность исключить сопутствующую тромбоэмболию легочной артерии (если была выполнена КТ-ангиопульмонография).
Стадии рака легкого
В первичном обследовании пациента, страдающего раком легкого, должны принимать участие несколько специалистов: опытный рентгенолог, специалист по ядерной медицине (радионуклидным методам — сцинтиграфии и ПЭТ), рентгенохирург (специалист в области интервенционной радиологии), пульмонолог, торакальный хирург; необходимо также использовать точные и экономически эффективные методы диагностики. Существующие на данный момент руководства содержат рекомендации, что методы нужно выполнять любому пациенту, у которого имеется высокий риск рака, предпочтительно с выполнением гистологического исследования и взятием образцов ткани. Это позволяет не только установить точный гистологический вариант опухоли, но и правильно стадировать заболевание. Во многих случаях предпочтительнее выполнить биопсию подозрительных лимфоузлов средостения, а не первичной опухоли, что позволяет лучше оценить стадию (например, при биопсии лимофузла с выполнением ПЭТ ставится стадия T2N2, в то время как без ее использования – T2Nx). Кроме того, для опухолей, осложненных обструктивной пневмонией, и образований с выраженными некротическими изменениями, данные играют важную роль для определения области биопсии.
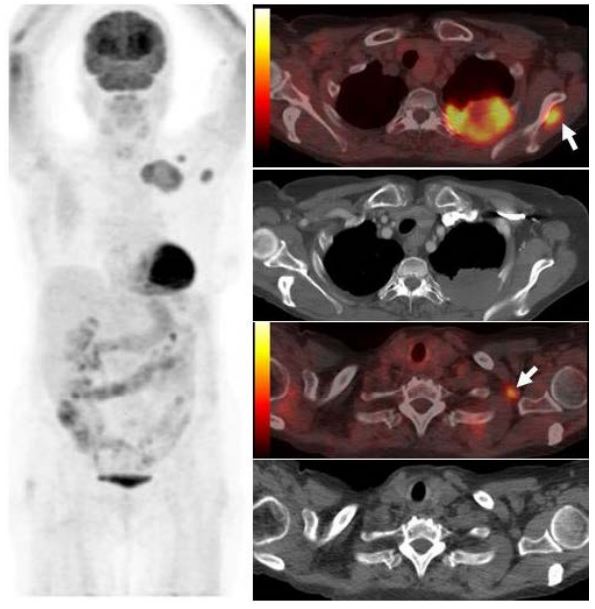
Опухоль левого легкого с частичным некрозом и деструкцией ребер. Визуализируются два метастаза в подключичных лимфоузлах и в мышцах (стрелки), которые на КТ не видны. Необходимо выполнить трансторакальную биопсию той части опухоли, которая расположена в периферических отделах, чтобы получить образец жизнеспособных тканей.
Варианты рака легкого
В 85–95% случаев рак легкого является немелкоклеточным и представляет собой аденокарциному, плоскоклеточный рак или крупноклеточный рак. Аденокарцинома может возникать как у курящих, так и некурящих пациентов; обычно представляет собой периферическую опухоль; рано дает отдаленные метастазы. Степень захвата аденокарциномой F18-ФДГ имеет тенденцию быть ниже по сравнению с опухолями иного гистологического строения; некоторые опухоли, характеризующиеся низким уровнем метаболизма глюкозы, могут обуславливать ложноотрицательный результат.
Плоскоклеточный рак тесно связан с курением, в большинстве случаев является центральным. Крупноклеточный рак обычно представляет собой периферическое объемное образование в легочной ткани большого размера с наличием метастазов на момент установления диагноза. Крупноклеточный и плоскоклеточный рак характеризуются повышенным накоплением F18-ФДГ. Стадирование немелкоклеточного рака легкого осуществляется в соответствии со шкалой TNM; таким образом, информация о стадии заболевания дает возможность планирования лечения и прогнозирования выживаемости.
Остальные 10–15% случаев обусловлены мелкоклеточным раком, биологически более агрессивным, при котором стадирование, лечение и прогноз отличаются от таковых при немелкоклеточном раке. Этот тип рака очень тесно связан с курением. Выделяют две стадии заболевания: ограниченную, при которой опухоль располагается в половине грудной клетки на стороне поражения, в том числе в средостении и ипсилатеральной надключичной области; и распространенную, когда опухоль распространяется за пределы одной половины грудной клетки. Поскольку мелкоклеточный рак легочной ткани в корне отличается от немелкоклеточного, его диагностика при помощи будет обсуждаться в специально отведенной главе в конце этой статьи.
Визуализация первичной опухоли: Т-стадия
С помощью КТ можно достоверно оценить размер опухоли практически во всех случаях. Тем не менее, при наличии обусловленных опухолью осложнений, например, ателектаза легкого или обструктивной пневмонии, истинный размер первичной опухоли оценить сложнее. Позволяет отличить паренхиму спавшегося участка легочной ткани от злокачественной опухоли, т. к. опухоль характеризуется интенсивным захватом ФДГ, а спавшееся легкое — нет. Также он помогает оценить опухолевую инвазию (прорастание) в плевру и средостение. Накопление плеврой ФДГ всегда является патологическим, и при наличии новообразования органов дыхания крайне подозрительно на метастатическое поражение. При прорастании опухоли в средостение необходимо выполнять КТ с внутривенным введением йодсодержащего контрастного вещества с целью определения взаимоотношения опухоли, крупных кровеносных сосудов и перикарда.
Интенсивный захват ФДГ первичной опухолью обусловлен ее биологическим типом и степенью «агрессивности» опухолевых клеток; повышенный захват ФДГ может становиться прогностическим фактором рецидива. В исследовании Kim et al. была продемонстрирована группа пациентов, подвергшихся оперативному вмешательству по поводу новообразований легких, у которых при патологическом исследовании была установлена стадия N0. У пациентов, у которых возник рецидив опухоли, максимальный стандартизированный уровень накопления (SUV max) первичной опухолью легкого был выше, чем у пациентов, у которых рецидива не было. Пороговое значение SUV max, отделяющее пациентов с высоким уровнем рецидива, было определено равным 6,9. Было также сделано заключение, что для пациентов высокой группы риска по развитию рецидива предпочтительна изначально более «агрессивная» терапия. Таким образом, помогает точно спрогнозировать, как будет вести себя опухоль после лечения.
ПЭТ-КТ лимфоузлов: N-стадия
С помощью ПЭТ можно обнаружить метастатическое поражение лимфоузлов корней легких и средостения лучше, чем с помощью любого другого метода, так как метаболически активные лимфоузлы при ПЭТ-КТ, даже малого размера, характеризуются повышенным захватом ФДГ. Это справедливо и для тех случаев, когда морфологические признаки злокачественного поражения узлов могут не обнаруживаться на КТ-изображениях. Также метод позволяет оценить увеличенные лимфоузлы, не накапливающие или минимально накапливающие радиофармпрепарат, которые часто носят реактивный характер или отражают остаточные изменения в отсутствие опухолевого поражения. При определении стадии N чувствительность составляет 81% против 61% у КТ, и специфичность 90%, в то время как КТ характеризуется специфичностью 79%.
Наибольшее преимущество в оценке средостения — это возможность исключить злокачественное поражение любого лимфоузла с высокой степенью точности. То есть, отсутствие интенсивного захвата ФДГ лимфоузлом достоверно говорит об истинном отсутствии метастазов (прогностическое значение отрицательного результата равно 99%). В то же время не все лимфоузлы средостения, характеризующиеся повышенным метаболизмом, обязательно являются злокачественными; ложноположительный результат может быть обусловлен воспалительными изменениями. Это объясняет, почему изменения со стороны средостения должны оцениваться количественно с использованием SUV (стандартизированного уровня накопления). Пороговое значение SUV max в пределах 4,0–5,3 позволяет рассматривать изменения со стороны лимфоузлов средостения как положительные (то есть, метастатическое поражение есть).
Лучшее картирование лимфоузлов средостения позволяет избежать медиастиноскопии, ограничившись трансбронхиальной игольной аспирацией под контролем УЗИ, особенно в труднодоступных областях, таких как аортопульмональное окно или область, находящаяся позади бифуркации трахеи.
Особенное значение в стадировании поражения лимфатических узлов имеет на ранних стадиях заболевания (I и II), что позволяет избежать ненужной торакотомии.
Оценка метастазов: M-стадия
У 40–50% пациентов, страдающих раком органов дыхания, в момент установления диагноза присутствуют метастазы. Наличие отдаленных метастазов в корне меняет план лечения этих пациентов, делая оперативное вмешательство намного более сложным, что приводит к гораздо более неблагоприятному прогнозу. ПЭТ-КТ имеет неоспоримые преимущества в диагностике метастазов по сравнению с традиционными методами исследования, особенно в случаях одновременного метастатического поражения множества органов, часто без какой-то определенной локализации вследствие диссеминации процесса. Повышенное накопление ФДГ в метастазах рака легкого и возможность исследования всего тела делают методом выбора при выявлении метастазов (вне головного мозга). Также метод позволяет выявить отдаленные метастазы, о которых до проведения исследования ничего не было известно, вплоть до 30% всех случаев.
Самые частые вторичные изменения при раке легкого – метастазы в кости, которые имеют место у 8–27% пациентов на момент установления диагноза. Вторичные изменения костей лучше обнаруживаются при помощи ПЭТ, чем при использовании других методов диагностики. Так, больше чем в половине случаев костных метастазов поражается только костный мозг и не происходит существенного нарушения костной структуры, из-за чего при помощи рентгенографии и КТ их не удается обнаружить, и даже сцинтиграфия скелета с использованием метилендифосфоната Tc-99m оказывается малоспецифичной при обнаружении этого типа поражений. Метастазы в кости могут иметь исключительно литический характер и интенсивно накапливать ФДГ, но в то же время гиперфиксация препарата в очагах поражения может и не определяться.
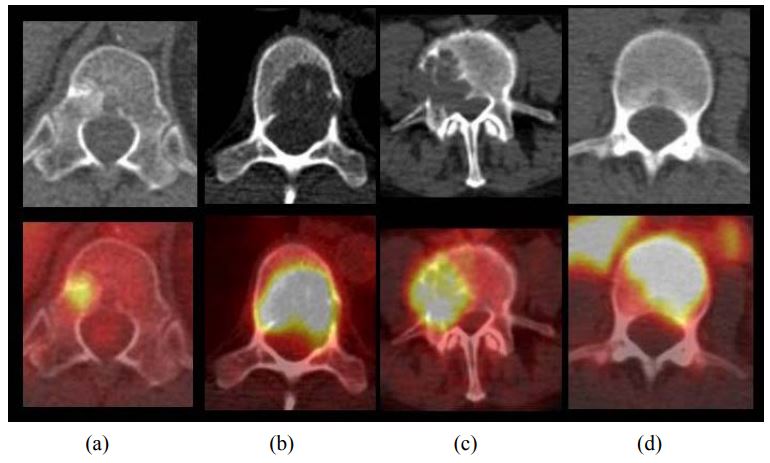
Типы метастазов в кости при раке легкого. (a) Остеобластический. (b) Остеолитический. (c) Смешанный. (d) Поражение костного мозга.
У пациентов, страдающих раком легкого, часто возникают метастазы в органы брюшной полости. Чаще всего поражаются печень и надпочечники. Поскольку также могут встречаться доброкачественные изменения печени и надпочечников, необходимо использовать диагностические методы, позволяющие распознать их и отличить от метастазов. В случаях изменений со стороны надпочечников, умеренное или выраженное накопление ФДГ обладает высокой прогностической ценностью положительного результата для метастазов. Чувствительность и специфичность ПЭТ с использованием SUV (стандартизированного уровня накопления) в целом в популяции составляет 87% и 87%, в то время как у пациентов с раком легкого 94% и 82% соответственно. Лучшим пороговым значением SUV max, позволяющим дифференцировать злокачественные и доброкачественные поражения, по-видимому, является 2,5.
В случаях метастазов в печень, практически все доброкачественные поражения (кисты, гемангиомы, фокальная нодулярная гиперплазия) характеризуются меньшим или идентичным по сравнению с паренхимой печени уровнем накопления ФДГ. Любой узел, любые объемные образования, накапливающие ФДГ интенсивнее, чем нормальная паренхима печени, крайне подозрительны на злокачественные изменения.

Метастазы в печени при аденокарциноме правого легкого. Определяется один метастаз в печени, который не виден на КТ с контрастным усилением.
Для обнаружения метастазов в надпочечники, почки и кости, в случаях, когда невозможно проведение, приемлемой альтернативой является МРТ всего тела с выполнением программы DWI. Позволяет оценить метастазы в областях, изменения в которых не стадируются при традиционных методах диагностики, например, в коже, скелетных мышцах, мягких тканях, поджелудочной железе, почках.
Второе мнение по ПЭТ-КТ
Необходимым условием достоверного определения стадии злокачественного новообразования является правильная оценка результатов ПЭТ-исследования. При неоднозначных или противоречивых результатах рекомендуется получить второе мнение специализированного радиолога. Повторный экспертный анализ исследования в профильном центре позволяет избежать ошибки интерпретации снимков, сделать более обоснованные выводы о стадии процесса, наличии или отсутствии метастазов, вторичных очагов в лимфатических узлов. Это исключительно важно и планировании тактики операции, химио- и лучевого лечения.
Стадирование метастазов в головной мозг
Даже несмотря на то, что вторичные изменения головного мозга не так часто встречаются у пациентов с раковыми опухолями легких, они имеют большое значение, поскольку их наличие приводит к высокому уровню заболеваемости и смертности, чего в некоторых случаях можно избежать или минимизировать путем подбора соответствующего лечения. Поскольку головной мозг характеризуется высоким базовым метаболизмом глюкозы, вторичные очаги в нем могут быть замаскированы, а чувствительность ПЭТ-исследования в обнаружении метастазов – ограничена. В связи с этим, в соответствии с существующими на данный момент протоколами рекомендуется дополнительное использование МРТ. В случаях, когда провести МРТ невозможно, можно сделать КТ с внутривенным контрастным усилением. Это дает схожие результаты с МРТ головного мозга.
Одновременное присутствие легочной и внелегочной опухоли
У 1–8% пациентов, страдающих раком легкого, на момент установления диагноза обнаруживается рак иной локализации. Большинство этих новообразований также тесно связаны с табакокурением. И, действительно, у 6,5% хронических курильщиков, которым была выставлена та или иная стадия рака любого типа, на момент установления диагноза обнаруживался одновременно существующий рак других органов и систем.
В случаях множественного рака используемые диагностические критерии являются следующими:
- Оба очага гистологически различны.
- Гистологический тип один и тот же, но нет поражения лимфоузлов и экстраторакальных метастазов.
На основании этих критериев, частота синхронного множественного рака легкого, описанная в литературе, составляет 0,5–3,3%. Наиболее часто одновременно существующие раковые опухоли, обнаруживаемые у пациентов, страдающих раком легкого, располагается в молочных железах, в голове и шее, пищеводе и щитовидной железе. Более чем 80% этих синхронных поражений обнаруживаются на ранней стадии, что предполагает возможность лечения, устраняющего причину заболевания. Тем не менее, возможность лечения в значительной степени зависит от того, насколько далеко зашла раковая опухоль на момент установления диагноза.
ПЭТ-КТ: планирование лучевой терапии
Возможность ПЭТ различить метаболически активную ткань опухоли от ателектаза, обструктивной пневмонии или фиброзных изменений имеет решающее значение в определении объема опухоли. Это очень полезно при планировании лучевой терапии, так как позволяет скорректировать форму и размер облучаемого объема тканей и уменьшить степень облучения непораженных опухолью органов (например, пищевода, сердца, спинного мозга), находящихся вблизи опухоли. Кроме того, использование ПЭТ значительно изменяет поле облучения по сравнению с КТ. Так, использование ПЭТ в дополнение к традиционным методам диагностики приводило к изменению объема облучаемых тканей более чем у 20% пациентов, и изменение стадии происходило в 20–50% случаев. В различных источниках описывается, что изменения планируемого целевого объема достигают 50% у пациентов с немелкоклеточным раком.
Контроль лечения и прогноз рака легкого
Наиболее важный прогностический фактор опухоли, подвергаемой хирургическому лечению — это степень ее диссеминации на время установления диагноза. В случает отсутствия метастазов пятилетняя выживаемость равна 57–67%; в случае вторичного поражения лимфоузлов ворот легкого — 47% , при поражении лимфоузлов средостения на стороне, противоположной опухоли — 23%. Обнаружение отдаленных метастазов является одним из основных критериев невозможности удаления опухоли хирургическим путем. Ввиду важности изложенных фактов особое значение принимает второе мнение по ПЭТ.
Василий Вишняков, врач-радиолог
При подготовке текста использованы материалы:
Читать по теме:
Может ли ПЭТ-КТ ошибаться?
ПЭТ-КТ при раке молочной железы
Кандидат медицинских наук, член Европейского общества радиологов
Источник