Созревание и дифференцировка т лимфоцитов в тимусе
Т-лимфоциты несут на себе поражающее воображение разнообразие рецепторов, позволяющее распознавать практически любые чужеродные субстанции, с которыми может столкнуться организм. Путь от гемопоэтической стволовой клетки к 107–109 клонов Т-лимфоцитов с уникальными антиген-связывающими последовательностями — удивительное достижение эволюции. Многостадийное развития Т-лимфоцитов может выглядеть пугающим и запутывающим со страниц учебников. Однако, если вы дадите ему второй шанс, вы увидите, что это красивый и слаженный процесс.
Как и остальные клетки крови, Т-лимфоциты берут свое начало в костном мозге от гемопоэтической стволовой клетки. Такие клетки-предшественницы имеют мало общего со зрелыми функциональными Т-лимфоцитами: они не имеют антигенных рецепторов (TCR) и не умеют узнавать чужеродные антигены. Их ждет сложный путь развития, который осилят немногие, однако те, которые выживут, создадут армию, готовую к любой угрозе. Для развития Т-лимфоцитов в нашем теле формируется специальный орган — тимус. Создав достаточный репертуар рецепторов, тимус подвергается инволюции и практически не детектируется после пубертатного периода. Численность Т-лимфоцитов во взрослом организме в основном поддерживается делением зрелых клеток.
Для миграции в тимус клетки, чья судьба — стать Т-лимфоцитом, используют хемокиновый рецептор CCR9, лиганд для которого — CCL25 — секретируют клетки тимуса. Достигнув тимуса, предшественники Т-лимфоцитов становятся тимоцитами. Первым делом они получают сигнал от эпителиальных клеток тимуса через рецептор Notch-1, который окончательно определяет их судьбу в пользу Т-лимфоцита.
Следующая задача тимоцитов — активная пролиферация. Скорость деления тимоцитов крайне высока, поскольку 95 %–98 % этих клеток погибает. Дело в том, что судьба развивающегося Т-лимфоцита по умолчанию — апоптоз, спасти от которого его может только успешное прохождение нескольких раундов отбора. Сигнал для первого раунда деления — интерлейкин 7, который выделяют эпителиальные и другие клетки тимуса. Мутации в гене ИЛ-7 или его рецептора приводят к тяжелым иммунодефицитам. Пролиферация приводит к созданию большого пула клеток, которые называют дважды негативными клетками, поскольку они не несут на себе корецепторы CD4 и CD8. Большинство из них (90 %) дадут начало αβ Т-лимфоцитам, а 10 % — γδ Т-лимфоцитам.
После этого тимоциты приступают к перестройке генов антигенных рецепторов. Это тот самый момент, когда из небольшого количества генов возникает всё разнообразие антигенных рецепторов — миллионы и миллиарды. В ходе этого процесса участки генов антигенных рецепторов перестраиваются случайным образом. Ключевое слово здесь — случайный, поскольку процесс формирования рецепторов, способных эффективно распознавать чужеродные антигены, никак не зависит от этих антигенов и происходит задолго до встречи с ними!
До сих пор тимоциты содержали гены TCR в зародышевой конфигурации, т. е. не подвергшиеся перестройке. Такие гены не могут образовать TCR. Тимоциты начинают с перестройки генов одной из двух цепей TCR — β-цепи. После этого тимоциты проходят через первую контрольную точку. В случае успешной перестройки клетка экспрессирует β-цепь, которая вместе с инвариантной α-цепью формирует на поверхности клетки pre-TCR. Такой рецептор активируется без участия лиганда и передает в клетку сигналы для дальнейшего развития. Остальные клетки не проходят отбор: в случае неудачной перестройки pre-TCR не экпрессируется и клетка подвергается апоптозу в отсутствие сигналов к выживанию.
Активация pre-TCR поставляет в клетку важные сигналы для дальнейшего развития:
- Останавливается перестройка локуса β-цепи во втором аллеле. Это называется аллельное исключение — зрелые Т-лимфоциты экспрессируют β-цепь TCR только с одного аллеля.
- Начинается экспрессия двух ко-рецепторов CD4 и CD8, теперь тимоциты называются дважды позитивными.
- Начинается второй раунд пролиферации. Через pre-TCR клетки получают мощный сигнал к делению, приводящий к еще более интенсивной экспансии, чем в первом раунде.
- После этапа деления запускается перестройка α-цепи рецептора.
В отличие от цепи-партнера, α-цепь может подвергаться многократной перестройке, и большинство тимоцитов успешно с ней справятся. После перестройки α-цепи тимоциты наконец экспрессируют на своей поверхности полный αβ TCR. Однако впереди главная проверка, пройти которую суждено немногим.
Задачи последнего этапа отбора:
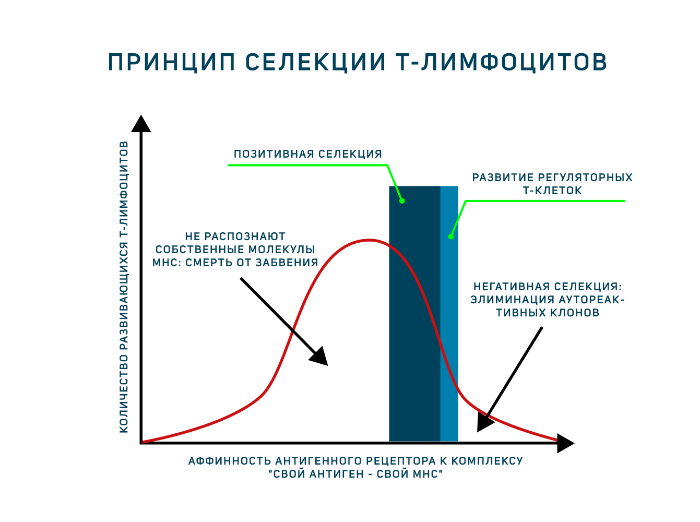
- Отобрать клетки, распознающие молекулы главного комплекса гистосовместимости (MHC) организма. Этот этап присутствует в развитии тимоцитов, поскольку зрелые Т-лимфоциты способны распознавать антигены только в составе МНС. Поэтому они должны знать МНС своего организма в лицо. Это называется позитивная селекция.
- Элиминировать клетки, распознающие собственные антигены. Это называется негативная селекция.
Однако антигенпрезентирующие клетки тимуса (эпителиальные клетки тимуса, дендритные клетки и макрофаги) располагают только комплексами «свой МНС — свой антиген». И позитивная, и негативная селекция осуществляется на основании взаимодействия TCR с такими комплексами! Для объяснения была предложена гипотеза аффинности. Тимоциты, чьи антигенные рецепторы проявят низкую аффинность к таким комплексам, продолжат развитие. Тимоциты, чьи рецепторы свяжутся с представленными антиген-МНС комплексами прочно, подвергнутся апоптозу как аутореактивные клоны (клональная делеция). Клетки, не распознающие МНС вовсе, т. е. не прошедшие позитивную селекцию, умрут особым способом, который называется смерть от забвения (death by neglect). Ещё один вариант развития — среднее связывание рецептора с антигенным комплексом, такие тимоциты могут дать начало регуляторным Т-клеткам. Таким образом, регуляторные Т-клетки — единственные лимфоциты, которые взаимодействуют со своим будущим антигеном в процессе развития! Развитию этого подтипа Т-лимфоцитов сейчас посвящено много исследований.

Особую роль в негативной селекции играет белок AIRE (аутоиммунный регулятор), который заставляет клетки тимуса экспрессировать в небольших количествах антигены, в норме присутствующие только в определенных тканях. Это позволяет сформировать толерантность к тканеспецифичным антигенам, встречающимся только за пределами тимуса. Мутация в белке AIRE приводит к развитию аутоиммунного полиэндокринного синдрома. AIRE содержится в эпителиальных клетках медуллы. При этом известно, что наиболее эффективно негативная селекция осуществляется при презентации антигена дендритными клетками и макрофагами, а не стромой тимуса. В новом исследовании был показан перенос антигенов из эпителиальных клеток тимуса в дендритные клетки, которые их и презентируют!
Одновременно с позитивной и негативной селекцией осуществляется проверка, соответствует ли корецептор распознаваемому классу МНС — т. е. происходит дифференцировка в функциональные подклассы. Выживают только клетки с правильной комбинацией: CD8 + MHC I — цитотоксические Т-лимфоциты и CD4 + MHC II — Т-хелперы.
Последнее, что должен сделать лимфоцит перед тем, как покинуть тимус — это изменить тип сигналинга через антигенный рецептор. Если незрелые Т-лимфоциты с высоким родством к антигену погибают, то зрелые — активируются (молекулярные основы такой принципиальной разницы не ясны). Теперь лимфоциты готовы заселить периферические лимфоидные органы и нести оборону. Зрелые Т-лимфоциты покидают тимус, используя градиент сфингозин-1-фосфата, — липида, присутствующего в высоких концентрациях в крови и лимфе, для хемотаксиса в кровяное русло. Для хоуминга во вторичные лимфоидные ткани они используют CD62L (L-селектин).
γδ Т-лимфоциты несут менее разнообразные антигенные рецепторы, по-видимому, не зависящие от МНС. Они не экспрессируют корецепторы CD4, CD8. γδ Т-лимфоциты выступают в роли первой линии обороны против часто встречающихся бактерий в эпителиальных и слизистых тканях и скорее относятся ко врожденной иммунной системе, чем к адаптивной.
Источники:
- Kenneth Murphy, Casey Weaver. Janeway’s Immunobiology 9th edition. Garland Science, 2017.
- Abul Abbas, Andrew H. Lichtman, Shiv Pillai. Cellular and Molecular Immunology 9th Edition. Elsevier, 2017.
- Perry J. S. et al. CD36 Mediates Cell-Surface Antigens to Promote Thymic Development of the Regulatory T Cell Receptor Repertoire and Allo-tolerance //Immunity. – 2018. – 923-936.
Нашли опечатку? Выделите фрагмент и нажмите Ctrl+Enter.
Источник
Стволовая гемопоэтическая клетка, мигрирующая в тимус,
превращается (дифференцируется) под влиянием тимического микроокружения в
Т-лимфоцит. Цель дифференцировки:
- обучить распознаванию чужеродного
материала, попавшего в организм, и его разрушению (т. е. осуществлению
киллинг-эффекта); - создать толерантность по отношению к собственным (self)
антигенам. тимус играет главную роль в этих процессах, поскольку является тем
органом, где про¬исходит антигеннезависимая дифференцировка Т-клеток и создание
(генерирование) чрезвычайно разнообразного набора (репертуара)
антигенраспознающих Т-клеточных рецепторов.
Вначале стволовая гемопоэтическая клетка попадает в корковую
зону тимуса и превращается в ранний предшественник Т-лимфоцита. Фенотип этой
клетки следующий: ТАГРР-альфа, бета +, CD3+ CD4-, CD8-, т. е. характеризуется
наличием Т-клеточного распознающего рецептора, в составе которого имеются
альфа- и бета-цепи, CD3 структура, но отсутствуют молекулы CD4 и CD8.
Далее, здесь же в корковой зоне тимуса, под влиянием тимического
микроокружения, гормонов тимуса и, особенно, ИЛ-7 ранний предшественник
Т-лимфоцита превращается в незрелый Т-лимфоцит, фенотип которого следующий:
ТАГРР-альфа, бета +, CD3+, CD4+, CD8+. Набор таких мембранных структур говорит
о том, что данная клетка способна: 1) распознать любой антиген с помощью
ТАГРР-альфа, бета; 2) после распознавания передать сигнал внутрь клетки для ее
активации с помощью CD3 структуры: 3) превратиться как в CD4+ (хелпер), так и в
CD8+ (киллер) клетки при развитии эффекторного звена иммунного ответа.
На следующем этапе
дифференцировки незрелый предшественник Т-лимфоцита переходит в мозговое
вещество тимуса, где завершается тимический этап созревания. При этом
происходят два важнейших события: 1) индуцируется толерантность к аутоантигенам;
таким образом, минимизируется возможность развития аутоиммунного заболевания;
2) происходит разделение Т-лимфоцитов на две субпопуляции: CD4+CD8- (хелперы) и
CD4-CD8+ (киллеры) (не нужно за-бывать, что на их мембране сохраняются молекулы
ТАГРР-альфа, бета и CD3). Этот этап также реализуется при важном участии ИЛ-7.
Покидая тимус, зрелые покоящиеся Т-лимфоциты, которые
находятся в G(O) стадии клеточного цикла, расселяются в Т-зоны периферических
лимфоидных органов. Такие Т-лимфоциты характеризуется следующими свойствами:
- способностью распознавать чужеродные антигены, которые презентируются ему в
виде пептида с помощью молекул ГКГ класса I и класса II, и развивать
эфферентную часть иммунного ответа; - неспособностью распознавать большинство
аутологичных антигенов, как в растворимой форме, так и в виде молекул на
мембране клеток. Это главное препятствие на пути к развитию аутоиммунного
ответа.
Часть Т-лимфоцитов, покидающих тимус, все же способна распознавать
аутоантигены, однако такие Т-лимфоциты (и В-лимфоциты) либо подвергаются делении
(разрушению) в периферических органах, либо находятся в состоянии анергии
(неспособности к активации и реализации эфферентной части иммунного ответа).
Т-лимфоциты-хелперы (CD4+ клетки) представлены тремя
субпопуляциями: т. н. нулевыми Т-хелперами (Тх0), которые дифференцируются в
Т-хелперы 1-го типа (Tx1) и 2-го типа (Тх2). В этой дифференцировке основную
роль играют ИЛ-12, ИЛ-2, гамма-интерферон, ИЛ-10, ИЛ-4, ИЛ-5.
Т-лимфоциты-хелперы (CD4+ клетки) участвует в распознавании
атигенногопептида , который презентируется с помощью молекул ГКГ класса П. В
этом случае для активации Т-лимфоцита необходим дополнительный,
костимуляционный, сигнал.
Источник