Регионарные лимфоузлы шейки матки

Пути метастазирования опухоли при раке шейки матки и тела матки. Лимфатическая система яичников.
Клинические наблюдения показывают, что чаше всего метастазы при раке шейки матки обнаруживаются в следующих шести группах лимфатических узлов, являющихся для шейки матки регионарными: околошеечных (парацервикальных), околоматочных (параметральных), запирательпых, внутренних подвздошных, наружных подвздошных и общих подвздошных. Значительно реже наблюдается метастазирова-ние рака шейки матки в околоаортальные и паховые лимфатические узлы. Перечисленные группы узлов, в свою очередь, могут быть подразделены на три подгруппы: первичная (околошеечные и околоматочные), промежуточная (наружные и внутренние подвздошные, запирательные) и вторичная подгруппа (общие подвздошные, околоаортальные и паховые лимфатические узлы).
Существует два основных пути лимфогенного метастазирования при раке шейки матки. Первый путь: от околошеечных и околоматочных узлов к наружным подвздошным и запирательным, а затем к околоаортальным и значительно реже — паховым лимфатическим узлам. Второй основной путь: от околошеечных и околоматочных узлов к внутренним подвздошным, а затем к общим подвздошным и околоаортальным лимфатическим узлам. Распространение раковых клеток может происходить как по одному из этих путей, так и по обоим, а также только с одной стороны или с обеих сторон одновременно (Papadia, 1958).
Общность лимфатической и венозной системы шейки матки и влагалища, а также тесный контакт между этими органами является анатомическим обоснованием нередкого распространения карциномы шейки матки на стенки влагалища.
Согласно клиническим данным, при раке шейки матки сначала поражаются внутренние подвздошные и подвздошные (общие и наружные), а затем околоаортальные лимфатические узлы; при раке тела матки в первую очередь поражаются околоаортальные и паховые лимфатические узлы; метастазирование при раке шейки матки происходит быстрее, чем при раке тела матки.
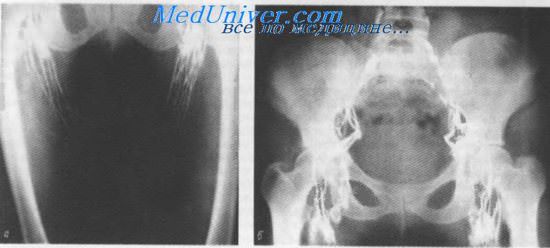
Лимфограмма. Глубокие лимфатические сосуды и узлы нижней конечности (а) и таза (б)
Лимфатическая система яичников
Лимфатические сосуды яичника на поверхности органа представлены в виде грубой сети. В воротах и в брыжейке яичника отводящие лимфатические сосуды образуют богатое подъяичниковое сплетение (plexus subovaricus); по выходящим из него 2—3 лимфатическим стволам лимфа оттекает в общие для яичника, тела матки и маточной трубы лимфатические узлы, расположенные по ходу яичниковых сосудов (nodi lymphatici ovarici) и далее — в регионарные лимфатические узлы; последние расположены преимущественно: слева— по левой полуокружности брюшной аорты, справа — по передней поверхности нижней полой вены.
Взаимоотношения лимфатических сосудов дна матки, яичников и маточной трубы также самые тесные. Отводящие лимфатические сосуды всех трех органов сливаются в упоминавшееся выше общее для них подъничниковое сплетение. Отток лимфы из матки, яичника и маточной трубы происходит в околоаортальные лимфатические узлы, в которые впадают также лимфатические сосуды и от органов брюшной полоста (Д. А. Жданов, 1952). Существует тесная связь путей оттока лимфы матки, мочевого пузыря и прямой кишки.
Хирургическая анатомия лимфатической системы матки имеет практическое значение и в связи с использованием в клинике метода предоперационного (прижизненного) окрашивания лимфатических узлов, например при операции Вертгейма (Е. В. Антипова, 1963; М. Марков, 1960).
Обнаружение метастазов в лимфатических узлах таза затруднено из-за огромного числа вариантов нормы; тем не менее, применение метода лимфографии перед операцией и во время последней имеет много преимуществ в связи с реальной возможностью более полного осуществления лимфаденэктомии. Методом лимфографии, выполнявшейся, в частности, после операции Вертгейма, было установлено, что в зоне иссечения лимфатических узлов последние контрастируются в тех случаях, когда удаление узлов было неполным, так как возможна частичная их регенерация. При тщательном же удалении лимфатических сосудов и узлов на большом протяжении последние не восстанавливаются и на лимфотраммах не обнаруживаются.
Восстановленные лимфатические узлы не достигают исходного состояния: они уменьшены в размерах, полигональны по форме и менее контрастны.
Лимфатические сосуды после операции Вертгейма теряют прямолинейность хода, образуют между собой многочисленные связи, не имеют четкообразных утолщений, становятся более извилистыми и чрезвычайно узкими. Ниже места резецированных лимфатических узлов и сосудов (паховая область, бедро) примерно в половине случаев образуется широкая сеть коллатералей, направляющихся к лимфатическим сосудам противоположной стороны. Основные лимфатические коллекторы бедра подвергаются редукции и деформации.
– Также рекомендуем “Расширенная абдоминальная экстирпация матки.”
Оглавление темы “Операции в гинекологии.”:
1. Хирургическое лечение трубного бесплодия
2. Сальпинго-сальпингоанастомоз. Техника сальпинго-сальпингоанастомоза.
3. Операция пересадки яичника в полость матки. Лимфатическая система матки.
4. Пути метастазирования опухоли при раке шейки матки и тела матки. Лимфатическая система яичников.
5. Расширенная абдоминальная экстирпация матки.
6. Основные этапы расширенной абдоминальной экстирпация матки.
7. Мочеточник. Хирургическая анатомия женского мочеточника.
8. Мочевой пузырь. Хирургическая анатомия женского мочевого пузыря.
9. Мочеиспускательный канал. Хирургическая анатомия женского мочеиспускательного канала.
10. Операции при недержании мочи. Операция прямой мышечной пластики сфинктера мочевого пузыря.
Источник
ГЛАВА 34 РАК ШЕЙКИ МАТКИ
ЭПИДЕМИОЛОГИЯ
Рак шейки матки – злокачественная эпителиальная опухоль, поражающая влагалищную часть шейки матки (portio vaginalis) или шеечный канал (canalis cervicalis) в
виде экзоили эндофитного образования. В настоящее время в мире ежегодно
регистрируется до 500 тыс. новых случаев рака шейки матки. Большинство
из них приходится на развивающиеся страны, тем не менее рак шейки матки
остается серьезной проблемой и для индустриально развитых стран.
В
России раком шейки матки ежегодно заболевают до 13 тыс. женщин. В 2007
г. абсолютное число больных с впервые в жизни установленным диагнозом
составило 13 419. За период с 1992 по 1997 г. показатели заболеваемости
колебались в пределах 10,5 на 100 тыс. женского населения. С 1998 г.
заболеваемость в РФ постепенно нарастала, достигнув в 2007 г. 17,6
женского населения. Летальность в 2007 г. была ниже (19,0 %), чем в 1997
г. (20,6 %). Средний возраст больных раком шейки матки – 45 лет, однако
заболевают им женщины как пожилого возраста, так и молодые. Рак шейки
матки остается одной из причин смерти женщин молодого возраста от
онкологических заболеваний.
ФАКТОРЫ РИСКА
Среди
факторов риска рака шейки матки – раннее начало половой жизни,
сексуальная активность, частая смена половых партнеров как самой
женщиной, так и мужчиной, венерические заболевания, вирусные инфекции,
среди которых наибольшее значение придается папилломавирусу (HPV),
курение, иммунодефицитные состояния, прием оральных контрацептивов и др.
ЭТИОЛОГИЯ И ПАТОГЕНЕЗ
В настоящее время доказано, что рак шейки матки связан с инфекционным агентом, передаваемым половым путем. Исследования
последних
лет показали, что 95 % рака шейки матки содержат разновидности HPV,
принадлежащие к так называемым типам высокого риска (HPV 16, 18, 31, 33,
45 и других серотипов), инфицированность в популяции здоровых женщин не
превышает 5-20 %. Основной путь передачи генитальной HPV-инфекции –
половые контакты. Попадая в организм, HPV локализуется в базальном
клеточном слое эпителия, который представляет собой популяцию делящихся
клеток. По мере эпителиальной дифференциации геном HPV проходит все
стадии продуктивной инфекции. Этот процесс завершается в зрелых
кератиноцитах. Такая форма инфекции приводит к цитопатическим эффектам,
проявляющимся в форме коилоцитоза, остроконечных кондилом.
В
большинстве случаев наблюдается достаточно длительная персистенция HPV
ДНК в клетках базального слоя эпителия. Дальнейшая динамика HPV-инфекции
может заключаться в регрессии либо, наоборот, в прогрессии,
сопровождающейся включением HPV ДНК в клеточный геном и появлением
характерных для злокачественной трансформации морфологических изменений
эпителия. Несмотря на высокую потенциальную опасность, HPV являются
условными патогенами. Носительство HPV свидетельствует не о
злокачественном процессе как таковом, а о многократно повышенном риске
возникновения последнего. Факторы, модифицирующие патогенность HPV и как
следствие провоцирующие опухолевый рост у инфицированных женщин,
остаются неизвестными.
В случае злокачественной
трансформации эпителий шейки матки проходит несколько этапов
внутриэпителиальных атипических изменений (предрак), предшествующих
инвазивному раку. Внутриэпителиальные атипические изменения
(цервикальная интраэпителиальная неоплазия – CIN) разделены на 3
степени: CIN I соответствует слабой дисплазии многослойного плоского
эпителия, CIN II – умеренной дисплазии и CIN III – выраженной дисплазии и
карциноме in situ. Средний возраст больных CIN на 10-15 лет меньше, чем при инвазивном раке шейки матки, т.е. 30-35 лет.
CIN
I и II могут самопроизвольно регрессировать в 60 % случаев, но в 30 %
отмечается прогрессия до CIN III в среднем в течение 3-5 лет. CIN III в
редких случаях также может регрессировать, но более чем в 60-70 %
прогрессирует в инвазивный рак в течение 3 лет.
По морфологическому строению плоскоклеточные формы рака шейки матки составляют 80-90 % случаев, железистые – 20-10 %.
Метастазирование. Регионарными
лимфатическими узлами являются лимфатические узлы таза:
парацервикальные, параметриальные, гипогастральные (внутренние
подвздошные, обтураторные), общие подвздошные, наружные подвздошные,
пресакральные, латеральные сакральные. Поражение других лимфатических
узлов, таких, как парааортальные, классифицируется как отдаленные
метастазы.
КЛИНИЧЕСКАЯ КЛАССИФИКАЦИЯ ПО СИСТЕМЕ TNM (2002) И МЕЖДУНАРОДНОЙ ФЕДЕРАЦИИ АКУШЕРОВ И ГИНЕКОЛОГОВ (FIGO, 1994)
При
раке шейки матки критерии выделения категорий Т и М соответствуют
стадиям FIGO. Ниже для сравнения приведены обе классификации (табл.
34.1).
Классификация FIGO основана на результатах
клинического обследования. Стадии TNM имеют как клинический, так и
патоморфологический вариант.
Правила классификации
Представленная
ниже классификация применима только для первичного рака шейки матки. В
каждом случае необходимо гистологическое подтверждение диагноза.
Анатомические области
1. Шейка матки.
2. Наружная часть шейки матки.
Регионарные лимфатические узлы
1. Околошеечные лимфатические узлы.
2. Лимфатические узлы параметрия.
3. Внутренние подвздошные лимфатические узлы, включая запирательные.
4. Наружные подвздошные лимфатические узлы.
5. Общие подвздошные лимфатические узлы.
6. Предкрестцовые лимфатические узлы.
7. Латеральные крестцовые лимфатические узлы.
Таблица 34.1. Классификация рака шейки матки TNM и Международной
Окончание табл. 34.1
Обратите внимание!
*
Буллезный отек слизистой оболочки не позволяет отнести опухоль к группе
Т4. Поражение слизистой оболочки мочевого пузыря и прямой кишки следует
доказывать путем биопсии.
Клиническая классификация TNM
Т – первичная опухоль
N – регионарные лимфатические узлы
? – состояние регионарных лимфоузлов оценить невозможно.
N0 – метастазов в регионарных лимфоузлах нет.
N1 – метастазы в регионарных лимфоузлах имеются.
М – отдаленные метастазы
Mх – недостаточно данных для определения отдаленных метастазов.
M0 – нет признаков отдаленных метастазов. М1 – имеются отдаленные метастазы.
Патоморфологическая классификация pTNM
Критерии выделения категорий рТ, рN и рМ соответствуют таковым для категорий Т, N и M.
С целью
патоморфологической оценки показателя N проводят удаление десяти тазовых
регионарных лимфатических узлов и более. В настоящее время принято, что
отсутствие характерных изменений ткани при патоморфологическом
исследовании биоптатов меньшего количества лимфатических узлов позволяет
подтвердить стадию
G – гистопатологическая дифференцировка
Ох – степень дифференцировки не может быть установлена.
G1 – высокая степень дифференцировки. G2 – средняя степень дифференцировки.
G3 – низкая степень дифференцировки или недифференцированные опухоли.
КЛИНИЧЕСКАЯ КАРТИНА
HPV-инфекция
и внутриэпителиальные неоплазии шейки матки не имеют специфических
симптомов заболевания. Женщину не беспокоят ни выделения из половых
путей, ни боли. Слизистая оболочка шейки матки не изменена или
выявляются доброкачественные образования в виде эрозированного
эктропиона, лейкоплакии и др.
Клиническая симптоматика
заболевания проявляется при прогрессировании опухолевого процесса в
инвазивные формы. У молодой женщины появляются кровянистые выделения
после половых контактов, ациклические маточные кровотечения; у женщин
старшего возраста – кровомазание и кровотечения в постменопаузе. В
дальнейшем кровянистые выделения из влагалища принимают зловонный
характер из-за распада опухоли (рис. 34.1, 34.2). Болевой синдром в
пояснице, крестце, по ходу седалищного нерва появляется при инфильтрации
опухоли в ткани малого таза. В связи со сдавлением мочеточников
появляются признаки нарушения оттока мочи. В случае прорастания опухолью
мочевого пузыря и прямой кишки развивается клиническая картина
«клоаки».
Рис. 34.1. Рак шейки матки
Рис. 34.2. Рак шейки матки. Биопсия опухоли
ДИАГНОСТИКА И ПРОФИЛАКТИКА
HPV
тестируется с помощью молекулярно-биологических исследований мазков с
шейки матки (ПЦР). Специфического лечения HPV-инфекции нет; предлагается
различного рода иммуномодулирующая терапия (индукторы интерферона и
др.). В настоящее время разработаны и внедряются в практику
профилактические вакцины против рака шейки матки как двухвалентные,
содержащие вирусоподобные вещества 16, 18 типов, так и четырехвалентные –
6, 11, 16, 18 типов. В некоторых странах уже приняты государственные
программы по профилактической вакцинации против рака шейки матки
подростков в возрасте 9-14 лет.
Предрак, или
внутриэпителиальная неоплазия шейки матки (ON различной степени
выраженности), выявляется при морфологическом исследовании
(цитологическом и гистологическом). Цитологическое исследование является
весьма чувствительным методом диагностики предрака (дисплазий) и
начального преклинического рака шейки матки (карциномы in situ, микроинвазивного
и скрытого инвазивного рака). Следовательно, если с помощью
цитологического метода обследовать всех женщин, то можно выявить больных
предраком и с начальными стадиями рака, которые хорошо поддаются
лечению, и таким образом предотвратить развитие инвазивного рака.
Выявление заболевания в преклинической фазе дает возможность излечения с
помощью «сберегательных» методов, позволяет сократить сроки лечения,
снизить показатели инвалидизации и смертности. ВОЗ рекомендует
цитологический скрининг для выявления ранних стадий рака шейки матки,
что позволит снизить смертность от этого заболевания. Цитологический
скрининг подразумевает обязательное ежегодное взятие мазков с шейки
матки и из цервикального канала для цитологического исследования у
женщин, начавших половую жизнь. При выявлении атипии проводится
углубленное обследование, включающее кольпоскопию с прицельной биопсией
патологических очагов для гистологического исследования. В случаях
диагностики предрака (CIN II, III) выполняется органосохраняющее лечение
в объеме конизации шейки матки с предварительным выскабливанием
цервикального канала. Конизация шейки матки может быть выполнена с
помощью скальпеля, электрохирургическим способом и посредством луча
лазера.
При клинической картине инвазивного рака шейки
матки (экзофитная или эндофитная опухоль с переходом на влагалище и
параметрий или без него), помимо общего и гинекологического осмотра с
обязательным ректовагинальным обследованием, стандартных лабораторных
исследований крови, функции почек и печени, рентгенографии легких,
показано УЗИ и КТ или МРТ брюшной полости и малого таза. КТ или МРТ
позволяют определить обструкцию почек, мочеточников, а также выявить
забрюшинные метастазы (размером >1 см), так как рак шейки матки
метастазирует преимущественно лимфогенно. Регионарными лимфатическими
узлами являются общие, наружные, внутренние подвздошные, запирательные и
крестцовые. При местно-распространенном процессе в малом тазу показаны
цистоскопия и ректороманоскопия для исключения прорастания опухоли в
мочевой пузырь и прямую кишку.
ЛЕЧЕНИЕ
В
лечении рака шейки матки используются хирургический и лучевой методы, а
также их комбинации. Хирургическое лечение применяется при
локализованных формах (I-IIA стадии). Лучевую терапию назначают при
местно-распространенном процессе (IIB- III стадии), в последние годы – в
сочетании с химиотерапией.
Хирургическое лечение
включает в себя операции различного объема: от сберегательных в виде
конизации шейки матки при 0 и IA стадиях, до сверхрадикальных –
экзентерации таза при IV стадии.
Первые операции по
поводу рака шейки матки были выполнены в Европе во второй половине XIX
века. Приоритет в разработке и внедрении радикальных хирургических
вмешательств при раке шейки матки принадлежит австрийскому
врачу-гинекологу E. Wertheim и датируется 1902 г. За столетие, прошедшее
с момента выполнения операции Э. Вертгеймом, она претерпела
значительные технические изменения. В настоящее время выполняют при
инвазивном раке шейки матки хирургические вмешательства 5 типов.
Экстрафасциальная экстирпация матки обозначена как операция I типа.
Модифицированная радикальная экстирпация матки (II тип) включает
удаление медиальной половины
кардинальных и
крестцово-маточных связок. Радикальная экстирпация матки (III тип),
описанная американским хирургом J. Meigs (1944), предусматривает
удаление большей части кардинальных, крестцово-маточных связок, верхней
трети влагалища и лимфатических узлов таза. При расширенной радикальной
экстирпации матки IV типа удаляются периуретральные ткани, резецируются
верхняя пузырная артерия и 3/4 влагалища. Операция
V типа, которая обозначается как частичная экзентерация,
предусматривает удаление дистальных отделов мочеточников и мочевого
пузыря и выполняется при прорастании опухоли в мочевой пузырь. Наиболее
частым интраоперационным осложнением при выполнении расширенной
гистерэктомии бывает ранение мочевого пузыря, мочеточников и крупных
сосудов; это осложнение устраняется во время операции. В раннем
послеоперационном периоде самые грозные осложнения – кровотечения,
эмболия легочной артерии и спаечная кишечная непроходимость.
Характерными отсроченными осложнениями операции Вертгейма являются
образование мочеточниково-влагалищных и пузырно-влагалищных свищей,
гипо- и атония мочевого пузыря и мочеточников с развитием восходящей
инфекции.
Одновременно с
развитием радикальной хирургии рака шейки матки наступает эра лучевой
терапии. Современные принципы лучевой терапии предусматривают
необходимость сочетанного воздействия внутриполостного и дистанционного
компонентов. Внутриполостная радиотерапия подразумевает непосредственное
контактное облучение опухоли радиоактивными источниками (цезием,
иридием, кобальтом и др.) на современных аппаратах, исключающих
облучение медицинского персонала. Целью дистанционной мегавольтной
терапии малого таза с помощью линейных ускорителей является облучение
зон регионарного лимфогенного метастазирования. Характерные осложнения
лучевой терапии – ранний и поздний цистит, ректит, энтероколит.
Сочетанная лучевая терапия это не только основной, но (чаще) и
единственно возможный метод лечения больных во ПВ-Ш стадии в связи с
невозможностью выполнения радикальной операции из-за
местно-распространенного опухолевого процесса. В настоящее время
проведение лучевой терапии при местнораспространенных стадиях
заболевания комбинируется с химиотерапией. Кроме того, лучевая терапия
может быть альтернативой хирургическому лечению у пациенток с I стадией
заболевания при высоком операционном риске.
Лечебная тактика в зависимости от стадии заболевания
• 0 стадия –
конизация шейки матки (электро-, лазерная или ножевая) с выскабливанием
цервикального канала. Экстирпация матки выполняется, если опухоль
распространяется за пределы края выполненного конуса или женщинам
пострепродуктивного возраста. При противопоказаниях к хирургическому
лечению рекомендуется только внутриполостная лучевая терапия до СОД
35-50 Гр на точку А.
Результаты лечения приближаются к 100 %.
• IA1 стадия – тотальная
гистерэктомия I типа. Сохранение яичников молодым женщинам. Как
исключение – выполнение конизации шейки молодым женщинам, желающим
сохранить фертильность, при условии опухольнегативных краев конуса. При
противопоказаниях к хирургическому лечению рекомендуется внутриполостная
лучевая терапия до СОД 50-60 Гр на точку А.
• IA2 стадия – радикальная
гистерэктомия с подвздошной лимфаденэктомией II типа. При
противопоказаниях к хирургическому лечению рекомендуется сочетанная
лучевая терапия с СОД 65-70 Гр на точку А и 40 Гр – на точку B.
• IB1 стадия – результаты
хирургического и лучевого лечения идентичны и достигают 85-90 %.
Молодым пациенткам предпочтительнее хирургическое лечение в объеме
радикальной гистерэктомии II типа с подвздошной лимфаденэктомией и
последующей послеоперационной дистанционной терапией в дозе 40 Гр на
точку B. При противопоказаниях к хирургическому лечению и пожилым
пациенткам проводится сочетанная лучевая терапия с СОД 65-70 Гр на точку
А и 40 Гр – на точку B.
• IB2 стадия – результаты
хирургического и лучевого лечения идентичны и достигают 75-80 %. При
выборе хирургического метода лечения рекомендуется неоадъювантная
химиолучевая терапия. Доза неоадъювантной лучевой терапии – до 20-30 Гр
на точку В в сочетании с цисплатиновой химиотерапией. Операция в объеме
радикальной гистерэктомии II-III типа с подвздошной лимфаденэктомией с
продолжением послеоперационного дистанционного облучения до СОД 40-50 Гр
на точку В.
Пожилым пациенткам или при противопоказаниях к хирургическому лечению назначается сочетанная лучевая терапия также
с
цисплатиновой химиотерапией. СОД составляет на точку А 70-75 Гр, на
точку В – 40-55 Гр. В пяти рандомизированных исследованиях показаны
более высокие результаты (на 10-15 %) при проведении химиолучевой
терапии, чем только лучевой. Химиотерапию назначают на фоне лучевой
терапии цисплатином в монорежиме (цисплатин – 40мг/м2 еженедельно до 6 нед) или в комбинации с 5-фторурацилом длительными инфузиями.
• IIA стадия – химиолучевая
терапия, как при IB2 стадии. У молодых пациенток предпочтительнее
комбинированное лечение с хирургическим компонентом после неоадъювантной
химиолучевой терапии, как при IB2 стадии с последующей адъювантной
лучевой терапией.
• IIB стадия – химиолучевая терапия. Молодым пациенткам показано проведение комбинированного лечения.
• III стадия – химиолучевая терапия.
• IV стадия – паллиативная
лучевая терапия. Химиотерапия цисплатином, капецитабином, ифосфамидом,
паклитакселом, иринотеканом и др. При IVA стадии может быть выполнена
операция тазовой экзентерации.
РЕЦИДИВЫ
При
рецидивах в малом тазу после хирургического лечения проводится лучевая
терапия. Применяется также химиотерапия цисплатином, капецитабином,
ифосфамидом, паклитакселом, иринотеканом и др.
Отдаленные результаты хирургического
лечения рака шейки матки в I стадии достигают 90 % случаев, при раке
шейки матки II стадии – 60-75 % в случае комбинации радикального
хирургического лечения с лучевой терапией. 5-летняя выживаемость больных
при
I стадии после сочетанной лучевой терапии достигает 85-90 %, при
II стадии – 45-75 % , при III стадии – 30-45 %.
Вопросы для самоконтроля
1. Приведите данные об эпидемиологии рака шейки матки.
2. Какая роль отводится инфицированию вирусом папилломы человека в этиологии рака шейки матки?
3. Какие факторы повышают риск возникновения рака шейки матки?
4. Какие существуют возможности профилактики рака шейки матки?
5. Какие выделяют морфологические варианты рака шейки матки?
6. Приведите
клиническую классификацию рака шейки матки по системе TNM и
Международную классификацию федерации акушеров и гинекологов.
7. Какие методы применяются в диагностике рака шейки матки?
8. Какие методы лечения рака шейки матки используются на современном этапе?
9. Как меняется лечебная тактика в зависимости от стадии заболевания?
10. Каков прогноз при раке шейки матки?
Источник