Региональные лимфоузлы толстого кишечника

Толстая кишка (термин толстый кишечник некорректен с точки зрения хирургии и топографической анатомии, однако широко используется в литературе) – это протяженный отрезок желудочно-кишечного тракта, включающий в себя:
- слепую кишку с аппендиксом,
- восходящую ободочную кишку,
- поперечную ободочную кишку,
- нисходящую ободочную кишку
- и сигмовидную кишку до прямой кишки.
Общая длина толстой кишки взрослого человека составляет от 1,5 до 2 метров. Злокачественные онкологические заболевания толстой кишки занимают третье место по распространенности среди раковых заболеваний.
Опухоли обычно называемые раком кишечника или колоректальным раком, включают несколько различных по строению, преимущественному расположению и течению злокачественных новообразований. Как правило, они представляют собой аденокарциномы – новообразования из клеток слизистой оболочки, продуцирующих слизь. Хирургическое лечение опухолей толстой кишки проводится врачами – колопроктологами, онкологами, хирургами.
Молекулярный анализ опухоли при раке кишки — новый шаг в лечении особо агрессивных опухолей. Европейская онкологическая клиника предоставляет своим пациентам возможность проведения высокотехнологичного теста опухоли на чувствительность к химиопрепаратам. На основании этого теста мы получаем очень эффективный план борьбы с раком, дающий максимально благоприятный шанс на выздоровление.
В каких отделах толстой кишки может развиваться рак?
Начальной частью толстой кишки является слепая кишка. Слепая кишка имеет вид купола, направленного вниз, от которого отходит червеобразный отросток — аппендикс. Немного выше в слепую кишку впадает конечный отдел тонкого кишечника — подвздошная кишка.
Слепая кишка находится в брюшной полости внизу справа — в подвздошной области. В месте впадения тонкой кишки слепая кишка заканчивается, и начинается восходящая ободочная кишка. Она имеет длину примерно 12 см, поднимается вверх до печени и делает изгиб, переходя в поперечную ободочную кишку.
Поперечная ободочная кишка расположена горизонтально, имеет длину 25–30 см. Она проходит справа налево, после чего делает изгиб и переходит в нисходящую ободочную кишку.
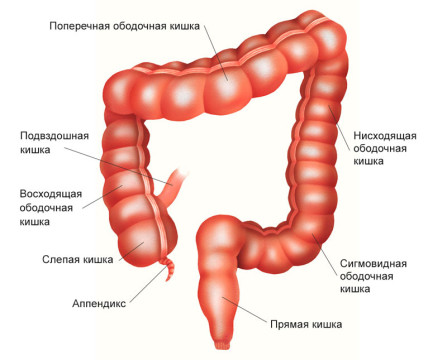
Нисходящая ободочная кишка имеет длину 10-30 см, проходит сверху вниз в левой части брюшной полости и переходит в сигмовидную ободочную кишку. Последняя, изгибаясь, переходит в прямую кишку — конечный отдел толстого кишечника.
Ширина просвета толстой кишки в разных отделах различается. В слепой кишке она в среднем составляет 7 см, а в сигмовидной — 4 см. Поэтому симптомы опухоли в конечных отделах толстого кишечника обычно нарастают быстрее.
Кто чаще страдает раком кишечника?
Чаще колоректальный рак (рак кишечника) встречается у людей старше 50-60 лет с примерно одинаковой частотой у мужчин и женщин. Наиболее часто поражается ободочная кишка. Повышают риск развития опухолей толстой кишки высококалорийная диета с большой долей животных жиров и небольшим содержанием грубой клетчатки и пищевых волокон, курение, хронические запоры, постоянный многомесячный прием нестероидных противовоспалительных средств, длительно существующие хронические воспалительные заболевания толстого кишечника – неспецифический язвенный колит, болезнь Крона, аденоматозный полип. Пациенты с имевшейся ранее злокачественной опухолью также имеют риск развития второй опухоли толстой кишки.
Метаболический синдром (комбинация артериальной гипертензии, висцерального ожирения, нарушений липидного и углеводного обмена) у мужчин способствует развитию рака толстого кишечника из-за нарушения гормонального баланса и процесса эпителизации толстой кишки. Около 10% случаев толсто-кишечных опухолей составляют наследственные формы, среди которых синдром наследственного неполипозного рака, обусловленный мутациями генов, отвечающих за репарацию ДНК, семейный аденоматозный полипоз, связанный с потерей гена FAP, и ряд других заболеваний.
Возможно ли что-то сделать для предупреждения развития рака толстой кишки?
Чтобы предупредить развитие злокачественной опухоли толстой кишки, особенно лицам старшей возрастной группы, рекомендуется вести здоровый образ жизни и придерживаться универсальных профилактических мероприятий – проходить ежегодное обследование (ректальное обследование, анализ кала на скрытую кровь, колоноскопия). На нашем сайте мы разместили подробный материал о скрининге рака толстой кишки.
Выявление предраковых изменений и злокачественных опухолей толстой кишки на ранних стадиях позволяет своевременно начать лечение. Ранняя диагностика и активное лечение, широко внедренные в широкую клиническую практику, позволили добиться высоких показателей пятилетней выживаемости – при первичном выявлении колоректального злокачественного новообразования на 1 стадии этот показатель составляет 90-93%, на 2 стадии – около 70-75%, на 3-й стадии – 40-48%. И несмотря на совершенствование методов лечения, выживаемость при первичном выявлении рака на 4-й стадии не превышает 5-9%.

Проведение колоноскопии позволяет диагностировать предраковые состояния и опухоли на ранних стадиях развития, своевременно выявлять злокачественные опухоли с помощью биопсии и гистологического исследования, а также быстро и малотравматично удалять полипы, склонные к «озлокачествлению» (малигнизации). В Европейской онкологической клинике активно используются методики хромоскопии, NBI-эндоскопии, которые позволяют уже во время диагностической эндоскопии с высокой степенью достоверности поставить диагноз предраковых изменений на начальной стадии и осуществить эндоскопическую внутрипросветную операцию резекции небольших опухолей без метастазов. Удаленный макропрепарат обязательно пройдет гистологическое, а при необходимости и иммуногистохимическое исследование. Такие диагностические и лечебные возможности позволяют быстро возвращать пациентов к активной жизни, а также убеждать пациентов из групп высокого риска проходить своевременное обследование, поскольку многих людей пугает перспектива колостомы, и они даже при наличии симптомов тянут с обращением за помощью.
Какие симптомы должны насторожить в отношении злокачественной опухоли толстого кишечника?
- Как правило, на ранних стадиях заболевания симптомы скудные: хроническая усталость, вялость, потеря интереса к жизни, общий дискомфорт в животе, необъяснимая потеря веса, гипохромная нормоцитарная анемия.
- На более поздних стадиях могут появиться упорные запоры, отвращение к пище, недержание газов или фекалий, кровь в стуле (могут быть как прожилки, так и существенное количество алой крови), болезненные позывы на неэффективные испражнения (тенезмы).
- При далеко зашедших опухолях может развиться хроническая или острая непроходимость кишечника. Симптомами этого опасного для жизни осложнения являются рези в животе, тошнота, рвота, иногда даже каловая, невозможность испражнения в сочетании с болезненными позывами на дефекацию.
- При распространении процесса по брюшине – канцероматозе брюшины — развивается асцит. При этом в брюшной полости накапливается жидкость, которая сдавливает внутренние органы и усугубляет тяжелое состояние больного.
В возрасте старше 50 лет сочетание даже невыраженного дискомфорта в области живота с гипохромной анемией (снижение гемоглобина и эритроцитов в общем анализе крови) в сочетании с повышением СОЭ и уровня лейкоцитов, а также положительным анализом кала на на скрытую кровь и повышением свертываемости крови должны в обязательном порядке повлечь за собой эндоскопическое исследование кишечника.
История пациентки с заболеванием толстой кишки
Существуют ли методы, на 100% гарантирующие точность диагностики рака толстой кишки?
Современный уровень эндоскопической техники при своевременном проведении позволяет диагностировать и типировать опухоли кишечника на самых ранних стадиях, при необходимости данные ректороманоскопии или колоноскопии с биопсией подозрительных участков могут быть дополнены проведением ректального УЗИ, ирригоскопии, УЗИ брюшной полости и малого таза. Эти исследования позволяют уточнить локализацию опухоли, степень её прорастания в близлежащие органы и ткани, наличие воспаления в окружающих тканях. Для получения всей полноты картины проводят МРТ и компьютерную томографию. Современные технологии позволяют при психологической невозможности выполнения колоноскопии провести так называемую виртуальную колоноскопию. Для диагностики наличия и локализации отдаленных метастазов используется ПЭТ-КТ (позитронно-эмиссионная томография).
Диагностика рака кишечника по анализу онкомаркеров
Онкомаркеры СА 19,9 и раково-эмбриональный антиген (РЭА) используются для скрининговой диагностики рака толстой кишки. Определение РЭА бывает полезным для предоперационного стадирования и наблюдения за больными с колоректальным раком после хирургического лечения. Как правило, на фоне прогрессирования болезни концентрация РЭА в сыворотке неуклонно растет.
Однако, повышение уровня онкомаркеров в скрининговом анализе крови не всегда означает наличие опухоли кишечника. Описаны многочисленные случаи впервые выявленного колоректального рака на поздних стадиях без существенного повышения этих показателей. Ведущими методами диагностики колоректального рака являются эндоскопические методы, а онкомаркеры используются в комплексе с другими лабораторными и клиническими показателями для оценки стадии процесса, эффективности лечения и стабильности ремиссии.
Согласно исследованиям, представленным 1 июля 2015 года на конгрессе Европейского общества медицинской онкологии (European Society for Medical Oncology World Congress on Gastrointestinal Cancer), при раке ободочной кишки средняя выживаемость среди пациентов с лишним весом на 2,5 месяца выше, чем у людей с субтильным телосложением и больных ожирением.
Особенности болезни при раке прямой кишки
Злокачественные опухоли прямой и толстой кишки часто объединяют общим термином “колоректальный рак”. Эти опухоли во многом схожи, однако, для них сильно различается лечение. в первую очередь это связано с большими различиями в технике хирургических вмешательств, так как прямая кишка, в отличие от ободочной и сигмовидной, находится в более ограниченном пространстве, в непосредственной близости от нее расположены другие органы (мочевой пузырь, матка, простата и др.). Причины, симптомы, диагностика и лечение рака прямой кишки рассмотрены в нашей отдельной статье – «рак прямой кишки».
Разновидности рака толстой кишки
Около 96% злокачественных опухолей толстой кишки представлены аденокарциномами. Они возникают в результате злокачественного перерождения железистых клеток слизистой оболочки, продуцирующих слизь. Когда произносят словосочетание «рак толстой кишки», как правило, имеют в виду именно аденокарциному толстой кишки. Существуют разные ее подтипы. Некоторые из них, такие как слизистая аденокарцинома и перстневидноклеточный рак, ведут себя более агрессивно и имеют более неблагоприятный прогноз.
Цены в Европейской онкологической клинике на лечение рака толстой кишки
- Консультация онколога — 5100 руб.
- Консультация химиотерапевта — 6900 руб.
- Восстановление непрерывности толстой кишки после ранее наложенной колостомы — 119700 руб.
- Фотодинамическая терапия при опухолевом стенозе толстой кишки (без стоиомости фотосенсибилизатора) — 178300 руб.
- Эндоскопическая резекция слизистой толстой кишки — 69000 руб.
В отдельном материале сайта мы подробно рассматриваем вопросы лечения рака толстой кишки.
Источник
Цель лечения: удаление опухоли ободочной кишки или уменьшение опухолевой массы.
Схемы лечения больных раком ободочной кишки в зависимости от стадии заболевания
1. Операция:
– полипэктомия;
– сегментарная резекция.
2. Лапароскопическая резекция ободочной кишки.
3. Наблюдение.
I стадия:
1. Операция – широкая резекция с наложением анастомоза (объем операции в зависимости от локализации опухоли).
2. Наблюдение.
1. Операция – широкая резекция с наложением анастомоза (объем операции в зависимости от локализации опухоли и распространенности опухолевого процесса).
2. Послеоперационная химиотерапия или лучевая терапия (при степени местного распространения опухоли, соответствующей Т4, и/или высокий риск, молодой возраст).
3. Наблюдение.
1. Операция – широкая резекция с наложением анастомоза (объем операции в зависимости от локализации опухоли и распространенности опухолевого процесса).
2. Послеоперационная лучевая терапия (при степени местного распространения опухоли, соответствующей Т4).
3. Адъювантная химиотерапия.
4. Наблюдение.
1. Операция (чаще паллиативная; при резектабельной опухоли и наличии солитарных и единичных метастазов в отдаленных органах – операция с одномоментным или отсроченным удалением метастазов).
2. После комбинированных операций:
– послеоперационная химиотерапия или лучевая терапия (химио-лучевая) при степени местного распространения опухоли, соответствующей Т4;
– адъювантная химиотерапия (при солитарных и единичных метастазах в отдаленных органах);
– наблюдение;
– симптоматическое лечение.
Немедикаментозное лечение: режим II, безшлаковая диета.
Патогенетическая тактика:
1. Проведение адъювантной полихимиотерапии после ранее проведенной радикальной операции. Обоснованием необходимости применения химиотерапии при раке ободочной кишки служит тот факт, что в момент выполнения 25-30% хирургических вмешательств, клинически оцениваемых как радикальные, уже имеются субклинические метастазы. В настоящее время 5-фторурацил в комбинации с лейковорином считается главным (базовым) химиотерапевтическим препаратом при колоректальном раке.
2. Проведение самостоятельной полихимиотерапии при наличии рецидива опухоли или метастазирования (прогрессирование, генерализация процесса).
3. Проведение самостоятельной химиотерапии при IV стадии заболевания (неоперабельные и генерализованные формы).
4. Клиническая тактика: химиотерапия при колоректальном раке применяется в качестве адъювантной терапии после хирургического или комбинированного лечения (операция + лучевая терапия), в комбинации с лучевой терапией и как самостоятельный метод лечения при распространенном процессе.
Химиотерапия должна начинаться сразу после восстановления пациента после операции, должна обязательно включать в себя фторпиримидины.
Схемы выбора: FOLFOX4, FOLFOX6, XELOX, FLOX, XELOX, кселода в монорежиме.
Лечение в адъювантном периоде должно длиться не менее 6 месяцев и не должно включать в себя иринотекан, бевацизумаб, цетуксимаб.
– кальция фолинат* 20 мг/м2, в/в струйно с последующим болюсом;
– фторурацила 425 мг/м2, в/в, с 1-го по 5-й дни.
Повторять курс каждые 4 недели до общих 6 курсов.
2. Roswell Park (недельный режим, высокие дозы):
– кальция фолинат* 500 мг/м2, в/в 2-часовая инфузия с последующим болюсом;
– фторурацила 500 мг/м2, в/в, еженедельно, 6 недель.
Повторять цикл каждые 8 недель (перерыв 2 недели) до общих 4 циклов.
3. De Gramont (упрощенный):
– кальция фолинат* 400 мг/м2, в/в 2-часовая инфузия с последующим болюсом;
– фторурацила 400 мг/м2 в/в и с последующей 46-часовой инфузией фторурацила 2400-3000 мг/м2 в/в.
Повторять курс каждые 2 недели.
– оксалиплатин 85 мг/м2 в/в, 2-часовая инфузия, в 1-й день;
– кальция фолинат* 200 мг/м2, в/в 2-часовая инфузия, в 1-й и 2-й дни;
– фторурацил 400 мг/м2, струйно, в/в, в 1-й и 2-й дни;
– фторурацил 600 мг/м2, в/в 22-часовая инфузия в 1-й и 2-й дни.
Повторять курс каждые 2 недели до общего количества 12 курсов.
5. FOLFOX6:
– оксалиплатин 100 мг/м2 в/в, 2-часовая инфузия, в 1-й день;
– кальция фолинат* 400 мг/м2, в/в 2-часовая инфузия, в 1-й день;
– фторурацил 400 мг/м2, струйно, в/в, в 1-й день;
– фторурацил 2400 мг/м2, в/в 46-часовая инфузия в 1-й день.
Повторять курс каждые 2 недели до общего количества 12 курсов.
– оксалиплатин 85 мг/м2 в/в, 2-часовая инфузия, в 1-й, 15-й, 29-й дни;
– кальция фолинат* 500 мг/м2, в/в струйно с последующим болюсом;
– фторурацила 500 мг/м2, в/в в 1-й, 8-й, 15-й, 22-й, 29-й дни.
Повторение цикла каждые 8 недель (перерыв 2 недели).
– оксалиплатин 135 мг/м2 в/в, капельно в 1-й день;
– капецитабин 2000 мг/м2/сут., внутрь в два приема в день (утром/вечером), с 1-го по 14-й дни.
Повторение курса каждые 3 недели, в течение 6 месяцев.
8. Капецитабин 1250 мг/м2, внутрь, дважды в день, с 1-го по 14-й дни. Повторять курс каждый 21 день до общего количества 8 курсов. В случае развития явлений токсичности доза может быть редуцирована до 850-1000 мг/м2, внутрь, дважды в день, с 1-го по 14-й дни, для уменьшения риска токсичности без снижения клинической эффективности.
9. Тегафур 800-1000 мг/м2 внутрь в два приема ежедневно до суммарной дозы 30 г. Повторение курса через 2 недели.
10. УФТ 400 мг/м2 внутрь в два приема ежедневно в течение 3-4 недель. Повторение курса через 1-2 недели.
* В режимах, включающих в себя фторпимидины, наравне с кальция фолинатом возможно применение его биоэквивалента натрия фолината.
Химиотерапия метастатического процесса
Выбор схемы для I линии терапии зависит от степени выраженности клинических симптомов: мало выраженные клинические симптомы – монотерапия фторпиримидинами либо оксалиплатин+фторпиримидины, иринотекан ± фторпиримидины; при выраженных клинических симптомах – оксалиплатин + фторпиримидины, иринотекан+фторпиримидины, иринотекан+ оксалиплатин, оксалиплатин+ иринотекан+фторпиримидины.
Режимы: клиники Мейо, Roswell Park, De Gramont, FOLFOX4, FOLFOX6, FLOX, XELOX, в монорежиме капецитабин, тегафур, УФТ.
– иринотекан 125 мг/м2, в/в в течение 90 минут, 1 раз/нед., 4 недели (в 1, 8, 15, 22-й дни);
– кальция фолинат* 20 мг/м2, в/в, струйно, 1 раз/нед., 4 недели (в 1, 8, 15, 22-й дни);
– фторурацил 500 мг/м2, в/в, 1 раз/нед., 4 недели (в 1, 8, 15, 22-й дни).
Повторять курс каждые 6 недель.
2. Модифицированный IFL (режим Saltz):
– иринотекан 125 мг/м2, в/в, в течение 90 минут, 1 раз/нед., 2 недели (в 1-й и 8-й дни);
– кальция фолинат* 20 мг/м2, в/в, струйно, 1 раз/нед., 2 недели (в 1-й и 8-й дни);
– фторурацил 500 мг/м2, в/в, 1 раз/нед., 2 недели (в 1-й и 8-й дни).
Повторять курс каждые 3 недели.
– иринотекан 180 мг/м2, в/в 90 минут в 1-й день;
– кальция фолинат* 400 мг/м2, в/в 2 часа, 1-й день;
– фторурацил 400 мг/м2, в/в, струйно, 1-й и 2-й дни;
– фторурацил 2400 мг/м2, в/в, 46-часовая инфузия.
Повторять курс каждые 2 недели.
– оксалиплатин 130 мг/м2, 1-й день;
– кальция фолинат* 400 мг/м2, в/в 2 часа в 1-й день, затем фторурацил 2400 мг/м2, в/в 46-часовая инфузия.
Повторять курс каждые 2 недели.
– оксалиплатин 85 мг/м2, в/в 2 часа в 1-й, 15-й и 29-й дни;
– кальция фолинат* 20 мг/м2, в/в струйно с последующим болюсом в 1-й, 8-й, 15-й, 22-й, 29-й и 36-й дни;
– фторурацила 500 мг/м2, в/в в 1-й, 8-й, 15-й, 22-й, 29-й и 36-й дни.
Повторение цикла каждые 8 недель.
– оксалиплатин 100 мг/м2, 1-й день;
– кальция фолинат* 400 мг/м2, 1 дн., 2-х часовая инфузия;
– фторурацил 3000 мг/м2, в/в, в/в 46-часовая длительная инфузия.
Повторять курс каждые 2 недели.
– оксалиплатин 130 мг/м2, в/в, 1-й день;
– капецитабин 1000 мг/м2, внутрь, дважды в день, с 1-го по 14-й дни.
Повторять курс каждые 3 недели.
– оксалиплатин 70 мг/м2, в/в капельно, 1-й и 8-й дни;
– капецитабин 1000 мг/м2, внутрь, дважды в день, с 1-го по 14-й дни.
Повторять курс каждые 3 недели.
– иринотекан 200-250 мг/м2, в/в 90-минутная инфузия в 1-й день;
– капецитабин 1000 мг/м2, внутрь, дважды в день, с 1-го по 14-й дни.
Повторять курс каждые 3 недели.
– оксалиплатин 85 мг/м2, в/в, 1-й день;
– иринотекан 200 мг/м2, 1-й день.
Повторять курс каждые 3 недели.
– иринотекан 180 мг/м2, в/в 90-минутная инфузия в 1-й день;
– кальция фолинат* 200 мг/м2, в/в 2-часовая инфузия в 1-й и 2-й дни;
– фторурацил 400 мг/м2, в/в, струйно 1-й и 2-й дни;
– фторурацил 600 мг/м2, в/в, 22-часовая инфузия в 1-й и 2-й дни.
Повторять курс каждые 2 недели.
– иринотекан 80 мг/м2, в/в 2-часовая инфузия, 1-й день;
– кальция фолинат* 500 мг/м2, в/в 2-часовая инфузия в 1-й день;
– фторурацил 2000 мг/м2, в/в 24-часовая инфузия, еженедельно, 4 недели.
Повторение цикла через 2 недели.
– иринотекан 165 мг/м2, в/в, в 1-й день;
– оксалиплатин 85 мг/м2, в 1-й день;
– кальция фолинат* 200 мг/м2, в/в 2-часовая инфузия в 1-й день;
– фторурацил 3200 мг/м2, в/в 48-часовая инфузия.
Повторение курса каждые 2 недели.
– митомицин С 5 мг/м2, 1 раз в 3 нед. или 10 мг/м2, 1 раз в 6 недель;
– капецитабин 2000 мг/м2/сут., в два приема, с 1-го по 14-й дни, 3 недельный цикл.
– УФТ (тегафур+урацил) 250 мг/м2/сут., ежедневно, внутрь, с 1-го по 14-й дни;
– кальция фолинат* 90 мг/м2/сут., ежедневно, внутрь, с 1-го по 14-й дни.
Повторение курса каждые 3 недели.
16. Иринотекан в монорежиме:
- иринотекан: 125 мг/м2, в/в, в течение 90 минут, еженедельно, в течение 4 недель. Повторять каждые 6 недель;
- иринотекан: 125 мг/м2, в/в, в течение 90 минут, еженедельно, в течение 2 недель. Повторять каждые 3 недели;
- иринотекан: 175 мг/м2, в/в, в 1-й и 10-й дни. Повторять каждые 3 недели;
- иринотекан: 350 мг/м2, в/в, в 1-й день. Повторять каждые 3 недели.
*В режимах, включающих в себя фторпимидины, наравне с кальция фолинатом возможно применение его биоэквивалента натрия фолината.
Примечание. При достижении резектабельности метастаза(ов) первичной или рецидивной опухоли хирургическое лечение может быть выполнено не ранее чем через 3 недели после последнего введения химиопрепаратов.
Таргетная терапия метастатического процесса
В лечении распростарненного рака ободочной кишки, метастатического или рецидивного, оптимальным является сочетание цитостатиков с моноклональными антителами (таргетной терапией).
Бевацизумаб – моноклональные антитела к VEGF (эндотелиальный фактор роста). Назначается в качестве 1-й и 2-й линии лекарственной терапии до прогрессирования процесса.
Режимы:
| Схема химиотерапии | Схема таргетной терапии |
| FOLFOX | Бевацизумаб 5,0 мг/кг, в/в, 30-90 минутная инфузия, 1 раз в 2 недели |
| FOLFIRI | |
| IFL | |
| De Gramon | |
| Rosvell Park | |
| XELOX | Бевацизумаб 7,5 мг/кг, в/в, 30-90 минутная инфузия, 1 раз в 3 недели |
| XELIRI |
Примечание. При достижении резектабельности метастаза(ов) первичной или рецидивной опухоли оперативное лечение может быть выполнено не ранее чем через 6 недель после последнего введения бевацизумаба.
Цетуксимаб – моноклональные антитела к EGFR (рецепторы эпидермального фактора роста). Назначается при немутантном («диком», «wild») типе гена K-ras (KRAS) больным с распространенным процессом. В монорежиме рекомендован для III и IV линии терапии. В I и II линиях назначается в комбинации с химиопрепаратами.
Комбинация цетуксимаба и иринотекана у резистентных к химиотерапии (в том числе и к иринотекану) больных с «диким» типом K-ras – стандарт лечения.
Режимы:
| Схема химиотерапии | Схема таргетной тарпии |
| FOLFOX | Цетуксимаб: - стартовая доза 400 мг/м2, 2-часовая инфузия - затем 250 мг/м2, в/в, 1-часовая инфузия еженедельно |
| САPOX | |
| FOLFIRI | |
| XELIRI | |
| UFT/LV | |
| Иринотекан 350мг/м2, в/в, 1-й день. Повторять курс каждые 3 недели. | |
| Монорежим | |
| XELOX | Цетуксимаб не назначается |
| FLOX |
Панитумумаб – моноклональные антитела к EGFR. На момент разработки данных Протоколов не зарегистрирован в Республике Казахстан.
Примечание. Сочетание моноклональных антител к EGFR и к VEGF ухудшает результаты лечения и допустимо только в рамках специальных исследований.
Другие виды лечения
Послеоперационная лучевая терапия показана при степени местного распространения колоректального рака, соответствующей Т4 (распространение опухоли на стенки живота), через 3-4 недели после комбинированных операций.
Лучевая терапия проводится в конвенциальном (стандартном) или конформном режиме облучения в статическом многопольном режиме РОД 2-2,5-3,0 Гр до СОД 40-60 Гр на зону врастания опухоли. При проведении лучевой терапии возможно применение препаратов, защищающих организм от лучевого повреждения.
Облучение проводят на гамма-терапевтических аппаратах или линейных ускорителях.
Хирургическое вмешательство
Основным методом лечения рака ободочной кишки является хирургический.
Принципы радикальной операции:
1. Дистальный и проксимальный края отсечения кишки должны быть на достаточном расстоянии от опухоли, чтобы при микроскопическом исследовании они не содержали опухолевых клеток.
2. Вместе с опухолью должны быть удалены все регионарные лимфатические узлы.
3. Объем и характер хирургического вмешательства зависят от ряда факторов, важнейшими из которых являются локализация опухоли, степень распространенности процесса, наличие или отсутствие осложнений основного заболевания.
4. При расположении опухоли в правой половине ободочной кишки (червеобразный отросток, слепая кишка, восходящая ободочная кишка, печеночный изгиб, правая половина поперечной ободочной кишки) показана правосторонняя гемиколэктомия.
5. Если опухоль локализуется в левой половине поперечной ободочной кишки, селезеночном изгибе, нисходящей ободочной кишке, проксимальной части сигмовидной кишки, выполняют левостороннюю гемиколэктомию.
6. При небольших опухолях, локализующихся в средней части поперечной ободочной кишки, возможна ее резекция. При расположении опухоли в средней и нижней части сигмовидной кишки показана ее резекция.
7. При осложненном течении опухолевого процесса (кишечная непроходимость, перфорация опухоли и др.) может быть выполнена обструктивная резекция ободочной кишки с последующим возможным восстановлением непрерывности толстой кишки.
8. При распространении опухоли толстой кишки в прилежащие органы и ткани, показано проведение комбинированных операций, а при наличии солитарных и единичных метастазов (в печени, легких, яичниках и т.д.) – одномоментное или отсроченное их удаление.
9. Критерием радикально выполненной операции является гистологическое заключение об отсутствии злокачественного роста:
– в дистальном и проксимальном краях отсечения кишки;
– по окружности резецированного сегмента кишки (периферический клиренс).
10. При нерезектабельных опухолях толстой кишки и множественных метастазах в отдаленных органах по показаниям необходимо выполнение паллиативных операций (формирование обходных анастомозов, наложение колостом).
Профилактические мероприятия
Факторы риска:
1. Питание – малошлаковая пища с преобладанием животных жиров, белков и рафинированных углеводов (сахар).
2. Малоподвижный образ жизни (гипокинезия, ожирение, возраст старше 50 лет).
3. Курение, злоупотребление алкоголем.
4. Нестероидные противовоспалительные препараты.
5. Хронические воспалительные заболевания кишечника (болезнь Крона, неспецифический язвенных колит), нарушение моторики кишечника (запоры).
6. Отягощенный семейный анамнез раком желудочно-кишечного тракта. Семейный аденоматозный полипоз.
7. Злокачественная опухоль в анамнезе.
8. Метаболический синдром (сахарный диабет, артериальная гипертензия, увеличение объема живота) у мужчин.
Первичная профилактика: здоровый образ жизни, регулирование режима питания, формирование «групп риска».
Обнаружение аденоматозных полипов, на фоне которых развивается большинство опухолей, наряду с хорошим прогнозом при ранних стадиях делает колоректальный рак идеальным кандидатом для проведения скрининга.
– первый год – 1 раз в 3 мес.;
– второй год – 1 раз в 6 мес.;
– в последующем, пожизненно – 1 раз в год.
- физикальное;
- лабораторное (по показаниям);
- ирригоскопия (по показаниям);
- колоноскопия (по показаниям);
- рентгенологическое исследование легких;
- МРТ, КТ органов брюшной полости и забрюшинного пространства;
- ПЭТ;
- ультразвуковое исследование брюшной полости, забрюшинного пространства;
- другие методы исследования (компьютерная томография, экскреторная урография и т.д.) и консультации специалистов (гинеколог, уролог и др.) по показаниям.
Индикаторы эффективности лечения и безопасности методов диагностики и лечения, описанных в протоколе
Удовлетворительное состояние при условии отсутствия осложнений и заживления п/о раны.
Данные, свидетельствующие об отсутствии признаков прогрессирования процесса, полученные клиническими и/или визуализирующими методами исследования, а также повышение качества жизни больного.
Источник