Рак матки и яичников лимфоузлов

Пути метастазирования опухоли при раке шейки матки и тела матки. Лимфатическая система яичников.
Клинические наблюдения показывают, что чаше всего метастазы при раке шейки матки обнаруживаются в следующих шести группах лимфатических узлов, являющихся для шейки матки регионарными: околошеечных (парацервикальных), околоматочных (параметральных), запирательпых, внутренних подвздошных, наружных подвздошных и общих подвздошных. Значительно реже наблюдается метастазирова-ние рака шейки матки в околоаортальные и паховые лимфатические узлы. Перечисленные группы узлов, в свою очередь, могут быть подразделены на три подгруппы: первичная (околошеечные и околоматочные), промежуточная (наружные и внутренние подвздошные, запирательные) и вторичная подгруппа (общие подвздошные, околоаортальные и паховые лимфатические узлы).
Существует два основных пути лимфогенного метастазирования при раке шейки матки. Первый путь: от околошеечных и околоматочных узлов к наружным подвздошным и запирательным, а затем к околоаортальным и значительно реже — паховым лимфатическим узлам. Второй основной путь: от околошеечных и околоматочных узлов к внутренним подвздошным, а затем к общим подвздошным и околоаортальным лимфатическим узлам. Распространение раковых клеток может происходить как по одному из этих путей, так и по обоим, а также только с одной стороны или с обеих сторон одновременно (Papadia, 1958).
Общность лимфатической и венозной системы шейки матки и влагалища, а также тесный контакт между этими органами является анатомическим обоснованием нередкого распространения карциномы шейки матки на стенки влагалища.
Согласно клиническим данным, при раке шейки матки сначала поражаются внутренние подвздошные и подвздошные (общие и наружные), а затем околоаортальные лимфатические узлы; при раке тела матки в первую очередь поражаются околоаортальные и паховые лимфатические узлы; метастазирование при раке шейки матки происходит быстрее, чем при раке тела матки.
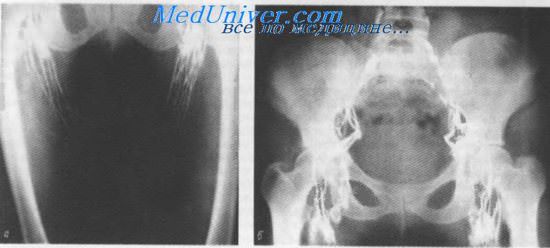
Лимфограмма. Глубокие лимфатические сосуды и узлы нижней конечности (а) и таза (б)
Лимфатическая система яичников
Лимфатические сосуды яичника на поверхности органа представлены в виде грубой сети. В воротах и в брыжейке яичника отводящие лимфатические сосуды образуют богатое подъяичниковое сплетение (plexus subovaricus); по выходящим из него 2—3 лимфатическим стволам лимфа оттекает в общие для яичника, тела матки и маточной трубы лимфатические узлы, расположенные по ходу яичниковых сосудов (nodi lymphatici ovarici) и далее — в регионарные лимфатические узлы; последние расположены преимущественно: слева— по левой полуокружности брюшной аорты, справа — по передней поверхности нижней полой вены.
Взаимоотношения лимфатических сосудов дна матки, яичников и маточной трубы также самые тесные. Отводящие лимфатические сосуды всех трех органов сливаются в упоминавшееся выше общее для них подъничниковое сплетение. Отток лимфы из матки, яичника и маточной трубы происходит в околоаортальные лимфатические узлы, в которые впадают также лимфатические сосуды и от органов брюшной полоста (Д. А. Жданов, 1952). Существует тесная связь путей оттока лимфы матки, мочевого пузыря и прямой кишки.
Хирургическая анатомия лимфатической системы матки имеет практическое значение и в связи с использованием в клинике метода предоперационного (прижизненного) окрашивания лимфатических узлов, например при операции Вертгейма (Е. В. Антипова, 1963; М. Марков, 1960).
Обнаружение метастазов в лимфатических узлах таза затруднено из-за огромного числа вариантов нормы; тем не менее, применение метода лимфографии перед операцией и во время последней имеет много преимуществ в связи с реальной возможностью более полного осуществления лимфаденэктомии. Методом лимфографии, выполнявшейся, в частности, после операции Вертгейма, было установлено, что в зоне иссечения лимфатических узлов последние контрастируются в тех случаях, когда удаление узлов было неполным, так как возможна частичная их регенерация. При тщательном же удалении лимфатических сосудов и узлов на большом протяжении последние не восстанавливаются и на лимфотраммах не обнаруживаются.
Восстановленные лимфатические узлы не достигают исходного состояния: они уменьшены в размерах, полигональны по форме и менее контрастны.
Лимфатические сосуды после операции Вертгейма теряют прямолинейность хода, образуют между собой многочисленные связи, не имеют четкообразных утолщений, становятся более извилистыми и чрезвычайно узкими. Ниже места резецированных лимфатических узлов и сосудов (паховая область, бедро) примерно в половине случаев образуется широкая сеть коллатералей, направляющихся к лимфатическим сосудам противоположной стороны. Основные лимфатические коллекторы бедра подвергаются редукции и деформации.
– Также рекомендуем “Расширенная абдоминальная экстирпация матки.”
Оглавление темы “Операции в гинекологии.”:
1. Хирургическое лечение трубного бесплодия
2. Сальпинго-сальпингоанастомоз. Техника сальпинго-сальпингоанастомоза.
3. Операция пересадки яичника в полость матки. Лимфатическая система матки.
4. Пути метастазирования опухоли при раке шейки матки и тела матки. Лимфатическая система яичников.
5. Расширенная абдоминальная экстирпация матки.
6. Основные этапы расширенной абдоминальной экстирпация матки.
7. Мочеточник. Хирургическая анатомия женского мочеточника.
8. Мочевой пузырь. Хирургическая анатомия женского мочевого пузыря.
9. Мочеиспускательный канал. Хирургическая анатомия женского мочеиспускательного канала.
10. Операции при недержании мочи. Операция прямой мышечной пластики сфинктера мочевого пузыря.
Источник
Как возникает рак матки?
Рак всегда начинается с клеток — основы для формирования тканей. Из тканей состоят все органы тела человека, в том числе и матка. Здоровые клетки растут и делятся, чтобы появились новые клетки. Когда здоровые клетки стареют или повреждаются, они умирают, а их место занимают новые клетки. Но иногда этот процесс нарушается. Новые клетки начинают расти даже когда организм в них не нуждается, или же например старые и поврежденные клетки перестают умирать. Когда новых лишних клеток становится слишком много, формируется образование из ткани, которое и называется опухолью.
Доброкачественные опухоли матки, например, миомы, полипы, эндометриоз:
- не представляют угрозу для жизни;
- обычно могут быть удалены и не вырастают снова;
- не врастают в соседние органы и ткани;
- не распространяются в другие части тела
Злокачественные опухоли матки:
- представляют угрозу для жизни;
- обычно могут быть удалены и не вырастают снова;
- могут врастать и повреждать соседние ткани и органы, например, влагалище;
- могут распространяться в другие части тела.
Раковые клетки могут распространяться в другие части тела от самой опухоли матки. Они могут добираться до соседних лимфоузлов по лимфатическим сосудам. По кровеносным сосудам клетки переносятся к легким, печени, костям или головному мозгу. Клетки опухоли могут прикрепляться к другим тканям и начинать расти уже там, образовывать новые опухоли, которые точно также могут повреждать ткани. В разделе «Стадии» подробно написано о распространенном раке эндометрия.
Факторы риска рака эндометрия
Если у вас или ваших близких диагностирован рак эндометрия, совершенно естественно интересоваться и беспокоиться: что могло вызвать такое заболевание? Очень часто врачи просто не могут объяснить, почему у одной женщины появляется рак эндометрия, а у другой нет.

Но врачи знают, что существуют определенные факторы риска, которые могут с большей вероятностью привести к развитию рака матки. Среди них:
- Чрезмерный рост ткани эндометрия (гиперплазия эндометрия: патологическое увеличение числа клеток, которыми выстлана поверхность матки является фактором риска развития рака эндометрия. Гиперплазия сама по себе не является раком, но иногда может перерождаться в злокачественную опухоль. Частыми симптомами этого состояния являются: тяжелые и обильные менструации, кровянистые выделения между менструациями и кровотечения после менопаузы. Гиперплазия эндометрия — нередкое состояние у женщин старше 40 лет.
- Ожирение: Женщины с увеличенной массой тела больше подвержены риску развития рака эндометрия.
- Репродуктивный и менструальный анамнез: женщины, у которых никогда не было детей, женщины, у которых менструации начались до 12 лет, женщины, у которых менструации продолжались после 55 лет.
- Прием ТОЛЬКО эстрогена в анамнезе: риск рака эндометрия выше у женщин, которые принимали только эстроген (без прогестерона) много лет в качестве гормональной заместительной терапии при менопаузе.
- Прием тамоксифена в анамнезе: женщины, которые принимали тамоксифен для лечения или профилактики рака молочное железы.
- Лучевая терапия органов малого таза в анамнезе.
- Семейный анамнез: женщины, у которых у матери, сестры или дочери были случаи рака эндометрия находятся в зоне риска по возникновению этого заболевания, а также женщины с наследственной формой рака толстой кишки (синдром Линча).
Нужно помнить, что не у всех женщин с раком эндометрия присутствуют вышеперечисленные факторы риска. Совершенно не у всех женщин, у которых имеются эти факторы риска, возникнет рак эндометрия.
Онкология матки: симптомы по стадиям
- Первая стадия. Как правило, симптомов нет, либо могут иметься незначительные патологическое отделяемое из влагалища, например, коричневатые выделения, наличие прожилок крови на белье или общее увеличение объема влагалищных выделений.
- Вторая стадия. Симптомы более выражены. У женщин фертильного возраста это может быть увеличение продолжительности менструации, увеличение объема теряемой крови, ациклические кровотечения. У пациенток в менопаузе могут возникать скудные или обильные маточные кровотечения. Также может быть лейкорея — обильные водянистые выделения. Таким образом, распознать рак матки на ранней стадии по симптомам сложно, поскольку признаки сходны с другими заболеваниями, например, с менструальной дисфункцией.
- На третьей стадии, когда в процесс вовлекаются окружающие ткани, может наблюдаться болевой синдром (боли могут носить как постоянный, так и схваткообразный характер), выделения могут быть гнилостные (цвет мясных помоев) с неприятным запахом. При сдавлении опухолевыми массами мочеточников может развиваться гидронефроз, который характеризуется болью в пояснице и развитием азотемии — отравлением организма азотистыми продуктами обмена веществ, которые в норме должны выводиться почками.
- На четвертой стадии усиливается боль. В процесс может вовлекаться толстая кишка, что сопровождается развитием симптомов кишечной непроходимости (запоры, вздутие живота). Если опухоль проросла в стенку мочевого пузыря, в моче могут быть примеси крови. Довольно часто возникает асцит — скопление свободной жидкости в брюшной полости. При наличии отдаленных метастазов симптоматика будет определяться пораженным органом. Чаще всего рак тела матки метастазирует в печень и легкие. Также на 4 стадии отмечается общее воздействие опухоли на организм — кахексия, общая слабость и др.
Диагностика рака эндометрия
Для диагностики рака эндометрия используют следующие методики:
- Физикальное обследование органов малого таза: ваш врач будет исследовать вашу матку, влагалище и близлежащие органы, чтобы исключить наличие образований или изменений в форме и размере.
- Ультразвуковое исследование: аппарат для ультразвукового исследования использует звуковые волны, которые не слышны человеку. Эти волны отражаются от участков разной плотности. Таким образом создается изображение матки и близко расположенных органов. Такая картинка может показать опухоль эндометрия. Для получения более четкого изображения, ультразвуковое исследование может проводиться и трансвагинально (когда ультразвуковой датчик помещается во влагалище).
- Гистероскопия: использование тонкой, гибкой трубки, которая помещается во влагалище. На конце этой трубки располагается камера, которая выводит на экран изображение матки. Таким образом врач может детально рассмотреть состояние матки и эндометрия.
- Биопсия: это удаление ткани и ее дальнейшее исследование в поисках раковых клеток. Обычно используется тонкая трубка, которая помещается в матку через влагалище. Тонкий слой ткани соскабливается со стенки матки, а затем врач-патолог исследует эту ткань под микроскопом. Часто биопсия это единственный способ точной диагностики злокачественной опухоли матки.
Степень дифференциации опухоли
Если обнаружена опухоль, врач исследует образец ткани под микроскопом, чтобы определить тип и степень дифференциации опухоли. Эта степень говорит о том, насколько тип раковых клеток отличается от нормальных клеток эндометрия. По степени дифференциации опухоли можно определить как быстро она будет расти. Высоко дифференцированные опухоли часто растут быстрее и чаще распространяются. Степень дифференциации также помогает определить дальнейший протокол лечения.
При диагностике рака эндометрия очень важно определить стадию заболевания. Это самая важная информация для определения тактики лечения. Стадии заболевания определяются на основании того вросла ли опухоль в соседние органы или распространилась в другие части тела.
Когда опухоль распространяется в другие органы, то она состоит из точно таких же патологических клеток как и первичная опухоль и называется точно также. Например, рак эндометрия может распространяться в легкие; при этом в легком будут присутствовать клетки опухоли эндометрия. Это называется метастатический рак эндометрия, а не рак легкого. Лечится такое осложнение по протоколам лечения рака эндометрия, а не рака легкого.
Чтобы определить распространилась ли опухоль, врач может назначить один из следующих видов исследований:
- Лабораторные анализы. Pap-тест может показать распространился ли опухолевый процесс на шейку матки, а анализы крови могут выявить нарушения функции печени и почек. Также ваш врач может назначить анализ на субстанцию CA-125, которая часто повышается при различных видах рака.
- Рентген грудной клетки: рентген грудной клетки может помочь выявить опухоль в легком.
- Компьютерная томография: Компьютерная томография делает много последовательных рентгеновских снимков-срезов, охватывая большое количество органов, и позволяет получить высоко точную картину, найти опухоль в отдаленных участках тела: лимфоузлах, легких и др. Иногда компьютерная томография проводится с введением контрастного вещества.
- МРТ работает как большой магнит, который подключен к компьютеру и помогает получить очень точные изображения матки, других внутренних органов и лимфоузлов. Иногда МРТ также проводится с введением контрастного вещества.

Часто, чтобы точно определить стадию заболевания, необходима операция. Хирург удаляет матку и берет образцы ткани из органов малого таза и живота. Когда матка удалена, препарат исследуют и оценивают, насколько глубоко вросла опухоль. Хирург также проверяет повреждены ли соседние органы и лимфоузлы.
Стадии рака эндометрия
Стадия 0 — Патологические раковые клетки найдены ТОЛЬКО на слизистой оболочки внутреннего слоя матки такая опухоль называется карцинома матки in situ.
Стадия I — Опухоль проросла через слизистую в эндометрий. Иногда опухоль прорастает и в миометрий.
Стадия II — Опухоль проросла в шейку матки.
Стадия III — Опухоль проросла через все слои матки и внедрилась в соседние органы: влагалище и лимфоузлы.
Стадия IV — Опухоль проросла в мочевой пузырь или кишечник. Или клетки опухоли распространились в отдаленные части тела: печень, легкие или кости.
В лечении рака матки используют хирургию, химиотерапию и гормональную терапию. Часто используют комбинацию этих методов.
Прогноз выживаемости при раке тела матки
Прогноз выживаемости будет определяться стадией заболевания, возрастом пациентки и патогенетическими особенностями опухоли. Наиболее благоприятно протекают гормонально зависимые опухоли без метастазов у пациенток младше 50 лет. У них удается добиться 5-летней выживаемости у 90% пациенток. Наиболее неблагоприятный прогноз у женщин старше 70 лет с автономным типом опухоли. При отсутствии отдаленных метастазов у них удается добиться пятилетней выживаемости в 60% случаев.
Цены в Европейской клинике на лечение рака матки
- Консультация онколога — 5100 руб.
- Консультация химиотерапевта — 6900 руб.
- Пангистерэктомия (экстирпация матки) с придатками — 172700 руб.
- Влагалищная экстирпация матки — 154600 руб.
- Проведение химиотерапии (инфузия, без стоимости лекарственных препаратов) — 15000 руб.
- Проведение иммунотерапии (без стоимости лекарственных препаратов) — 15000 руб.
Источник
Метастазирование рака эндометрия в лимфоузлы и ее прогноз
Длительное время абдоминальная гистерэктомия с придатками считалась стандартом лечения рака эндометрия (РЭ). По этой причине без внимания оставалась большая частота метастазирования в лимфоузлы. Несмотря на то что и первые, и более поздние публикации указывали на то, что у большого числа больных раком эндометрия (РЭ) даже с I стадией появятся метастазы в лимфоузлах, эти потенциальные очаги распространения опухоли в схемах лечения не учитывали.
В 1973 г. Morrow и соавт. установили, что из 369 пациентокс I стадией рака эндометрия (РЭ) метастазы влимфоузлахтаза обнаружены у 39. В 1976 г. Creasman и соавт. привели примеры еще 140 больных, у 16 из которых выявлены метастазы в тазовых лимфоузлах. Эти данные уточняли по ходу появления новых случаев рака эндометрия (РЭ). В относительно большой группе пациенток с клинически установленной I стадией рака эндометрия (РЭ) почти у 10% были обнаружены метастазы в лимфоузлах таза.
В исследовании Morrow и соавт. только 31 % больных с I стадией заболевания и метастазами в лимфоузлах пережили 5-летний рубеж, при том, что большинству из них была проведена послеоперационная ЛТ. Polish и соавт. опубликовали показатели выживаемости больных с микроскопическими метастазами в лимфоузлах, которым провели ЛТ как этап первичного лечения.
5-летняя выживаемость при подтвержденных хирургическим стадированием метастазах в лимфоузлах таза составила 67%, а в случаях поражения парааортальных узлов с метастазами или без таковых в лимфоузлах таза — 47 и 43% соответственно. В исследовании Creasman и соавт. у 102 больных для гистологической диагностики удаляли парааортальную жировую клетчатку, в результате чего в 10 (9,8 %) случаях выявили метастазы в этой области.
Boronow и соавт. при дополнении и обновлении одного из первых в этом направлении исследований GOG обнаружили, что из 222 пациенток с I стадией рака эндометрия (РЭ) у 23 (10,4 %) выявлены метастазы в лимфоузлах таза. Из 156 больных, которым провели микроскопическую оценку парааортальных лимфоузлов, метастазы были выявлены у 16 (10,2 %).
DiSaia в ходе длительного наблюдения отметил рецидивы заболевания у 21 (10,5%) из 199 пациенток, у которых не было метастазов в лимфоузлах таза, и у 13(56 %) из 23, имевших метастатическое поражение этих узлов. При отсутствии метастазов в парааортальных узлах рецидивы наблюдались у 15 (11 %) из 140 больных, а при их поражении — у 10 (59 %) из 17. Creasman, анализируя данные GOG о 621 пациентке с I стадией РЭ, обнаружил, что в 144 (22%) случаях заболевание распространилось за пределы матки: в тазовые и парааортальные лимфоузлы, придатки матки, органы брюшной полости — и/или были обнаружены злокачественные клетки в смывах.
Частота метастазирования в лимфоузлы у больных со II стадией рака эндометрия (РЭ) значительно выше, чем при 1 стадии заболевания. Morrow и соавт. привели данные о 85 пациентках: в 31 (36,5 %) случае выявлены метастазы в лимфоузлахтаза. В исследовании GOG 148 больным с клинически установленной II стадией РЭ провели хирургическое стадирование; у 66 процесс распространялся на шейку матки. Среди больных с поражением только желез эндоцервикса метастазы в тазовых лимфоузлах были обнаружены у 3 (17%) по сравнению с 35% пациенток с вовлечением стромы. Ни у одной больной с поражением только желез шейки матки метастазов в парааортальных лимфоузлах не было по сравнению с 23 % пациенток с вовлечением стромы.
При наличии инвазии в строму шейки матки метастазы в тазовых и парааортальных лимфоузлах выявляли у 46 % больных. В годовом отчете FIGO приведены данные о 43, 103 и 121 пациентке с III стадией рака эндометрия (РЭ) и степенью дифференцировки G1, G2 и G3 соответственно. 5-летняя выживаемость составила 62, 61 и 47 % соответственно.
Ben-Shachar и соавт. представили результаты лечения 349 больных, которых прооперировали по поводу рака эндометрия (РЭ). До операции у 52 % из них диагностированы высокодифференцированные опухоли (G1). Хирургическое стадирование ± парааортальная лимфаденэктомия были выполнены в 82 % случаев. После сравнения результатов пред- и послеоперационного гистологического исследования у 19 % пациенток оказалась более высокая степень дифференцировки (G2 или G3).
Метастазы в лимфоузлах обнаружены у 3,9 % пациенток с высокодифференцированной аденокарциномой (G1), у 10,5% заболевание распространилось за пределы матки. Признаки высокого риска — инвазия, захватывающая более половины толщины миометрия, низкодифференцированные (G3) и неблагоприятные морфологические варианты опухоли, переход процесса на шейку матки — были выявлены у 26 % больных, у которых до операции диагностирован высокодифференцированный рак (G1). Результаты хирургического стадирования указали па необходимость проведения адъювантной терапии у 12 % пациенток и отказ от нее — у 17 %.
С 1988 г., когда эксперты FIGO перешли с клинического определения стадии рака эндометрия (РЭ) на хирургическое стадирование, возник вопрос о роли лимфаденэктомии при лечении стадии рака эндометрия (РЭ). Несет ли она только диагностическую функцию, что уже существенно, или служит и лечебной процедурой? В первоначальных исследованиях выполняли селективную лимфаденэктомию — удаление подозрительных на наличие метастазов лимфоузлов.
Все большее количество данных свидетельствует о том, что необходимо выполнять полную лимфаденэктомию. Onda и соавт. провели тазовые и парааортальные лимфаденэктомии у 173 больных при 1—III стадии стадии рака эндометрия (РЭ), удалив в среднем 38 тазовых и 29 парааортальных узлов. Метастазы в лимфоузлах обнаружены у 30 (17%) пациенток: у 10 — только в тазовых лимфоузлах (группа Т), у 2 — только в парааортальных и у 18 — в тех и других (последние 20 больных вошли в группу А). В группе Т провели ЛТ обычными полями, в группе Л — расширенными и/или ПХТ. У 143 больпых без метастазов в лимфоузлах 5-летняя выживаемость составила 95 %, у 30 пациенток с метастазами в группе Т — 100 %, а в группе А — 75%.
По мнению авторов, системная тазовая и парааортальная лимфаденэктомия, а также последующие ЛТ и XT, назначенные на основании результатов гистологического исследования лимфоузлов, позволили улучшит!) выживаемость больных. Mohan и соавт. проанализировали результаты лечения 159 больных с I стадией заболевания,которым была выполнена тазовая лимфаденэктомия е последующей брахитерапией (контактной лучевой терапией). Общая 15-летняя выживаемость составила 92%, частота рецидивирования — 4,4%; во всех случаях рецидивы представляли собой отдаленные метастазы. В публикации под редакцией Podratz и соавт. рассмотрены 4 исследования, включая и вышеназванное, в которых лимфаденэктомию выполняли самым тщательным образом больным в группах умеренного и высокого риска, а послеоперационную ЛТ не назначали.
Среди 305 больных диагностировано 20 (6,6%) рецидивов заболевания; только в 5 из них рецидивы были местными/регионарными, причем 4 локализовались во влагалище. Этим 4 пациенткам не провели послеоперационную брахитерапию, но в последующем излечение было достигнуто с помощью ЛТ.
Выживаемость в зависимости от того, выполнена тазовая лимфаденэктомия или нет, и группы риска: низкого (р = 0,026) и высокого (р = 0,0006)
В ретроспективном исследовании, выполненном в клинике Мауо, 137 больных с высоким риском поражения лимфоузлов метастазами, которым была выполнена парааортальная лимфаденэктомия (ПЛА+), сравнили с пациентками, которым этот этап не выполняли (ПЛА—). В группе ПЛА+ 5-летняя выживаемость составляла 85 % по сравнению с 77 % в группе ПЛА—. У 51 больной с метастазами в тазовых или парааортальных лимфоузлах показатель выживаемости равнялся 77 % в группе ПЛА+ по сравнению с 42 % в группе ПЛА—. Kilgore и соавт., анализируя результаты лечения 649 пациенток, пришли к выводу о том, что выживаемость перенесших тазовую и парааортальную лимфаденэктомию значительно лучше, чем у пациенток с сохраненными лимфоузлами.
Кроме того, выживаемость после лимфаденэктомии лучше, чем без нее, но с послеоперационной ЛТ. В небольшом исследовании, включавшем 41 пациентку с РЭ III стадии, Bristow и соавт. установили, что безрецидивная выживаемость больных значительно возрастает при полном удалении всех макроскопически измененных лимфоузлов по сравнению со случаями, когда во время операции не были удалены явно метастатические узлы (37,5 vs 8,8 мес; р = 0,006).
В исследовании Havrilesky у 91 больной была установлена III стадия РЭ, причем у 39 обнаружены микрометастазы в нормальных по размеру лимфоузлах и у 52 — увеличенные метастатические узлы. После операции 92 % этих больных получали адъювантную терапию; ЛТ проведена 85% пациенток. У 39 пациенток с микроскопическими метастазами в лимфоузлах 5-летняя выживаемость равнялась 58 %, а у 41 больной с полным удалением макроскопически увеличенных метастатических узлов — 48% и всего 22 % у 11 женщин с неудаленными лимфоузлами. Авторы пришли к выводу, что эти данные свидетельствуют о терапевтической эффективности лимфаденэктомии.
Schink и соавт. определили размер опухолей у 91 больной с I стадией РЭ. Частота метастазов в лимфоузлах при размере опухоли менее 2 см составляла всего 5,7%, более 2 см в диаметре — 21 %, а в случаях поражения всего эндометрия этот показатель возрастал до 40 %. У пациенток с опухолью менее 2 см и инвазией менее чем на 1/2 толщины миометрия метастазов в лимфоузлах не было. На основании многофакторного анализа авторы установили, что размер опухоли — независимый прогностический фактор.
Однако Watanabe и соавт. придерживаются другого мнения и считают, что этот показатель не коррелирует с частотой метастазов в лимфоузлах.
Сравнение показателей выживаемости больных, которым выполнена лимфаденэктомия, но лучевая терапия не проведена, и больных, которым лимфаденэктомия не выполнена, но проведена лучевая терапия на область таза.
Низкий риск, р = 0,003; высокий риск, р = 0,041
– Также рекомендуем “Метастазирование рака эндометрия в придатки матки и ее прогноз”
Оглавление темы “Аденокарцинома матки”:
- Секреторная аденокарцинома эндометрия
- Степень дифференцировки рака эндометрия и ее прогноз
- Стадии рака эндометрия и их прогноз
- Инвазия рака эндометрия в миометрий и ее прогноз
- Цитология смывов брюшной полости при раке эндометрия и ее прогноз
- Метастазирование рака эндометрия в лимфоузлы и ее прогноз
- Метастазирование рака эндометрия в придатки матки и ее прогноз
- Молекулярные маркеры рака эндометрия и ее прогноз
- Прогностические факторы рака эндометрия
- Лечение рака эндометрия и ее эффективность