При ревматоидном артрите лимфоциты

При подозрении на ревматоидный артрит (РА) проводится тщательное обследование пациента. Трудности при диагностировании патологии возникают из-за пока еще не установленных причин развития воспалительной реакции. Поэтому пациентам показан ряд лабораторных и инструментальных исследований, необходимых для выявления самого заболевания, стадии его течения, степени поражения суставных структур.
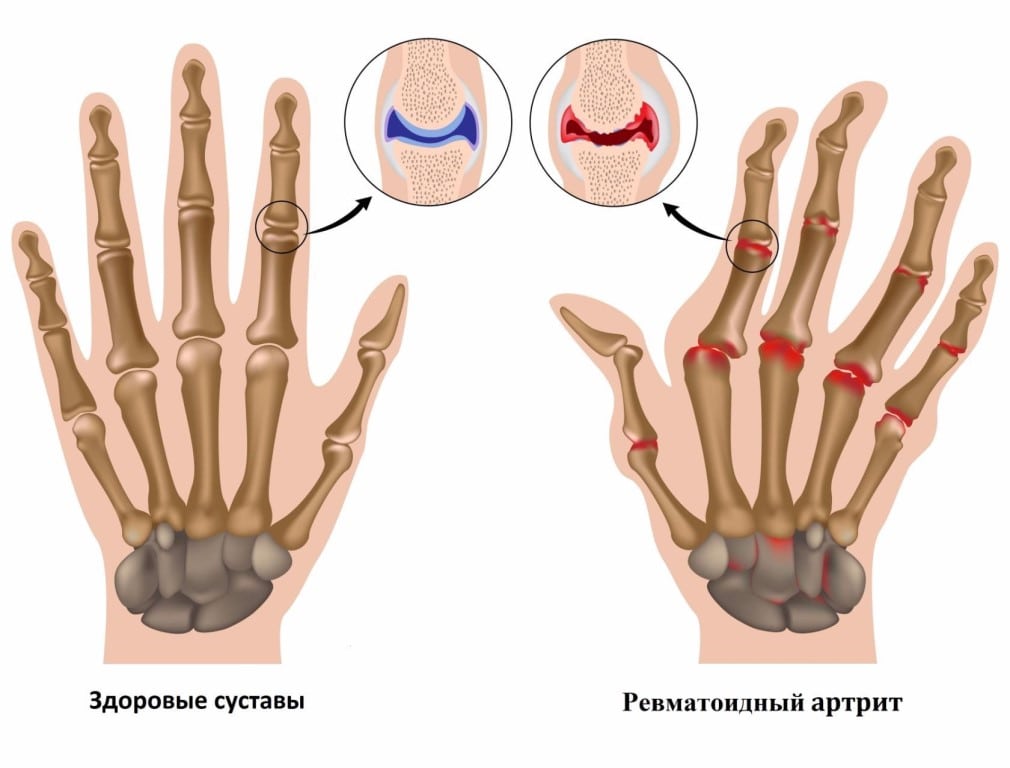
Ведущим диагностическим признаком РА считается ревматоидный фактор — специфические иммуноглобулины, вырабатываемые в процессе иммунного ответа. Но у более 20% больных серонегативной формой РА этого маркера суставной патологии в крови не обнаружено. При комплексном обследовании пациентов заболевание подтверждается анализами на антинуклеарный фактор, АЦЦП, С-реактивный белок. Биохимический анализ крови при ревматоидном артрите позволяет с максимальной точностью выявить аутоиммунную патологию.
Диагностические критерии
Важно знать! Врачи в шоке: “Эффективное и доступное средство от боли в суставах существует…” Читать далее…
Для ревматоидного артрита характерны эрозивно-деструктивные поражения преимущественно мелких периферических суставов. Заболевание опасно постепенным разрушением сочленений, расстройствами работы внутренних органов. Снижение их функциональной активности можно отследить по изменению состава биологических жидкостей — крови, мочи, синовия. Часто биохимические исследования помогают окончательно выставить диагноз «ревматоидный артрит», подтвердив результаты рентгенографии, МРТ, КТ, артроскопии. При подозрении на развитие патологии необходимо проведение следующих анализов:
- общего анализа мочи;
- общего анализа крови, включая подсчет СОЭ (скорость оседания эритроцитов);
- биохимический анализ крови для установления уровней печеночных ферментов, креатинина, С-реактивного белка;
- обнаружение ревматоидного фактора, антицитруллиновых и антинуклеарных антител;
- выявления маркеров развития гепатитов в качестве дифференциальной диагностики реактивных артритов.
Это самые распространенные методы клинического выявления заболевания суставов. Диагностика ревматоидного артрита по лабораторным анализам одновременно позволяет оценить общее состояние здоровья.
Клинические анализы крови, мочи, кала
Общий анализ крови при артрите позволяет установить ее качественный и количественный состав, физико-химические свойства. Обнаружение некоторых биохимических субстратов помогает определить протекающий в организме воспалительный процесс, в том числе спровоцированный патогенными микроорганизмами.
| Исследования крови, назначаемые при подозрении на развитие ревматоидного артрита | Характерные особенности диагностических мероприятий |
| Определение уровня лейкоцитов | Состояние, при котором в крови повышается количество лейкоцитов. Такое изменение состава крови выявляется при тяжелом течении ревматоидного артрита с присутствием внесуставной симптоматики. Обычно лейкоцитоз выявляется одновременно с повышенным уровнем ревматоидного фактора и служит показанием для назначения пациенту глюкокортикостероидов. Большое количество лейкоцитов в системном кровотоке может быть признаком инфицирования вирусами, бактериями, грибками, что требует дифференциальной диагностики |
| Установление содержания гемоглобина | С помощью этого критерия можно оценить активность РА. Выявляется анемия только у 50% больных. Причина резкого снижения гемоглобина — воспалительный процесс, негативно сказывающийся на состоянии иммунитета. Железодефицитная анемия выявляется несколько реже, требует дифференциальной диагностики для исключения внутренних кровотечений |
| Выявление концентрации лимфоцитов | Повышенный уровень лимфоцитов при одновременном снижении количества лейкоцитов — типичный маркер вирусной инфекции. Подтверждения — увеличение лимфатических узлов, клинические проявления общей интоксикации организма. Такое изменение состава крови характерно для реактивного артрита, спровоцированного проникновением в суставные полости возбудителей гепатита |
Самый информативный анализ для диагностики артрита — скорость оседания эритроцитов. Это неспецифический лабораторный показатель, отражающий соотношение фракций белков плазмы. Кроме клеточных элементов, в крови содержатся белки, вода, различные биохимические субстраты. Эритроциты (красные кровяные тельца) не могут долго оставаться во взвешенном состоянии в пробирке с кровью, поэтому начинают опускаться на дно. Скорость их оседания зависит от присутствия в крови других компонентов. Если в ней много белков (диагностических маркеров воспаления), то эритроциты формируют агрегаты и быстро опускаются на дно пробирки. Выявления высоких значений СОЭ свидетельствует о протекании острого воспаления, которое может быть признаком аутоиммунной реакции. Такие параметры указывают и на развитие тяжелой формы РА, поражение внутренних органов.
Если при исследовании образцов мочи обнаружен повышенный уровень белка и лейкоцитов, необходимо устанавливать локализацию воспаления в организме. Это только косвенный признак ревматоидного артрита, требующий дальнейшей диагностики. Обязательно выявляется содержание в моче:
- глюкозы;
- кетоновых тел;
- билирубина;
- эритроцитов;
- эпителиальных клеток.
Повышенный уровень солей может указывать на нарушение обмена веществ, осложняющего течение РА.
Анализ кала при диагностировании ревматоидного артрита проводится для исключения реактивной патологии. Ее развитие провоцирует неадекватный ответ иммунной системы на проникновение в организм хламидий, сальмонелл, шигелл. Микроорганизмы легко выявляются при бактериологическом исследовании кала.
Биохимический анализ крови
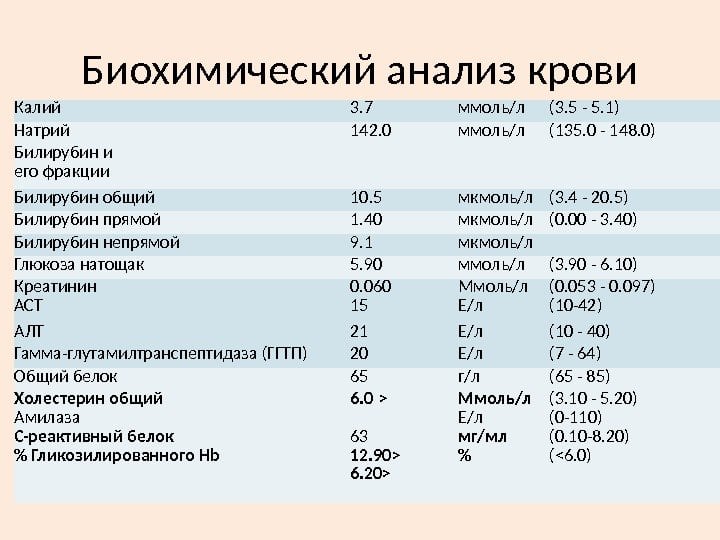
Обнаружение в крови определенных биохимических компонентов помогает установить воспалительный процесс в суставах, его интенсивность и стадию течения. Например, при рецидивах РА повышается уровень белка гаптоглобина, что служит признаком разрушения большого количества красных кровяных телец.
При проведении биохимического анализа крови на ревматоидный артрит обязательно определяется уровень фибриногена — специфического белка, находящегося в сыворотке в растворенном виде. Он служит субстратом для образования тромбов при сворачивании крови. У больных РА уровень фибриногена существенно превышает значения нормы (2-4 г/л).
Неспецифическим диагностическим маркером РА является уровень сиаловых кислот — актированных производных нейраминовой кислоты, которые входят в состав гликопротеинов. В плазме здорового человека их концентрация колеблется в пределах 2-2,33 ммоль/л. На развитие РА указывает превышение этого показателя, свидетельствующее о воспалении в суставных соединительнотканных структурах.
“Врачи скрывают правду!”
Даже “запущенные” проблемы с суставами можно вылечить дома! Просто не забывайте раз в день мазать этим…
>
При проведении биохимического анализа крови при ревматоидном артрите выявляется содержание серомукоидов (сывороточных протеинов), иммуноглобулинов, пептидов. Если их концентрация превышает значения нормы, то врачи подозревают острое, прогрессирующее течение РА.
C-реактивный белок

Так называется белок плазмы крови, относящийся к группе протеинов острой фазы, концентрация которых повышается при воспалительном процессе. С-реактивный белок вырабатывается в большом количестве во время иммунного ответа на проникновение в организм инфекционных или аллергических агентов. Обнаружение уровня этого диагностического маркера помогает дифференцировать РА от артритов невоспалительного характера. Количественное содержание С-реактивного белка необходимо для оценки активности воспаления. Этот критерий в дальнейшем позволяет отследить:
- результативность терапии;
- вероятность прогрессирования дегенеративно-дистрофических изменений в хрящевых, костных, соединительнотканных структурах.
Биохимический маркер не специфичен, так как не позволяет точно выяснить, что спровоцировало воспаление и ее локализацию. Уровень С-реактивного белка всегда увеличивается при аутоиммунных, бактериальных, вирусных патологиях. Но обнаружение этого изменения состава крови с высокой вероятностью указывает на развитие системной патологии, поражающей не только суставы, но и внутренние органы.
Ревматоидный фактор
Важный диагностический маркер РА, обнаруживаемый в крови более чем у 80% пациентов. Ревматоидный артрит развивается при атаке иммунной системы на собственные клетки организма, принимаемые ею за чужеродные белки. Для их уничтожения она продуцирует огромное количество антител — ревматоидного фактора. Эти иммуноглобулины разрушают сначала синовиальную оболочку, а при отсутствии врачебного вмешательства вскоре поражают соединительные ткани внутренних органов.
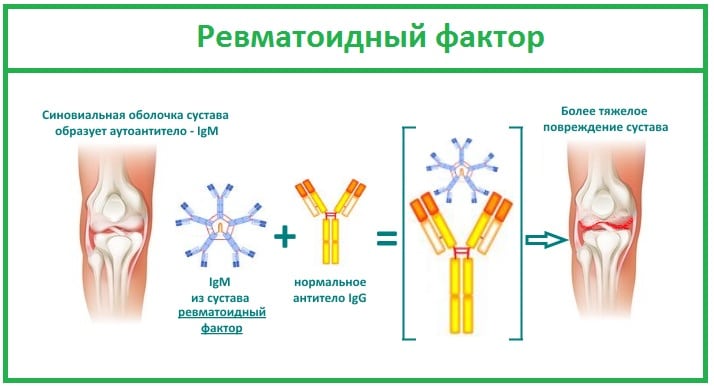
Ревматоидный фактор — один из важных диагностических критериев РА. Но является высокоспецифичным, но требует подтверждения данными, полученными при проведении инструментальных исследований. Дело в том, что высокий уровень ревматоидного фактора в крови характерен и для других заболеваний:
- системной красной волчанки;
- дерматомиозитов;
- васкулитов;
- склеродермии;
- бактериальных, вирусных, грибковых, паразитарных патологий.
Высокий уровень ревматоидного фактора на начальном этапе РА, когда суставы повреждены незначительно, является характерным признаком быстрого прогрессирования и тяжелого течения патологии. Этот критерий часто выявляется во время терапии для оценки ее эффективности.
Антицитруллиновые и антинуклеарные антитела
В процессе аутоиммунной реакции продуцируются антинуклеарные антитела, предназначенные для атаки белковых ядер собственных клеток организма. Показанием для определения количественного содержания обычно становится высокий уровень СОЭ, указывающий на развитие воспалительного процесса. Маркер неспецифичен, так как выявляется и при других патологиях:
- коллагенозе, системной красной волчанке, поражающих соединительные ткани;
- склеродермии;
- гепатите;
- реактивном артрите.
С помощью уровня антинуклеарных антител удается косвенно подтвердить развитие РА. Это особенно ценно при его серонегативной форме с отсутствием ревматоидного фактора в крови.
Самый специфичный маркер, выявляющий при проведении биохимических анализов при артрите, — наличие в крови антицитруллиновых антител, вырабатываемых иммунной системой к циклическому цитруллиновому пептиду. Химическая структура цитруллина схожа со строением аминокислоты, входящей в состав белковой молекулы. Эти белки — строительные элементы суставной капсулы, которая атакуется иммуноглобулинами при РА.
Если в крови пациента обнаруживается повышенный уровень АЦЦП, то с более чем 90% вероятностью можно предположить развитие ревматоидного артрита. Выявление антицитруллиновых антител позволяет обнаружить суставную патологию на начальной стадии и сразу приступить к лечению. Ранняя диагностика РА помогает избежать тяжелейших осложнений, в том числе необратимого поражения внутренних органов. Но, несмотря на высокую специфичность маркера, в некоторых случаях повышенный уровень АЦЦП указывает на развитие других заболеваний, не связанных с опорно-двигательным аппаратом.
Проведения этих лабораторных анализов на ревматоидный артрит бывает достаточно для подтверждения диагноза. Но в ревматологии существует 7 критериев, позволяющих с высокой точностью установить аутоиммунную патологию. Это количество вовлеченных в воспалительный процесс суставов, симметричность их поражения, выраженность симптоматики, длительность течения заболевания. При обнаружении у больного 4 из 7 критериев пациенту выставляется окончательный диагноз.
Похожие статьи
Как забыть о болях в суставах?
- Боли в суставах ограничивают Ваши движения и полноценную жизнь…
- Вас беспокоит дискомфорт, хруст и систематические боли…
- Возможно, Вы перепробовали кучу лекарств, кремов и мазей…
- Но судя по тому, что Вы читаете эти строки – не сильно они Вам помогли…
Но ортопед Валентин Дикуль утверждает, что действительно эффективное средство от боли в суставах существует! Читать далее >>>
загрузка…
Источник
При исследовании костного мозга у больных РА обнаруживают в большинстве случаев характерные, но неспецифические изменения. Прежде всего это умеренный плазмоцитоз (обычно не превышающий 5—7%), обнаруживающий параллелизм с активностью болезни и рассматриваемый как отражение повышенной активности В-системы иммунитета.
Закономерно наблюдаются также такие неспецифические признаки, как повышение коэффициента лейко: эритро (отношение числа всех форм гранулоцитов миелограммы к сумме ядерных клеток эритробластического ряда) более 4 и нарастание костномозгового индекса нейтрофилов (отношение суммы нейтрофильных промиелоцитов, миелоцитов и метамиелоцитов к сумме нейтрофильных палочкоядерных и сегментоядерных) выше 0,8. Индекс созревания эритронормобластов (отношение гемоглобинсодержащих ядерных клеток эритропоэза к сумме всех этих клеток), равный у здоровых людей 0,8—0,9, существенно не отличается.
Общее количество костномозговых клеток, а также процентное содержание лимфоцитов и эозинофилов, как правило, не отличается от нормального. Таким образом, при анализе миелограмм у больных РА обнаруживают лишь небольшой плазмоцитоз и некоторое «раздражение» лейкоцитарного ростка. Серьезной гематологической патологии при этом не регистрируется. В то же время при исследовании периферической крови наблюдаются более закономерные изменения.
Анемия — самое частое внесуставное проявление РА. Она встречается в развернутой стадии болезни не менее чем у 30% больных и в большинстве случаев бывает умеренной . (90—110 г/л). Ввиду медленного развития анемии больные обычно хорошо приспосабливаются к ней, в частности, за счет увеличения ударного объема сердца и часто наблюдаемого учащения сердечных сокращений. Тем не менее необходимо учитывать, что при выраженной анемии именно она может быть причиной общей слабости, легкой утомляемости, головокружения, а у лиц со значительным коронарным или церебральным атеросклерозом — причиной соответствующих ишемических расстройств. Как правило, анемия нормо или гипохромная и нормоцитарная, количество ретикулоцитов в пределах нормы.
Основной причиной анемии при РА является хронический воспалительный процесс, а не какие-либо специфические нозологические особенности. Поэтому наиболее существенные черты анемии у больных РА и другими хроническими воспалительными заболеваниями оказываются тождественными. В этом же смысле показательно, что выраженность анемии коррелирует не столько с длительностью болезни, сколько со степенью ее клинической активности — в частности, лихорадкой, количеством воспаленных суставов, интенсивностью синовитов и т. д.
Конкретные причины анемии при РА, как и при других заболеваниях, сочетающихся с хроническим воспалением, разнообразны, но на первом месте среди них нарушение утилизации железы. Уровень железа в крови обычно заметно снижен. Важнейшей особенностью рассматриваемой патологии является тот факт, что в отличие от обычных железодефицитных анемий (при кровопотере и т. д.) гипоферремия вызвана не уменьшением общего количества железа в организме, а его задержкой в макрофагальной (ретикулоэндотелиальной) системе, которая при РА отличается признаками гиперплазии и повышенной функции.
Значительная часть железа из распадающихся «старых» эритроцитов, которое в норме быстро связывается с белком-переносчиком трансферрином и доставляется им к нормобластам костного мозга, у больных РА остается в виде запасов в органах ретикулоэндотелиальной системы. Таким образом, несмотря на увеличение запасов железа, снабжение им костного мозга оказывается сниженным.
В соответствии с этим в тканях и сыворотке крови резко нарастает уровень ферритина — белка, содержащего «железо запасов», мало участвующего в активном метаболизме. В то же время содержание трансферрина, участвующего в доставке железа клеткам костного мозга, снижается. Полагают, что уровень железа в плазме уменьшается также вследствие его связывания с лактоферрином — белком, находящимся в гранулах нейтрофилов. Последние в процессе ревматоидного воспаления распадаются в больших количествах, в связи с чем нарастает и уровень лактоферрина, образующего с железом относительно инертные (в функциональном отношении) комплексы.
Среди других причин анемии, имеющих явно меньшее значение и встречающихся у небольшого числа больных, рассматривают уменьшение синтеза эритропоэтина (или сниженную реакцию на него костного мозга), небольшое увеличение объема плазмы с относительным уменьшением общего объема эритроцитов, умеренное укорочение длительности жизни эритроцитов с симптомами легкого гемолиза. Значение этих механизмов, однако, признается не всеми авторами, и результаты соответствующих исследовании нередко противоречивы.
Истинный аутоиммунный гемолиз с быстрым и значительным снижением уровня гемоглобина и положительной пробой Кумбса встречается очень редко. Он может быть вызван как холодовыми агглютининами типа IgM, так и тепловыми антителами класса IgG.
У отдельных больных отмечается макроцитарная анемия, поддающаяся терапии витамином Bia. Описана мегалобластическая анемия вследствие дефицита фолиевой кислоты. Тем не менее нет достаточных оснований для предположения о закономерной патогенетической связи этих расстройств с основным заболеванием.
Помимо анемии, связанной с плохо реализуемым накоплением железа в ретикулоэндотелиальной системе, при РА очень часто наблюдается и истинная железодефицитная анемия. Она вызвана прежде всего увеличенной потерей крови через желудочно-кишечный тракт вследствие раздражающего или эрозирующего влияния кортикостероидов и НПВП.
Нередко имеет значение усиление менструальных кровотечений в связи с назначением кортикостероидов (в том числе гидрокортизона и особенно кеналога внутрисуставно). Накопление внутриклеточного ферритина и уменьшение уровня трансферрина могут тормозить связывание железа с клетками пищеварительного тракта, а тем самым и его всасывание.
Анемия у больных РА отчасти может быть связана со специфическими свойствами применяемых лекарственных препаратов, следует иметь в виду также более редкие или менее доказанные возможности. Так, НПВП тормозят синтез простагландинов, которые способны стимулировать эритропоэз. Назначение сульфасалазина у единичных больных вызывает фолиеводефицитную анемию.
Угрожающая жизни апластическая анемия, встречающаяся при РА очень редко, почти всегда связана с назначением препаратов золота, бутадиона, D-пеницилламина или иммунодепрессантов. Значительно чаще применение иммунодепрессантов приводит к развитию нормохромной анемии, не имеющей существенного клинического значения и нередко исчезающей на фоне продолжающегося лечения (особенно при продолжительном лечебном эффекте).
Изменения числа лейкоцитов и лейкограммы не закономерны. Нейтрофильный лейкоцитоз, нередко с умеренным сдвигом влево, обычно встречается в следующих случаях:
- при выраженных обострениях РА с максимальной активностью процесса (особенно у детей и лиц молодого возраста);
- при назначении кортикостероидов, причем у ряда больных нейтрофильная реакция оказывается очень выраженной и стойкой;
- у больных системным ревматоидным васкулитом.
Стойкая лейкопения вследствие снижения нейтрофилов — типичный признак синдрома Фелти.
У большинства больных РА число лейкоцитов нормальное или умеренно сниженное (отчасти в результате лекарственной терапии—иммунодепрессантами, НПВП и т. д.). Лейкограмма почти всегда нормальна, при развитии лейкопении (обычно за счет нейтрофилов), как правило, наблюдается относительный лимфоцитоз.
У немногих больных отмечается эозинофилия выше 5%. Специального значения этот симптом обычно не имеет, хотя отдельные авторы полагают, что он чаще встречается у больных с висцеральными ревматоидными изменениями и васкулитом, в связи с чем должен вызывать соответствующую настороженность. Сравнительно часто эозинофилия сопутствует ауротерапии, сочетаясь с нарастанием уровня IgE, и иногда свидетельствуя о возможном развитии аллергических реакций на препараты золота.
Изменения тромбоцитов. Весьма характерен тромбоцитоз выше 400·109/л, встречающийся приблизительно у 15% больных РА и обнаруживающий отчетливый параллелизм с клиническими и лабораторными показателями активности заболевания. В миелограммах при этом отмечается увеличение числа мегакариоцитов с активной отшнуровкой тромбоцитов. При снижении активности болезни число тромбоцитов нормализуется или приближается к норме.
Как и анемия, тромбоцитоз у больных РА не может считаться характерным признаком болезни как таковой, а является неспецифической реакцией на воспалительный процесс. Продукты последнего (в частности, вырабатываемые макрофагами) оказываются, по-видимому, стимуляторами тромбоцитопоэза. Не подтверждается точка зрения на тромбоцитоз как на компенсаторную реакцию в связи с повышенным потреблением тромбоцитов вследствие усиленного внутрисосудистого свертывания. Последнее, вопреки ряду публикаций, не свойственно РА.
Гипертромбоцитоз, не соответствующий активности болезни, вызывает подозрение на латентное сопутствующее заболевание, которое может сопровождаться этим симптомом (злокачественные опухоли, миелопролиферативные заболевания, хронические инфекции). У отдельных больных тромбоцитоз служит реакцией на назначение кортикостероидов (как и лейкоцитоз).
Несмотря на частое повышение уровня тромбоцитов, тромбоэмболические осложнения при РА очень редки. По-видимому, это объясняется снижением функции тромбоцитов благодаря влиянию НПВП, которые угнетают синтез простагландинов и тромбоксанов и тем самым тормозят агрегацию тромбоцитов — один из основных этапов образования тромбов. Хинолиновые препараты в исследованиях in vitro уменьшают агрегацию тромбоцитов, вызванную АДФ и коллагеном, но в клинических условиях подобный эффект не наблюдается.
Тромбоцитопения при РА встречается редко. В подобных случаях следует рассмотреть вопрос о ее возможной связи с проводимым лечением (прежде всего иммунодепрессантами). Истинный синдром Верльгофа со снижением числа тромбоцитов ниже 40·109/л и кровоточивостью наблюдается чрезвычайно редко и обычно бывает аутоиммунной реакцией на такие лекарственные препараты, как D-пеницилламин, левамизол и препараты золота.
Изменения свертываемости и вязкости крови. Клинически значимая патология гемостаза встречается при РА очень редко. Тромбоцитоз как один из факторов риска тромботических осложнений уравновешивается за счет антиагрегационного влияния НПВП. Эффект последних иногда проявляется в заметном удлинении времени кровотечения, особенно выраженном при назначении ацетилсалициловой кислоты [Nadell J. et al., 1974].
У отдельных больных причиной кровоточивости оказывались своеобразные ингибиторы естественных факторов свертывания в крови. Один из них — антитела класса IgG к антигемофилическому глобулину (фактору VIII), вызывающие удлинение частичного тромбопластинового времени и серьезные геморрагические проявления (соответствующие клинической гемофилии), включая кровоизлияния в полость суставов и в крупные мышцы. Эти весьма редко обнаруживаемые антитела почти всегда находили только у больных, страдающих РА в течение многих лет.
У нескольких больных РА был описан так называемый волчаночный антикоагулянт, который значительно чаще обнаруживают при СКВ. Он представляет собой аутоантитело к комплексному активатору протромбина, состоящему из фактора Ха, фактора V, ионов кальция и фосфолипида. Его наличие сопровождается удлинением частичного тромбопластинового и протромбинового времени.
Считают, что волчаночный антикоагулянт при РА не вызывает серьезной кровоточивости, но может стать ее причиной при сочетании с иными дефектами в системе гемостаза.
К редкой патологии при РА относится синдром повышенной вязкости, проявляющийся лишь у тех больных, у которых вязкость сыворотки крови превышает вязкость воды в 4—5 раз (в норме это соотношение составляет 1,4—1,8).
Клиническими признаками данного синдрома в связи с развивающимся венозным стазом (особенно в ЦНС) служат вялость, сонливость, головная боль, головокружение, помутнение зрения, а при его максимальной выраженности — тромбозы вен глазного дна, ступор и угрожающая жизни кома. Непосредственной причиной повышенной вязкости в подобных случаях бывает наличие в сыворотке крови крупных молекулярных конгломератов, возникающих в результате взаимодействия РФ и полимерных комплексов IgG.
Сигидин Я.А.
Опубликовал Константин Моканов
Источник