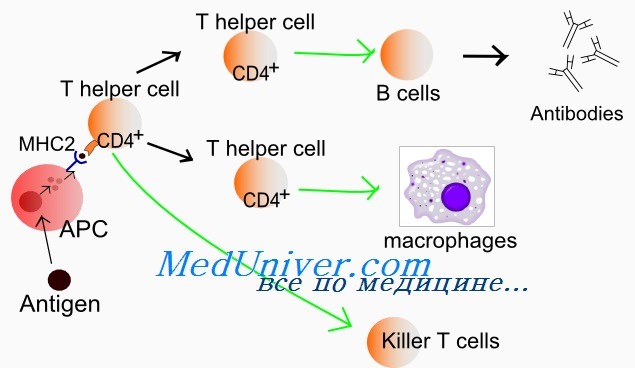
Предшественники т лимфоцитов костный мозг
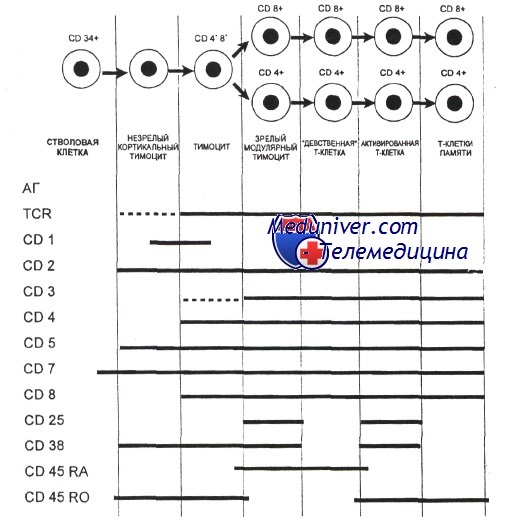
Гематология: Развитие Т-лимфоцитовПредшественники, прекоммитированные к развитию в Т-лимфоциты, непрерывно мигрируют от костного мозга в вилочковую железу, однако их число, по-видимому, очень мало. Незрелые предшественники Т-клеток поступают в область коры вилочковой железы, где созревают в функциональные субпопуляции Т-клеток. Особенностью развития тимоцитов является высокая скорость пролиферации. Различные стадии развития тимоцита можно определить по изменению экспрессии поверхностных и цитоплазматических молекул, рецепторов цитокинов и состояния реаранжировки генов Т-клеточного рецептора. Т-клеточный рецептор (TCR) распознает только короткие пептиды, которые заполняют полость в молекулах первого или второго класса главного комплекса гистосовместимости (МНС I и II, МНС комплекс у человека обозначается как HLA). Презентация таких пептидов Т-лимфоцитам обеспечивается антигенпредставляющими клетками. TCR — гетеродимерный комплекс, сформированный при ассоциации а-и бета- или у- и S-субъединиц. Каждая из этих субъединиц кодируется отдельным геном. Т-клетки с рецепторами типов ар и уq являются различными линиями, которые разделяются до начала реаранжировки гена TCR. Наименее зрелые клетки-предшественники в вилочковой железе экспрессируют антиген CD7. Некоторые из них экспрессируют также CD44. CD44, рецептор для гиалуроновой кислоты, — один из факторов, определяющих перемещение предшественников Т-клеток в вилочковую железу. Из этих предшественников далее образуются CD2+/CD7+ клетки, в цитоплазме которых присутствует CD3. Белковый комплекс CD3 обеспечивает передачу сигналов через TCR. Пептидные цепи CD3-комплекса начинают синтезироваться на стадии про-Т-лимфоцита, и их экспрессия предшествует появлению на мембране TCR. Т-лимфоциты уq-линии первыми начинают экспрессировать рецептор CD3, но на них нет молекул CD4 или CD8. Несколько позднее на поверхности клеток, экспрессирующих рецептор типа аb, начинают одновременно экспрессироваться антигены CD4 и CD8. К этому времени заканчивается реаранжировка генов а- и р-цепей, и на поверхности клеток экспрессируется рецепторный комплекс TCR ab/CD3. По мере того как клетки, экспрессирующие CD4+, CD8+ и TCR (так называемые дважды положительные клетки), проходят от коры к мозговому веществу вилочковой железы, они созревают в CD4+ хелперные или CD8+ цитотоксические Т-клетки. Клетки, которые созревают до стадии CD4+ или CD8+, составляют менее 5% тимоцитов. Эти лимфоциты покидают вилочковую железу и заполняют вторичные лимфоидные ткани (лимфатические узлы, селезенку, лимфоидную ткань, ассоциированную со слизистыми оболочками). Т-лимфоциты с рецептором уq и CD5+B1-клетки являются функционально аналогичными популяциями, которые развиваются параллельно. Т-клетки с рецептором типа уq найдены в различных тканях, включая селезенку, эпидермис и эпителий слизистой оболочки матки, влагалища и языка. Предполагается, что эта популяция клеток может исполнять роль иммунного надзора в перечисленных тканях.
Формирование комплекса Т-клеточного рецептора и положительная и отрицательная селекция в вилочковой железеКак и гены иммуноглобулинов, гены Т-клеточного рецептора собираются из различных сегментов, находящихся первоначально в зародышевой конфигурации. Гены Т-клеточного рецептора подвергаются процессу соматической реаранжировки, при которой кодирующие сегменты присоединяются друг к другу, а присутствующие между ними интронные последовательности удаляются. Вариабельность соединений и вставок обеспечивает возникновение различий TCR и приводит к огромному количеству различных последовательностей гипервариабельного участка TCR. Репертуар различных TCR считается даже большим, чем репертуар молекул Ig (по оценкам, репертуар ab-TCR составляет 1015, а для yq-TCR — 1018). В отличие от В-лимфоцитов, Т-лимфоциты не секретируют свои рецепторы. Дважды позитивный тимоцит проходит через многоступенчатый процесс, известный как тимическая селекция. На первой фазе, называемой положительной селекцией, TCR дважды позитивного тимоцита взаимодействуют с молекулами МНС, которые экспрессируются эпителиальными клетками в коре вилочковой железы. Тимоциты, способные распознавать комплекс антигена с молекулой HLA, ускользают от апоптоза и вступают в дальнейшую дифференцировку, в то время как тимоциты, не способные к такому взаимодействию, погибают. Поскольку рекомбинации, затрагивающие возникновение TCR, являются случайными, в вилочковой железе могут развиваться и пройти позитивную селекцию Т-клетки, экспрессирующие TCR, специфичные к чужеродным и собственным антигенам. Существует вероятность, что Т-клетки, реактивные к собственным структурам организма, будут взаимодействовать с аутоантигенами в тканях, что может привести к нежелательным аутоиммунным реакциям. Для предотвращения этого дважды положительные клетки подвергаются второй фазе отбора, которая называется негативной селекцией. В ходе этой фазы дважды положительные клетки взаимодействуют с комплексом МНС-пептид, экспрессированным на поверхности дендритной клетки. Т-клетки, TCR которых взаимодействует с комплексом МНС-пептид с высокой аффинностью, подвергаются апоптозу. В ходе негативной селекции удаляются Т-клетки, экспрессирующие TCR, обладающие реактивностью к собственным антигенам. Дважды положительные клетки, пережившие негативную селекцию, снижают экспрессию корецепторов CD4 или CD8, что приводит к развитию или CD4+CD8″ или CD4″CD8+ (моноположительных) Т-лимфоцитов. При этом Т-лимфоциты, распознающие антигены, представляемые молекулами МНС II класса, сохраняют экспрессию корецептора CD4+, a Т-лимфоциты, распознающие антигены, представляемые молекулами МНС I класса, сохраняют экспрессию корецептора CD8+. Эти клетки покидают вилочковую железу и образуют периферические зрелые CD4+ и CD8+ Т-клетки.
Клетки и цитокины, регулирующие развитие Т-клетокВилочковая железа состоит из корковой и медуллярной областей, различающихся по количеству тимоцитов и составу стромальных клеток. Стромальные клетки вилочковой железы влияют на развитие тимоцитов как посредством прямых межклеточных взаимодействий, так и секрецией растворимых медиаторов. Тимоциты и клетки тимического эпителия экспрессируют ряд поверхностных клеточных детерминант, некоторые из которых вовлечены в адгезию этих клеточных популяций друг к другу. Рецептор CD2 на тимоцитах определяет связывание с детерминантой CD58 (LFA-3) и межклеточной адгезионной молекулой-1 (ICAM-1), представленными на клетках тимического эпителия. Взаимодействия между развивающимися лимфоцитами и стромой могут активировать обе популяции. Например, связывание тимоцитов со стромой может стимулировать продукцию ИЛ-1 стромальными клетками и повышать экспрессию рецептора ИЛ-2 на тимоцитах. ИЛ-7 стимулирует полиферацию тимоцитов, и фактор стволовых клеток увеличивает этот эффект. Эпителиальные клетки вилочковой железы у человека являются источником цитокинов ИЛ- 1а и b, ИЛ-3, ИЛ-6, ИЛ-8, колониестимулирующих факторов (Г-КСФ и ГМ-КСФ), лейкозингибирующего фактора (LIF) и TGF-p, а также гормонов тимозина или тимопоэтина, оказывающих влияние на пролиферацию и дифференцировку тимоцитов. Цитокины, необходимые для развития Т-клеток, могут продуцироваться самими Т-клетками. Тимоциты производят IFN-y, ФНО-а, ИЛ-2, ИЛ-3 и ИЛ-4. Естественные киллерные клетки. Естественные киллеры (NK) обладают способностью спонтанно лизировать некоторые опухолевые клетки-мишени. Человеческие NK-клетки экспрессируют CD16 и CD56, но не имеют TCR или CD3. По морфологическим характеристикам эти клетки представляют собой большие гранулярные лимфоциты (в них присутствуют крупные цитоплазматические гранулы). NK-клетки имеют гемопоэтическое происхождение и развиваются в костном мозге, но пока мало известно об их предшественниках. – Также рекомендуем “Гематология: Развитие лимфоцитов в лимфатических узлах и селезенке” Оглавление темы “Гематология”:
|
Источник
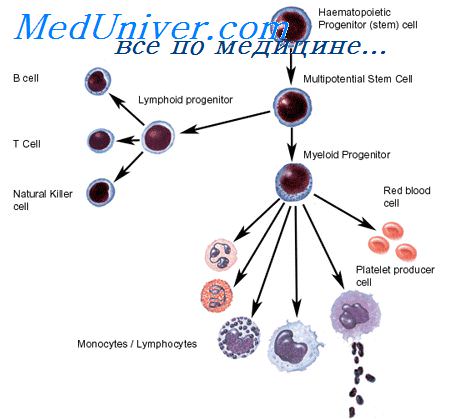
Образование предшественников лимфоцитов. Поражения стволовой клеткиСледующий шаг дифференцировки — образование отдельных предшественников для Т- и В-лимфоцитов. Предшественник Т-лимфоцитов несет на поверхности рецепторы для эритроцитов барана; число их увеличивается по мере созревания этого предшественника. По дифферен-цировочным антигенам на этой стадии происходит дальнейшая дифференцировка предшественника с образованием клеток-предшественников отдельно для мозговых и корковых лимфоцитов тимуса, которые представляют собой не последовательные стадии гистогенеза, а две независимые популяции Т-лимфоцитов. Обе эти популяции требуют для своего развития различного микроокружения. В частности, в селезенке преимущественно развиваются короткоживущие, кортизончувствительные корковые Т-лимфоциты, тогда как в лимфатических узлах — долгоживущие, кортизонрезистентные мозговые Т-лимфоциты. В ряду дифференцировки В-клеток различают ряд стадий. Первая из них дает предшественник, несущий на поверхности рецепторы для Fc-фрагмента агрегированных иммуноглобулинов и комплексов антиген— антитело (Fc) и третьего компонента комплемента (к). Из него дифференцируется клетка, несущая Fc, к, рецепторы для IgD и IgM (ц). И, наконец, этот предшественник дифференцируется в три категории В-лимфоцитов; все они характеризуются наличием Fc- и к-рецепторов и, кроме того, содержат либо рецептор а (для IgA), либо у (для IgG), либо u.
При комбинированных иммунодефицитных состояниях, при которых отсутствуют как Т-, так и В-клетки, поражена, видимо, стволовая кроветворная клетка. Это подтверждается способностью костного мозга, трансплантированного таким больным, излечивать иммунодефицит. Поражение ранних клеток-предшественников Т- или В-лимфоцитов происходит, видимо, при остром лимфолейкозе и агаммаглобулинемии. Поражение следующего предшественника в ряду Т-клеток наблюдается при хроническом лимфолейкозе (Т-клеточная форма), а в ряду В-клеток — при В-клеточном хроническом лимфолейкозе, не несущем иммуноглобулиновых маркеров, и при некоторых формах агаммаглобулинемии. При синдроме Сезари поражается, видимо, более зрелый предшественник Т-лимфоцитов, чем при хроническом Т-клеточном лимфолейкозе, так как злокачественные клетки при этом заболевании дают простые розетки с эритроцитами барана (60—90% всех клеток) при отсутствии на поверхности Fc и иммуноглобулинов. И, наконец, при поражении наиболее зрелых клеток В-ряда развиваются заболевания типа нодулярной лимфомы, В-клеточного хронического лимфолейкоза (вариант с иммуноглобулинами на клеточной поверхности), лимфомы Бэркитта и некоторые формы агаммаглобулинемии. – Также рекомендуем “Регуляция пролиферации стволовых клеток. Свойства стволовой клетки” Оглавление темы “Регуляция пролиферации стволовых клеток”: |
Источник
Образование Т-клеток в тимусе. Заселение тимуса предшественниками лимфоцитовОбразование Т-клеток в тимусе происходит из потомков костномозговых стволовых кроветворных клеток. Эмигрируя из костного мозга, они попадают по току крови в тимус и проникают в его ткань в области коркового слоя. В тимусе они активно пролиферируют и подвергаются дифференцировке и коммитированию. Их потомки перемещаются в корковый слой и либо гибнут внутри тимуса, либо покидают его, вновь поступая в кровоток. Стадии дифферепцировки, которые проделывают предшественники Т-клеток в тимусе, имеют антигенные, функциональные и морфологические маркеры. Наименее зрелые предшественники характеризуются высокой чувствительностью к кортизону, высокой концентрацией антигенов TL и Ly и низкой концентрацией Н2-антигенов. Морфологически эти клетки являются малыми лимфоцитами, содержащими монорибосомы и относительно мало органоидов. Они дают начало пролиферирующим в тимусе большим лимфоцитам с резко увеличенным количеством рибосом, собранных в полисомы в виде розеток. Наиболее зрелые в пределах тимуса Т-клетки находятся в его мозговом слое. Они резистентны к кортизону, имеют малые концентрации TL- и 8-антигенов, но много Н2-антигена. Морфологически — это малые лимфоциты, но содержащие полирибосомы и волокнистые цитоплазматические структуры. Таких клеток в тимусе содержится около 5% от всех тимоцитов, и именно они могут выходить из тимуса в кровоток и осуществлять колонизацию периферических лимфоидных органов в качестве антигенраспознающих, уже коммитированных Т-клеток. Окончательное дозревание Т-клеток происходит только после их попадания, во вторичные лимфоидные органы.
Гибель подавляющей части тимоцитов внутри тимуса позволяет предполагать, что избыточная пролиферация в нем Т-предшественников связана с апробированием их свойств и отбором еще до встречи с антигенами; последние практически не попадают в тимус благодаря наличию специального барьера. При заселении тимуса предшественниками Т-клеток ориентирами для них служат не лимфоциты (тимоциты) и не макрофаги (которые в тимусе крайне малочисленны), а клетки его стромы. На это указывают результаты типирования клеток в гетеротопных трансплантатах тимуса (Дидух, Фриденштейн, 1970). Стромальные клетки тимуса — ретикулярные клетки, или клетки его эктодермального эпителия,— создают и то микроокружение, которое необходимо для дифференцировки Т-клеток: в отсутствие тимической стромы Т-клетки в организме не образуются. Однако результаты, полученные на радиохимергх и при гетеротопной трансплантации тимуса, показали, что свойства образующихся в тимусе Т-клеток определяются генетической структурой заселяющих его предшественников, а не стромальными клетками, образующими территорию, на которой происходит их дифференцировка. Действительно, в случаях, когда тимэктомированный реципиент и донор тимуса, используемого для гетеротопной трансплантации, различаются по антигенам, тимоциты, которые образуются в пересаженном тимусе, имеют 6-антиген реципиента, а в случае, когда по 6-антигенам различаются донор клеток костного мозга и облученный реципиент, тимоциты радиохимеры имеют 6-антиген донора (Metcalf, Moore, 1971). Это показывает, что роль тимического микроокружения как индуктора образования Т-клеток состоит в создании возможности для реализации тех генетически закодированных в потомках стволовых кроветворных клеток свойств, которые характеризуют дифференцировку Т-клеток. Важный фактор тимического микроокружения — это секретируемый его стромальными клетками полипептид — тимозин (м. в. 35 000). Тимозин индуцирует созревание Т-клеток из костномозговых предшественников (в частности, синтез 6-антигена) как in vivo, так и in vitro (Scheid e. a., 1973). Исчерпывается ли специфическое действие тимического микроокружения секрецией тимозина, пока не выяснено. – Также рекомендуем “Колонизация периферических лимфоидных органов. Репопуляция лимфоцитов” Оглавление темы “Регуляция формирования антител”: |
Источник
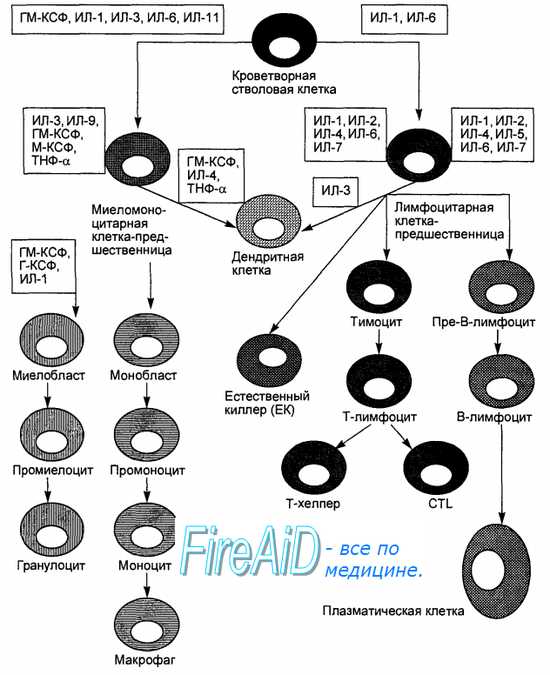
Оглавление темы “Иммунная система. Функции клеток иммунной системы. Т-лимфоциты. В-лимфоциты. Структура и функции органов иммунной системы.”: Костный мозг. Функции костного мозга. Миеломоноцитопоэз.Продолжая функцию эмбриональной печени, костный мозг является местом гемопоэза, в том числе лимфопоэза (рис. 8.3). Единая гемопоэтическая стволовая клетка может дифференцироваться в сторону общей клетки-предшественницы лимфоцитов. Эта клетка дает начало клеткам-предшественницам В-лимфоцитов, Т-лимфоцитов и естественных киллеров. Дальнейшая дифференцировка лимфоцитов зависит от влияния колониестимулирующих факторов, продуцируемых стромальными клетками костного мозга. Созревающие активированные лимфоциты начинают продуцировать цитокины, аутокринно влияющие на их пролиферацию и дифференцировку. Так, интерлейкин-1 и интерлейкин-6 служат синергиста-ми колониестимулирующих факторов в стимуляции пролиферации клеток-предшественниц; интерлейкин-2 является ростовым фактором Т-лимфоцитов; интерлейкины-4, -6, -7 способствуют выживанию, пролиферации и дифференцировке ранних предшественниц лимфоцитов; туморнекротизи-рующий фактор (ТНФ), гамма-интерферон, трансформирующий ростовой фактор-бета (ТРФ-бета), напротив, ингибируют процессы пролиферации и дифференцировки клеток-предшественниц.
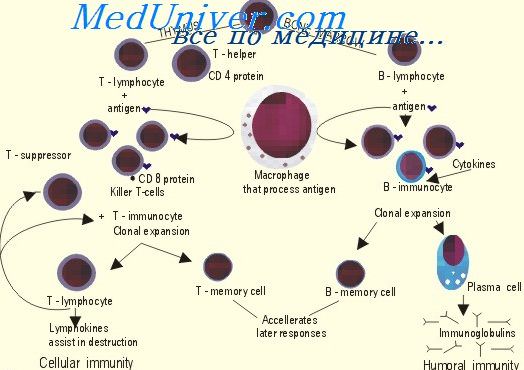
Созревшие в костном мозге клетки-предшественницы Т-лимфоцитов через кровоток попадают в тимус для дальнейшей дифференцировки. В отличие от Т-лимфоцитов, местом дальнейшего созревания В-лимфоцитов у млекопитающих является костный мозг. Один из продуктов стромальных клеток костного мозга — интерлейкин- 7 преимущественно стимулирует процесс созревания В-лимфоцитов из костномозговых предшественников. Созревшие В-лимфоциты выходят в кровь, заселяют лимфоидные органы, участвуют в рециркуляции, проявляя способность к распознаванию конкретного антигена. Распознавание антигена служит одним из сигналов активации В-лимфоцитов и их дальнейшей дифференцировки в плазматические клетки, продуцирующие и секретирующие антитела (иммуноглобулины). Иммуноглобулины продуцируются в костном мозге и в периферических органах иммунной системы, откуда поступают в кровоток. Таким образом, костный мозг в качестве одного из центральных органов иммунной системы выполняет следующие функции: является местом начальной дифференцировки и пролиферации ранних клеток-предшественниц лимфоцитов; является местом дальнейшей дифференцировки В-лимфоцитов вплоть до их выхода в кровоток и заселения периферических органов иммунной системы; является местом продукции и секреции колониестимулирующих факторов и цитокинов, влияющих на процессы пролиферации, дифференцировки и транспортировки Т- и В-лимфоцитов; является одним из мест продукции и секреции антител (иммуноглоблинов). – Также рекомендуем “Тимус (вилочковая железа). Тимоциты. Функции тимуса ( вилочковой железы ). Этапы отбора тимоцитов.” |
Источник