Побочные эффекты после лучевой терапии лимфоузлов

2 марта 2020
24917 917
Показать содержание статьи
Онкологические заболевания могут развиваться стремительно, распространяясь и поражая соседние органы. Все применяемые сегодня способы лечения рака достаточно агрессивны для организма и имеют побочные эффекты. Радиолучевая терапия – это один из способов борьбы с раковой опухолью, стоящий на втором месте по эффективности после хирургического вмешательства. По отчету Королевского колледжа радиологов (Великобритания) среди успешно пролеченных от рака пациентов 49 % из них удалили опухоли хирургически, 40 % прошли успешное радиологическое лечение, 11 % излечились благодаря химиотерапии.
Что это такое
Рентгено-, радио-, телегамма-, протоно-, нейтронная терапия и др. – это направленное действие пучков элементарных частиц или жесткого электромагнитного излучения на раковые клетки. Жесткое излучение вызывает разрывы цепочек ДНК и хромосомные мутации, размножение и деление клеток угнетается, из-за чего опухоли значительно уменьшаются либо разрушаются полностью. Расположенные вблизи здоровые клетки также повреждаются, но они обладают способностью к восстановлению. Крайне важно, чтобы интенсивность и направленность излучения были заранее точно просчитаны, так как даже относительно небольшое превышение терапевтической дозы может вызвать очень серьезные, а в некоторых случаях необратимые последствия.
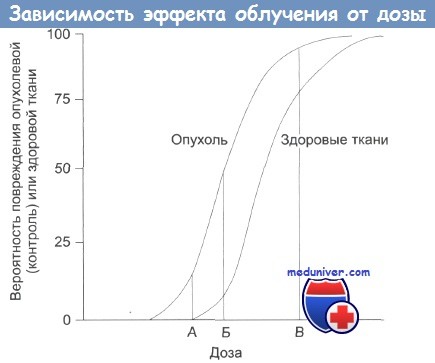
Чувствительность опухолей и здоровых тканей к лучевой терапии
Лучевая терапия применяется для лечения разных видов рака. Здоровые клетки органов и опухолей имеют различную радиочувствительность и способность к регенерации. От различия этих параметров напрямую зависит успешное уничтожение раковых клеток при помощи облучения. Чем более радиочувствительны клетки опухоли, тем меньшие дозы облучений можно применять.
Радиочувствительность здоровых тканей. Высокочувствительными принято считать костный мозг, гонады, кишечник, лимфотоки, глаза (хрусталик). К среднечувствительным относятся печень, легкие, почки, кожа, молочные железы, стенки кишечника, нервная ткань. Относительно нечувствительными считают кости, мышечную и соединительную ткани.
Радиочувствительность опухолей. К высокочувствительным новообразованиям относятся лимфомы, лейкемии, семинома, саркома Юинга, эмбриональные опухоли. К среднечувствительным – мелкоклеточный рак легкого, молочной железы, плоскоклеточные карциномы, аденокарцинома кишечника, глиома. К относительно нечувствительным относятся саркома костной и соединительной тканей, меланома.
Организация лечения
Для успеха применения радиолечения крайне важна правильная организация процесса лучевой терапии, начиная с планирования и заканчивая реабилитацией после лечения. Современные отделения радиационной терапии оснащены разнообразным оборудованием как для поверхностного облучения, так и для воздействия на глубоко залегающие злокачественные новообразования. В подготовке к лучевой терапии принимают участие терапевты-радиологи и физики.
Подбор оборудования для облучения. В зависимости от размещения источника излучения относительно тела, различают следующие их разновидности:
- внутритканевый – его вводят непосредственно в больной участок в виде раствора, игл, зондов;
- внутриполостной – когда он помещен в какую-либо полость тела;
- дистанционный – соответственно находится на расстоянии от тела.
В настоящее время уже применяется техника, позволяющая использовать множественные поля облучения, что позволяет индивидуально и точно выбирать режимы облучения конкретных пациентов.
Планирование процесса лечения. Процесс расчета оптимальных доз, временных периодов и участков воздействия лучевой терапии называется планированием. Эти сложные расчеты проводятся совместно высококвалифицированными радиологами, физиками, дозиметристами, математиками. При использовании современных компьютерных технологий создаются карты изодозных кривых. На данных картах определяются районы тела, получающие эквивалентные поглощенные дозы, а также проводится необходимая коррекция поглощенной дозы для органов и тканей с нерегулярной плотностью, таких как легкие и кости. Пациент также принимает участие в планировании. При помощи специального рентгеновского аппарата на теле лежащего пациента медики определяют поле облучения и проводят маркировку соответствующих участков. Эти маркировочные линии остаются до конца курса лучевой терапии. В довершение планирования проходит обсуждение возможных способов фиксации для того, чтобы пациент не мог пошевелиться во время экспозиции.
Изготовление защитных экранов и фиксирующего оборудования. При радиологических отделениях больниц работают специальные мастерские, в которых специалисты изготавливают для пациентов различные индивидуальные иммобилизирующие устройства. Такие, как, например, шлем из оргстекла для фиксации головы в определенном положении при облучении опухолей мозга и шеи. А также вырезают защитные экраны сложной формы из свинцовых пластин для создания индивидуального поля облучения на различных частях тела.
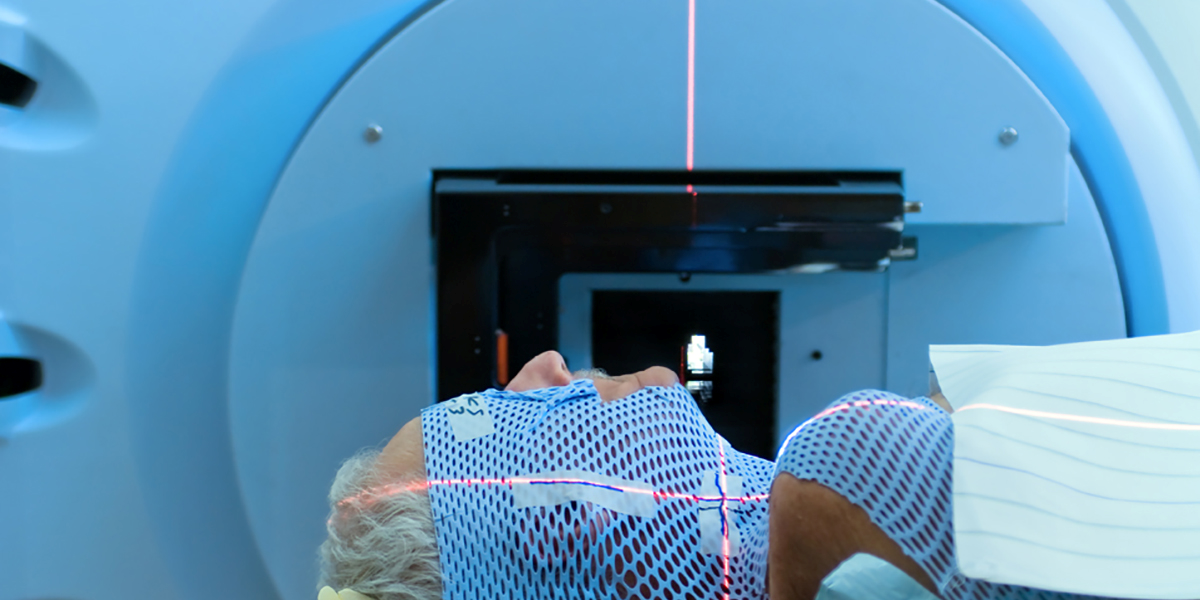
Возможные последствия
Последствия лучевой терапии делятся на острые побочные явления во время и после процедуры и отложенные (хронические) эффекты. На вероятность возникновения осложнений влияет физическое состояние и возраст пациента, тип онкологии и стадия развития патологии.
Побочные явления во время и после облучения. Часто во время и после процедур могут наблюдаться следующие симптомы:
- болевые ощущения и воспалительные процессы в облучаемых органах;
- чувство усталости и эмоциональной подавленности;
- снижение аппетита, тошнота;
- локальные ожоги кожи;
- нарушение в работе желудочно-кишечного тракта, диарея, спазмы.
Чаще всего побочные явления, развивающиеся во время лечения, нетяжелые. Они поддаются медикаментозному лечению или проходят благодаря коррекции рациона. Через две-три недели после окончания лучевой терапии они исчезают. У части пациентов побочные явления не возникают.
Отложенные последствия. Иногда пациенты чувствуют ухудшение состояния через полгода, год, несколько лет после окончания лучевой терапии. Поздние осложнения могут быть вызваны запуском механизмов тканевого нарушения, связанного с радиоповреждением эндотелия – внутреннего покрытия кровеносных сосудов. Закупорка мелких сосудов и последующая тканевая гипоксия приводят к фиброзу пораженных тканей. Среди отложенных последствий, в зависимости от места облучения, встречаются:
- радиационный некроз мягких тканей;
- снижение емкости мочевого пузыря, гематурия;
- кишечная непроходимость;
- образование свищей;
- утрата способности к зачатию;
- образование вторичных опухолей.
Некоторые из этих состояний поддаются хирургическому лечению.
Причины возникновения тяжелых последствий
Доказано, что радиация обладает канцерогенным, мутагенным и тератогенным воздействием, нарушая ядерные связи в структуре ДНК и повреждая генетический материал. Рассмотрим механизм возникновения вторичных опухолей. После облучения в высокой дозе ткань раковой опухоли исчезает, а окружающие нормальные ткани остаются. Но в них сохраняются однажды привнесенные радиацией изменения. Здоровая клетка, постоянно обновляясь, может устранить такие повреждения, но до определенного уровня. При подходящих условиях они все-таки передаются последующим поколениям клеток. Существует вероятность, что повреждения будут накапливаться, и спустя десятки лет это приведет к возникновению вторичной опухоли. Такие случаи известны медицине, хоть и достаточно редки. Следует также помнить, что остаточные лучевые повреждения обязательно должны учитываться при проведении лечебных процедур на данных частях тела в будущем, так как облученные ткани в целом хуже заживают.
Влияние на плод
Лучевая терапия запрещена у беременных из-за тератогенного свойства радиации. Среди причин:
- самопроизвольное патологическое прерывание беременности;
- перинатальная и неонатальная смертность;
- возникновение у плода серьезных пороков развития, включая микроцефалию и замедленное умственное развитие.
Если больная в период от 10 дней до 26 недель беременности подвергалась лучевой терапии, следует рассмотреть вопрос об искусственном прерывании беременности.
Новые методы
Медицинская наука не стоит на месте. Десятки ведущих ученых в развитых странах занимаются разработкой новых и совершенствованием существующих видов лечения онкологических заболеваний. В некоторых клиниках уже внедряются новейшие достижения в области лучевой терапии. Перечислим некоторые из них.
Интраоперационное облучение. В операционной, открыв доступ к больному органу и четко различая зону поражения, врачи направляют на нее воздействие пучка электронов, максимально отодвигая в сторону кишечник и другие чувствительные органы, чтобы не нанести им вреда.
Трехмерная конформная лучевая терапия. Данные компьютерной томографии в цифровом виде связывают с лечебным аппаратом таким образом, что на выходе создается форма пучка, соответствующая конфигурации опухоли-мишени. Врач корректирует направление в случае необходимости. При данном методе очень важна дополнительная иммобилизация пациента.
Лучевая терапия с модуляцией интенсивности. Эта методика основана на использовании специального программного обеспечения, которое рассчитывает сотни вариантов лечения, чтобы получить дозу, максимально возможную для клеток опухоли при минимальной степени вреда для нормальных клеток, при этом оптимальной конфигурации и интенсивности. В компьютер вводят данные о форме и месте дислокации опухоли, верхних пределах возможных значений доз для структур окружающих органов. На выходе устройства у оптического прицела-коллиматора имеются подвижные «лепестки», модулирующие интенсивность и конфигурацию конечной формы поля воздействия. Этот метод уже показал снижение числа осложнений у пациентов при лечении опухолей головного мозга, органов брюшной полости, женской и мужской половой сферы.
Стереотаксическая лучевая терапия. Данный метод по принципу действия схож с двумя предыдущими. Специальный модифицированный линейный ускоритель применяется точечно для подведения высокой дозы излучения к небольшой по размерам опухоли или метастазам. Чаще всего применяется при лечении опухолей головного мозга.
Иммунная терапия с радиоактивными метками. Новейшее достижение медицинской микробиологии – терапия при помощи моноклональных антител. Моноклональными называют антитела, вырабатываемые иммунными клетками, полученными из одной плазматической клетки с заданными свойствами, действующие против любых природных антигенов. В клинической онкологии уже применяют инфузии препарата, содержащего моноклональные антитела, меченные радионуклидами. Этим способом радиоактивный изотоп подводится к строго определенной мишени антитела. Метод успешно применяют в лечении лимфом. Ведется разработка препаратов для лечения онкогинекологических заболеваний.
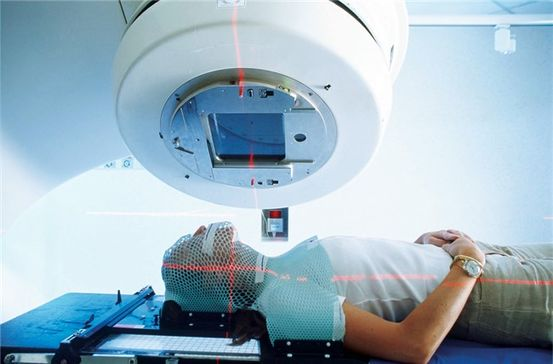
Реабилитация
После облучения человеческому организму требуется продолжительный период восстановления. Процесс реабилитации – это заключительный и очень важный этап лучевой терапии. Он может проходить дома или в тяжелых случаях в условиях стационара. Врач дает подробные рекомендации, обязательно включающие в себя индивидуальный рацион, распорядок дня, легкие физические нагрузки, режим трудовой деятельности и отдыха. Особо отмечается необходимость беречь облученные участки кожи от прямых солнечных лучей не менее года. Неукоснительное выполнение больным всех рекомендаций поможет его организму восстановить нормальную работу всех своих систем. По окончании периода реабилитации пациенту назначаются даты обязательных контрольных осмотров. При ухудшении состояния больному следует обратиться к лечащему врачу, не дожидаясь установленных сроков. Примерный перечень таких симптомов:
- повышение температуры тела, кашель;
- боль, не проходящая в течение 3–5 дней;
- потеря аппетита, тошнота, понос;
- появление опухоли или отека в области облучения;
- появление кожных высыпаний.
Последние исследования результатов лечения онкологических больных с применением лучевой терапии показывают, что с 90-х годов прошлого века риск осложнений значительно снизился благодаря применению качественно новых целенаправленных техник облучения. Все больше и больше пациентов, прошедших лучевую терапию, полностью восстанавливаются и сохраняют здоровье на долгие годы.
Источник
Осложнения лучевой терапии головы, шеи и ее побочные эффектыВсе побочные эффекты лучевой терапии можно подразделить на острые и хронические. Их возникновение зависит от общей дозы облучения, однократной дозы облучения, предыдущего или сопутствующего лечения (хирургического вмешательства и/или химиотерапии), объема опухоли. Одним из главных факторов, ограничивающих дозу лучевой терапии, является мукозит. Выраженный лучевой мукозит может стать причиной перерывов в лечении с последующим рецидивом опухолевого роста. Если иммунная система больного подорвана химиотерапией, слизистые оболочки могут инфицироваться. Наиболее распространенным хроническим побочным эффектом является ксеростомия. С целью повышения вероятности успеха лучевой терапии пациент должен отказаться от курения (курение повышает сопротивляемость опухолевых клеток облучению), тщательно следовать схеме лечения, избегая перерывов более чем на пять дней, активно искать поддерживающей терапии. Перед началом лечения пациента должен обследовать фониатр/специалист по глотанию, диетолог, специалист по контролю боли и психолог. Все они могут помочь пациенту справиться с острыми и хроническими побочными эффектами лучевой терапии. Также перед началом лучевой терапии пациента должен осмотреть стоматолог, необходимо выполнить ортопантомограмму, при необходимости удалить больные зубы, приобрести фторированные каппы для зубов, которые могут быть полезны у больных с пломбами (наличие пломб ведет к более выраженному мукозиту, т. к. ионизирующее облучение рассеивается при встрече с пломбировочным материалом).
а) Острые побочные эффекты лучевой терапии головы и шеи. Побочные эффекты обычно появляются на третьей неделе лечения. Развивается дерматит, снижается секреция слизи, появляются охриплость, боли в горле, дисфагия, утомляемость, нарушения вкуса, ксеростомия. В редких случаях на первой неделе может развиваться паротит (вследствие закупорки выводных протоков железы густой слизью). Ближе ко второй половине курса, когда симптомы усиливаются, у пациентов появляется необходимость в использовании кремов и масел для кожи, муколитиков, наркотических анальгетиков, противорвотных препаратов, изменений в диете (переход на жидкую пищу и жидкие питательные смеси). Пациентам, которые не способны перенести весь курс лечения (особенно в сочетании с химиотерапией), может быть наложена гастростома. Пациенты могут сильно терять в весе, у них нарушается заживление ран. Все это ведет к сложностям с завершением курса лечения. Важно минимизировать любые перерывы в лечении, поскольку подавление роста опухоли нарушается при прерывании лечения на пять дней и более. б) Хронические побочные эффекты лучевой терапии головы и шеи. Полное восстановление после курса лучевой терапии занимает несколько недель или месяцев. Отказаться от приема дополнительных препаратов пациенты обычно могут спустя 4-6 недель после окончания лечения. Наиболее тяжелыми хроническими побочными эффектами являются фиброз мягких тканей шеи и жевательной мускулатуры, выпадение волос, хондронекроз, дисфагия, гипотиреоз, ксеростомия. Избежать образования стриктур верхнего сфинктера пищевода и фиброза мышц, участвующих в глотании, можно при раннем начале специальных глотательных упражнений. Невозможность нормального глотания может вести к хронической аспирации и необходимости постоянного использования назогастрального зонда. Для предотвращения распада зубов и остеорадионекроза пациенты должны тщательно соблюдать гигиену полости рта, избегать удаления или имплантации зубов. в) Направление будущих исследований. В рандомизированном исследовании RTOG-H5022 будет оценена эффективность добавления С225 к курсу химиолучевой терапии (ускоренный курс облучения с двумя курсами цисплатина). С учетом того, что у пациентов с раком ротоглотки, ассоциированным с ВПЧ, удается достичь превосходных результатов при использовании традиционных методов лечения, многие лечебные учреждения и исследовательские группы занимаются поиском наименее агрессивного варианта. Аналогичных результатов можно достичь использованием меньших доз облучения и меньшим количеством курсов химиотерапии, снизив при этом общую токсичность. У пациентов с крайне агрессивными опухолями, которым требуется более радикальное лечение, возможно применение нескольких подходов: использование индукционной химиотерапии, эскалация дозы облучения, подключение брахитерапии или биологической терапии. С другой стороны, ведется поиск радиопротективных препаратов, которые помогут предотвратить развитие мукозита и других побочных эффектов и одновременно с этим увеличить вероятность сохранения функции пораженного органа, поскольку целью лечения является не только подавление опухолевого роста, но и поддержание общего качества жизни на достойном уровне. Например, исследуется возможность использования лучевой терапии с модулированной интенсивностью (ЛТМИ) для снижения риска развития дисфагии и снижения дозы химиолучевой терапии. Это позволит сохранить пациентам глотание и устранит необходимость в использовании назогастрального зонда. С целью дальнейшей персонализации лечения разрабатываются новые методы лучевой диагностики и молекулярной диагностики, с помощью которых, как мы надеемся, удастся найти сбалансированный способ излечения с использованием минимально допустимых доз и косметическими и функциональными результатами лечения.
г) Ключевые моменты лучевой терапии: – Также рекомендуем “Особенности анатомии полости рта” Оглавление темы “Болезни полости рта и глотки”:
|
Источник