Механизмы цитотоксического действия лимфоцитов
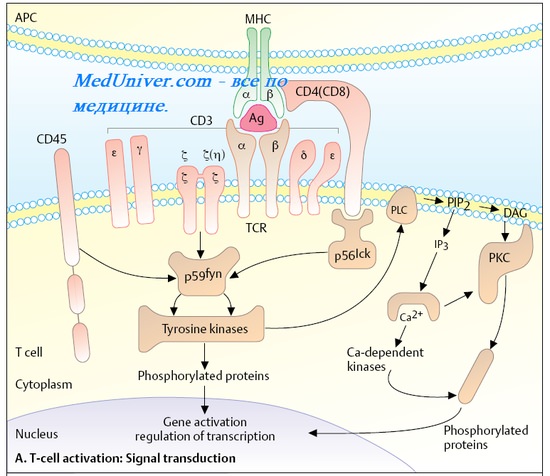
Т-ки́ллеры, цитотокси́ческие T-лимфоци́ты, CTL (англиц. killer «убийца») — вид Т-лимфоцитов, осуществляющий лизис повреждённых клеток собственного организма. Мишени Т-киллеров — это клетки, поражённые внутриклеточными паразитами (к которым относятся вирусы и некоторые виды бактерий), опухолевые клетки. Т-киллеры являются основным компонентом антивирусного иммунитета.
Механизм действия[править | править код]
Многие возбудители заболеваний находятся внутри поражённых клеток вне досягаемости для гуморальных факторов иммунитета (таких, как антитела). Чтобы справиться с внутриклеточными паразитами, возникла обособленная система клеточного приобретённого иммунитета, основанная на функционировании T-киллеров. Т-киллеры непосредственно контактируют с повреждёнными клетками и разрушают их. В отличие от NK-клеток, T-киллеры специфически распознают определённый антиген и убивают только клетки с этим антигеном. Существуют десятки миллионов клонов T-киллеров, каждый из которых «настроен» на определённый антиген. (Рецептор T-лимфоцитов структурно отличается от молекулы мембранного иммуноглобулина — рецептора B-лимфоцитов). Клетки клона начинают размножаться при попадании соответствующего антигена во внутреннюю среду организма после активации Т-киллеров Т-хелперами. T-лимфоциты могут узнать чужеродный антиген только в том случае, если он экспрессирован на поверхности клетки. Они узнают антиген на поверхности клетки в комплексе с клеточным маркером: молекулами MHC класса I. В процессе распознавания поверхностного антигена цитотоксический T-лимфоцит вступает в контакт с клеткой-мишенью и в случае обнаружения чужеродного антигена уничтожает её до начала репликации. Кроме того, он продуцирует гамма-интерферон, который ограничивает проникновение вируса в соседние клетки.
Большинство цитотоксических T-клеток относится к субпопуляции CD8+ и распознает антиген, презентированный в ассоциации с молекулами MHC класса I, но меньшая их часть (примерно 10 %), относящаяся к субпопуляции CD4+, способна распознавать антиген в ассоциации с молекулами MHC класса II[1]. Опухолевые клетки, лишённые MHC I, Т-киллерами не распознаются.
Активированные Т-киллеры убивают клетки с чужеродным антигеном, к которому имеют рецептор, вставляя в их мембраны перфорины (белки, образующие широкое незакрывающееся отверстие в мембране) и впрыскивая внутрь токсины (гранзимы). В некоторых случаях Т-киллеры запускают апоптоз заражённой клетки через взаимодействие с мембранными рецепторами.
Формирование и размножение цитотоксических Т-лимфоцитов[править | править код]
Цитотоксические T-лимфоциты развиваются в тимусе. В образовании уникального Т-клеточного рецептора участвуют сложные механизмы, включающие контролируемый мутагенез и рекомбинацию определённых участков генома. Как и Т-хелперы, Т-киллеры проходят положительную (выживают клетки, хорошо распознающие MHC) и отрицательную (уничтожаются клетки, активирующиеся собственными антигенами организма) селекцию. Предшественники цитотоксических клеток активируются комплексом антигена и молекул MHC класса I, размножаются и созревают под действием интерлейкина-2, а также еще плохо идентифицированных факторов дифференцировки. В ходе селекции бо́льшая часть клонов предшественников T-лимфоцитов погибает посредством индуцированного апоптоза.
Сформированные Т-киллеры циркулируют по кровеносной и лимфатической системам, периодически возвращаясь (хоминг лимфоцитов) в лимфоидные органы (селезёнку, лимфатические узлы и др.). При получении сигнала активации от Т-хелперов определённый клон Т-киллеров начинает пролиферацию (размножение).
Примечания[править | править код]
- ↑ А. Ройт, Дж. Бростофф, Д. Мейл. Иммунология. М., «Мир», 2000. Стр. 179
См. также[править | править код]
- Иммунная система
- Тимус
- Т-хелперы
- B-лимфоциты
- Естественные киллеры
Источник
Оглавление темы “СD8 лимфоциты. Антиген ( Аг ) представляющие клетки. Классификация антигенов ( Аг ).”:
1. Рецептор Т-клеток. Активация Т-лимфоцитов. Субпопуляции Т-лимфоцитов. СD4+ лимфоциты.
2. СD8 лимфоциты. Т супрессоры. Цитотоксические Т-лимфоциты ( ЦТЛ ). Т-киллеры. Цитотоксический эффект Т-киллеров. Т-клетки памяти.
3. В-лимфоциты. В-клетки. Созревание В-лимфоцитов. Продолжительность жизни B-лимфоцитов. Маркеры В-клеток ( В-лимфоцитов ).
4. Естественные киллеры ( NK-клетки ). Перфорины. Функция естественных киллеров. Задачи NK-клеток.
5. Антиген ( Аг ) представляющие клетки. Иммунные реакции. Классификация имунных реакций. Антигены. Свойства антигенов. Структура антигенов ( Аг ). Валентность Аг.
6. Классификация антигенов ( Аг ). Иммуногены. Гаптены. Непреципитирующие гаптены. Преципитирующие гаптены. Полугаптены. Проантигены.
7. Адъюванты. Адъювант Фройнда. Толерогены. Природа антигенов (Аг). Происхождение антигенов. Молекулярная масса антигенов (Аг).
8. Специфичность антигенов (Аг). Видовые антигены. Групповые антигены (Аг). Гетерогенные антигены (Аг). Антиген Форссмана. Аллоантигены ( изоантигены ).
9. Патологические антигены. Аутоантигены. Врождённые аутоантигены. Приобретённые аутоантигены. Суперантигены.
10. Антигены ( Аг ) микроорганизмов. Антигены бактерий. Капсульные антигены ( К-антигены ( Аг )). Соматические антигены ( O-антигены ( Аг )). Жгутиковые антигены ( H-антигены ( Аг )). Vi-Ar ( Антиген вирулентности ).
СD8 лимфоциты. Т супрессоры. Цитотоксические Т-лимфоциты ( ЦТЛ ). Т-киллеры. Цитотоксический эффект Т-киллеров. Т-клетки памяти.
СD8+-лимфоциты. Мембранные Аг CD8 экспрессируют субпопуляции Т-клеток, разделяемые на регуляторные (супрессоры) и эффекторные (цитотоксические Т-лимфоциты).
Т супрессоры.
Т-супрессоры [от англ. to supress, подавлять) регулируют интенсивность иммунного ответа, подавляя активность СD4+-клеток. Т-супрессоры предотвращают развитие аутоиммунных реакций, защищают организм от нежелательных последствий иммунных реакций. Эти клетки обеспечивают толерантность матери к чужеродным Аг, представленным на клетках вынашиваемого плода. Это даёт возможность развиваться чужеродному в иммунном отношении плоду в организме матери. Т-супрессоры дифференцируются из предшественников в результате антигенной стимуляции. По-видимому, активация супрессоров находится вне контроля МНС, и представления Аг макрофагом не требуется. Аутоантигены могут стимулировать развитие ауторегуляторных Т-супрессоров.
Чужеродные Аг в неиммуногенной форме (гаптены) или иммуногенные Аг в очень высокой концентрации также способны индуцировать специфическую супрессорную активность клеток. После распознавания Аг зрелые лимфоциты препятствуют развитию иммунного ответа, действуя непосредственно на клетки или секретируя супрессорные факторы.
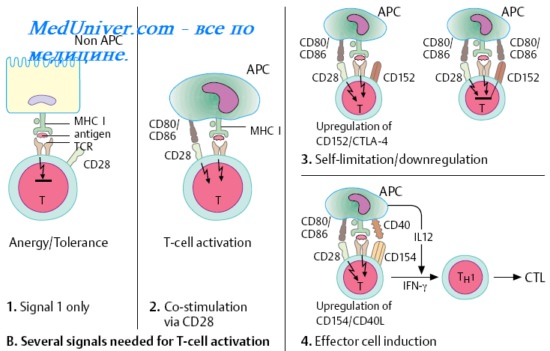
Цитотоксические Т-лимфоциты ( ЦТЛ ). Т-киллеры. Цитотоксический эффект Т-киллеров.
Цитотоксические Т-лимфоциты (ЦТЛ), или Т-киллеры [от англ. to kill, убивать] лизируют клетки-мишени, несущие чужеродные или видоизменённые аутоантигены (например, клетки опухолей, трансплантатов, инфицированные вирусами, клетки, несущие поверхностные вирусные Аг). В большинстве случаев функция ЦТЛ также МНС-рестригирована — цитотоксические Т-лимфоциты распознаёт чужеродный вирусный, опухолевый или трансплантационный Аг в комплексе с молекулой МНС I на мембране клетки-мишени. Индукция цитотоксических свойств клетки-предшественницы Т-киллера происходит под действием двух сигналов.
Первый сигнал включает взаимодействие между двумя комплексами: поверхностной молекулой CD8 лимфоцита и комплексом эпитоп-молекула МНС I на клетке-мишени. Второй сигнал — ИЛ, секретируемые близлежащими макрофагами и Т-клетками. Т-хелпер играет ключевую роль в стимуляции цитотоксических Т-лимфоцитов в качестве источника необходимых цитокинов, усиливающих их пролиферацию и созревание до функционально активных ЦТЛ.
Цитотоксический эффект Т-киллеров реализуется через образование в клетках-мишенях пор под действием особых белков — перфоринов. Нарушение осмотического баланса с внеклеточной средой приводит к гибели клетки.
Т-клетки памяти
Т-клетки памяти образуются при первичном иммунном ответе. Специфически распознают Аг и участвуют в иммунном ответе при вторичном попадании Аг. Большинство клеток памяти обладает функциями Т-клеток, экспрессируют CD4 и рестригированы по молекулам МНС II, то есть узнают Аг только на Аг-представляющих клетках в связи с молекулой МНС II.
– Также рекомендуем “В-лимфоциты. В-клетки. Созревание В-лимфоцитов. Продолжительность жизни B-лимфоцитов. Маркеры В-клеток ( В-лимфоцитов ).”
Источник
Оглавление темы “Клеточные имунные реакции. Иммунная память. Иммунное реагирование при инфекциях. Иммунодефициты.”:
1. Клеточные имунные реакции. Индукция Т-клеточно-опосредованных реакций. Клеточный иммунитет.
2. Уничтожение клетки-мишени цитотоксическими Т лимфоцитами. Альтернативный механизм уничтожения клетки-мишени. Реакции ГЗТ. Реакции гиперчувствительности замедленного типа.
3. Иммунная память. Бустер эффект. Вакцинопрофилактика.
4. Иммунное реагирование при инфекциях. Иммунный ответ при вирусных инфекциях. Гуморальные иммунные реакции при вирусемии ( вирусных инфекциях ).
5. Клеточные иммунные реакции при вирусных инфекциях. Иммунный ответ при бактериальных инфекциях.
6. Иммунный ответ при грибковых инфекциях. Иммунитет и грибы. Гуморальные реакции иммунитета при грибковых инфекциях. Клеточный иммунитет при грибковых инфекциях.
7. Иммунные реакции при протозойных инфекциях. Иммунитет при паразитах. Иммунная система при простейших в организме.
8. Толерантность иммунитета. Устойчивость иммунной системы. Механизмы поддержания толерантности иммунитета.
9. Естественная толерантность иммунитета. Искусственная толерантность иммунной системы. Иммунный паралич. Расщеплённая толерантность иммунитета. Нарушения толерантности иммунной системы. Аутоимунные заболевания.
10. Иммунодепрессивное состояние. Иммунодефициты. Врождённые иммунодефициты. Гиперкортицизм ( синдром Кушинга ). Двусторонняя гиперплазия коры надпочечников ( болезнь Иценко-Кушинга ) при иммунодефицитах. Ионизирующая радиация и иммунодефицит.
Уничтожение клетки-мишени цитотоксическими Т лимфоцитами. Альтернативный механизм уничтожения клетки-мишени. Реакции ГЗТ. Реакции гиперчувствительности замедленного типа.
Уничтожение клетки-мишени цитотоксическими Т лимфоцитами. Представленный на поверхности клетки-мишени Аг в комплексе с молекулой МНС I связывается с рецептором ЦТЛ. В этом процессе участвует молекула CD8 клеточной мембраны Т-клетки. Секретируемый Т-хелперами ИЛ-2 стимулирует пролиферацию ЦТЛ. ЦТЛ распознаёт клетку-мишень и прикрепляется к ней.
В цитоплазме активированного цитотоксического Т лимфоцита присутствуют мелкие гранулы, концентрирующиеся в той части цитотоксического Т лимфоцита, которая расположена в области контакта с клеткой-мишенью. Параллельно происходит переориентация цитоскелета, смещение в эту область комплекса Гольджи, в котором и формируются эти гранулы. Гранулы содержат белок перфорин.
Выделяемые цитотоксическими Т лимфоцитами молекулы перфорина полимеризуются в мембране клетки-мишени в присутствии Са2+ и формируют перфориновые поры, пропускающие воду и ионы, но не молекулы белка. В результате клетка-мишень погибает вследствие быстрого выравнивания ионного состава клетки и межклеточного пространства. Сам лимфоцит защищен от цитотоксического действия перфорина. Механизмы подобной самозащиты остаются неизвестными.

Альтернативный механизм уничтожения клетки-мишени
Нашло подтверждение представление о другом механизме цитотоксического действия, согласно которому цитотоксические Т лимфоциты и NK-клетки — источники сигнала, запускающего уже предеуществующую суицидальную программу в клетке-мишени. Действие этого сигнала усиливают глкжокортикоиды.
Реакции ГЗТ. Реакции гиперчувствительности замедленного типа
Тгзт-клетки распознают чужеродные Аг (преимущественно микроорганизмы), секретируют у-ИФН и другие лимфокины, стимулируя тем самым цитотоксичность макрофагов и усиливая другие Т- и В-клеточные ответы. ГЗТ— местный клеточно-опосредованный иммунный ответ. Реакции ГЗТ могут развиваться в любой ткани, но исторически их рассматривают в контексте кожного тестирования (например, проба с туберкулином). Кожная реакция ГЗТ развивается только у сенсибилизированного индивидуума приблизительно через 24-48 ч после внутри-кожного введения Аг.
В месте инъекции возникают эритема, уплотнение или, как крайняя степень реакции, некроз. Развитием гиперчувствительности замедленного типа на вводимый Аг отвечают только организмы с предсуществующей сенсибилизацией. Гистологически реакция ГЗТ характеризуется инфильтрацией очага: сначала нейтрофилами, затем лимфоцитами и макрофагами. Развитие реакции ГЗТ включает комплекс межклеточных взаимодействий, ведущих к активации макрофагов. Сенсибилизированные Тгзт распознают эпитопы (чаще внутриклеточных патогенов), представленные на мембране дендритных клеток, и секретируют цитокины, активирующие макрофаги и привлекающие другие провос-палительные клетки. Активированные макрофаги в свою очередь секретируют множество БАБ, вызывающих воспаление и уничтожающих бактерии, опухоли и другие чужеродные клетки. К этим БАВ относят цитокины (ИЛ-1, ИЛ-6, ФНО-а), активные метаболиты кислорода (О2-, ОН-, ОСl-, Н202 и др.), протеазы, катионные белки, лизоцим и лактоферрин.
– Также рекомендуем “Иммунная память. Бустер эффект. Вакцинопрофилактика.”
Источник
После реализации СD8+Т-лимфоцитами одной из своих важнейших функций — распознавания опухолевых антигенов, они приобретают способность осуществлять центральную эффекторную функцию — лизис клеток-мишеней.
Такая способность СD8+Т-лимфоцитов впервые была описана в 1960 г. A. Govaers в опытах с гомотрансплантацией почек.
В последующем получены доказательства, что цитотоксические лимфоциты (ЦТЛ) повреждают клетки-мишени при различных условиях — факт, отраженный во многих работах, который послужил основанием рассматривать эту функцию ЦТЛ как основной механизм клеточного иммунитета.
При описании антигенраспознающих функций ЦТЛ даны их характеристика и общие представления о механизме распознавания с участием этих клеток. Различные аспекты функционирования цитотоксических лимфоцитов подробно рассмотрены во множестве публикаций.
Подобно сведениям о СD4+Т-лимфоиитах, представления о ЦТЛ постоянно расширяются и пополняются новыми данными.
Цитотоксические лимфоциты в опухолевом процессе
Ниже представлены данные, касающиеся тех особенностей ЦТЛ, которые имеют существенное значение для понимания их роли в опухолевом процессе. Многие из них отражены в публикациях нового тысячелетия.
Рассмотрению вопроса о различных свойствах и эффекторных функциях цитотоксических лимфоцитов целесообразно предпослать ряд фактов, важных для понимания общих закономерностей функционирования ЦТЛ с позиций их участия в противоопухолевой защите.
Прежде всего необходимо отметить, что существовавшее традиционное представление в отношении ЦТЛ, как клетках, нуждающихся в обязательной помощи СD4+Т-лимфоцитов, в настоящее время звучит не столь догматично. Об этом свидетельствуют постепенно накапливающиеся данные, подтверждающие способность цитотоксических лимфоцитов развивать иммунологический ответ в отсутствие СD4+Т-лимфоцитов.
Например, в условиях прямого воздействия in vivo тетрамера главного комплекса гистосовместимости (ГКГ) показано, что при последовательной презентации антигенами ответ ЦТЛ может происходить без помощи СD4+Т-лимфоцитов и уровень этого ответа достаточно выражен. К аналогичному выводу пришли авторы, которые исследовали СD4+Т-лимфоциты и ЦТЛ, инфильтрирующие астроцитому, с целью получить ответ на вопрос, является ли присутствие СD4+Т-лимфоцитов необходимым для осуществления функций цитотоксических лимфоцитов.
Отрицательный ответ на этот вопрос они обосновывают тем, что молекулы II класса ГКГ слабо экспрессируются опухолевыми клетками, особенно клетками центральной нервной системы. Данные о том, что иммунологический ответ при астроцитомах ограничен ЦТЛ этими авторами получены впервые.
Необходимость участия СD4+Т-лимфоцитов в осуществлении иммунологического ответа в основном определяется особенностями антигенов, и поэтому при иммунизации одними антигенами ЦТЛ нуждаются в помощи СD4+Т-лимфоцитов, а при иммунизации другими — нет.
Интересные данные получены при исследовании белка теплового шока gp96 клеток различных линий мелкоклеточной карциномы человека; указанный белок может находиться и в секреторной форме, продуцируемой опухолевыми клетками.
Параллельным изучением gp96 и gp96-Ig установлено, что СD4+Т-лимфоциты необходимы лишь в ранней фазе иммунизации gp96-Ig, а в последующем этот антиген генерирует выраженный иммунологический ответ цитотоксических лимфоцитов без участия СD4+Т-лимфоцитов или макрофагов; иммунизация очищенным gp96 или облученными опухолевыми клетками в обоих случаях требует наличия СD4+Т-лимфоцитов.
Для правильной оценки функций ЦТЛ принципиально важен установленный факт диссоциации между цитотоксичностью и продукцией цитокинов — проявление киллерной активности уменьшается при продукции цитокинов. Подтверждением этому служат данные, полученные в различных экспериментальных системах.
Оказалось, что ЦТЛ проявляют высокую чувствительность к ингибиции пролиферации большими дозами антигена, что в конечном итоге приводит к апоптозу, обусловленному выделением высоких доз TNFa.
Однако такая ингибиция пролиферации не только не снижает цитотоксичность, но и усиливает ее — антигенный стимул, который подавляет пролиферацию, усиливает цитотоксичность. В результате сигнал, который должен индуцировать апоптоз, реализуется только после того, как цитотоксические лимфоциты выполнят свою цитотоксическую функцию.
Существование диссоциации между продукцией цитокинов и цитотоксичностью подтверждает и тот факт, что перфорин-дефицитные мыши обладают способностью к более активной продукции цитокинов.
Авторы объясняют это следующими причинами:
1) клетки, нагруженные антигеном, не имеют оптимальных условий для осуществления цитотоксичности;
2) период взаимодействия с мишенью возможно оказывается недостаточным для полной активации продукции цитокинов, но достаточным для осуществления цитотоксичности.
Оценив физиологическое значение диссоциации между цитотоксичностью и продукцией цитокинов, авторы пришли к заключению о том, что такой характер взаимодействия может регулировать функции ЦТЛ на различных этапах формирования иммунологического ответа (рис. 15).

Рис. 15. Соотношение различных функций ЦТЛ
Еще одним примером диссоциации продукции цитокинов и лизиса опухолевых клеток являются данные, полученные новыми методами исследований. В частности, с помощью lisispot assay показано, что продукция IFNy и цитотоксичность имеют независимую регуляцию.
Принципиальность факта отсутствия паралеллизма между продукцией цитокинов и цитотоксичностью заключается не только в правильном понимании соотношений между различными функциями цитотоксических лимфоцитов, но и имеет непосредственное значение для адекватной трактовки результатов иммунологических исследований в клинике.
Речь идет о том, что по уровню продукции ЦТЛ и/или их пролиферации, к сожалению, нередко судят об интенсивности цитотоксичности, что, как следует из представленных данных, не соответствует действительности.
Бережная Н.М., Чехун В.Ф.
Опубликовал Константин Моканов
Источник