Лимфорея после удаления лимфоузлов дренаж паховая
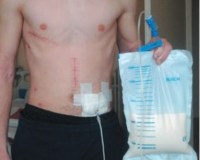
Лимфорея – это состояние, при котором лимфа вытекает на поверхность тела или в его полости. Развивается при ранениях крупных лимфатических протоков, операциях в зонах, богатых лимфатическими сосудами, спонтанном разрыве измененных сосудов на фоне ряда заболеваний. При наружных повреждениях выделяется прозрачная, затем мутная жидкость. При внутреннем истечении лимфы возникает воспалительный процесс. Лимфорея диагностируется с учетом анамнеза, данных осмотра, рентгенографии, лимфографии, плевральной пункции, лапароцентеза и других исследований. Лечение – тампонада или перевязка сосуда, инфузионная терапия.
Общие сведения
Лимфорея (lympha – влага, rhoe – течение), или лимфоррагия – достаточно редкое патологическое состояние. Может иметь травматическую или нетравматическую природу. Травматическая форма лимфореи чаще диагностируется у людей молодого и среднего возраста. Нетравматический вариант патологии выявляется преимущественно у пациентов средней и старшей возрастных групп. Незначительные потери лимфы не представляют опасности для организма. При массивной однократной лимфоррагии или хроническом истечении развивается истощение, возможен летальный исход.

Лимфорея
Причины лимфореи
Лимфоррагия является полиэтиологическим состоянием, возникает при травмах, операциях, некоторых заболеваниях. Основными причинами патологии считаются:
- открытые и закрытые травмы лимфатических сосудов значительного диаметра, чаще – грудного протока;
- случайное ранение сосудов или манипуляции на таких сосудах при операциях в некоторых анатомических зонах;
- разрыв измененных сосудов при лимфангиэктазиях, сосудистых опухолях, закупорке раковыми эмболами, особенно на фоне лимфостаза и лимфангиита.
Изменения хилезных сосудов с повышением вероятности их разрыва и развитием лимфореи могут наблюдаться как в области конечностей, так и в стенке внутренних органов, например, кишечника или мочевого пузыря. Хроническая недостаточность кровообращения ведет к формированию общей лимфедемы, при которой застой лимфы и поражение сосудов возникают во всех органах и системах.
Патогенез
Лимфатическая система дополняет кровеносную, участвует в обменных процессах, обеспечивает дренажную функцию, выводя из тканей воду и различные соединения. При нарушении целостности лимфатического сосуда организм теряет жидкость, белки, жиры и минералы, что приводит к обезвоживанию, нарушениям метаболического равновесия и истощению.
Классификация
Наряду с истечением хилезной жидкости наружу выделяют следующие варианты лимфореи:
- лимфоцеле – лимфа скапливается в тканях;
- хилоторакс – жидкость выявляется в плевральной полости;
- хилоперикард – лимфа вытекает в полость перикарда;
- хилоперитонеум – жидкость обнаруживается в брюшной полости.
Выделение лимфы с мочой вследствие ее истечения в мочевыводящие пути называется хилурией, просачивание через стенку кишечника приводит к развитию экссудативной энтеропатии.
Симптомы лимфореи
При наличии свежего открытого повреждения с нарушением целостности сосуда наблюдается выделение капель или истечение струйки прозрачной жидкости. При одновременном ранении кровеносных сосудов цвет отделяемого колеблется от слегка розоватого до почти красного. При отсутствии медицинской помощи через несколько дней рана инфицируется, вследствие чего хилезная жидкость становится мутной.
Формирование хилоперикарда сопровождается набуханием шейных вен, расширением границ сердца при перкуссии, ослаблением сердечных тонов при аускультации, возникновением или усилением проявлений сердечной недостаточности. При большом количестве жидкости в полости перикарда возможны гипотония, одышка, повышение венозного давления.
Незначительный хилоторакс протекает бессимптомно. При значительном объеме плеврального выпота отмечается дыхательная недостаточность, проявляющаяся одышкой и цианозом. Скопление менее 1 литра лимфы в области брюшной полости визуально не определяется. При хилоперитонеуме большего объема живот увеличивается, в положении стоя отвисает книзу, в положении лежа распластывается в стороны. В боковых отделах обнаруживается притупление перкуторного звука.
Хилурия проявляется окрашиванием мочи в молочно-белый цвет. При экссудативной энтеропатии наблюдаются стеаторея и хроническая диарея. При длительном выделении лимфы в кишечник определяются симптомы мальабсорбции. Если лимфорея в естественные полости и просвет полых органов развивается при сердечной недостаточности, у пациентов выявляются периферические отеки.
Осложнения
Значительные потери лимфоцитов при лимфорее могут стать причиной вторичного иммунодефицита. Из-за попадания бактерий в наружных ранах развивается инфекционный воспалительный процесс. При накоплении лимфы в естественных полостях (плевральной, брюшной, перикардиальной) нарушается работа внутренних органов, возникает асептическое хилезное воспаление. Массивные однократные или стойкие хронические потери лимфы приводят к кахексии.
Диагностика
В зависимости от причины развития лимфореи диагностикой данной патологии могут заниматься торакальные хирурги, онкологи, кардиологи и другие специалисты. Диагноз наружной лимфоррагии выставляют на основании анамнеза, жалоб и результатов физикального осмотра. При внутренних потерях лимфы необходимы дополнительные исследования. С учетом локализации лимфореи могут быть назначены следующие процедуры:
- Рентгенография. При хилотораксе в нижних отделах грудной клетки обнаруживается горизонтальный уровень жидкости, затемнение гомогенное. При хилоперитонеуме наблюдается высокое стояние и ограничение подвижности диафрагмы.
- УЗИ. Эхокардиография позволяет подтвердить наличие жидкости в перикардиальной полости и примерно определить ее количество. УЗИ плевральной полости предоставляет информацию о наличии и объеме хилоторакса.
- Пункции полостей. Требуются для уточнения характера жидкости. Хилоторакс подтверждают путем плевральной пункции. При хилоперикарде выполняют пункцию сердечной сумки, при хилоперитонеуме проводят лапароцентез.
- Лабораторные исследования. В моче (хилурия) или каловых массах (экссудативная энтеропатия) обнаруживаются следы лимфы.
- Лимфография. Рентгеноконтрастное исследование дает возможность оценить состояние лимфатической системы, выявить блоки, определить уровень повреждения сосуда.
Постановка диагноза наружной лимфореи обычно не представляет затруднений. Лимфоррагию в полости тела необходимо дифференцировать со скоплением других жидкостей. Хилоторакс отличают от гидроторакса, плеврита, гемоторакса. Хилоперитонеум дифференцируют от различных вариантов асцита, хилоперикард – от гемоперикарда и экссудативного перикардита.
Лечение лимфореи
Пациента госпитализируют в стационар по профилю основного заболевания. Тактика лечения определяется локализацией лимфоррагии. Применяются следующие методики:
- Наружная периферическая лимфорея. При незначительном выделении хилезной жидкости накладывают давящую повязку, при недостаточной эффективности данного метода лечения выполняют тампонаду. Прошивание или коагуляция сосуда требуются редко.
- Хилоторакс. Проводят плевральные пункции, при отсутствии результата требуется перевязка грудного протока с использованием торакотомии или торакоскопии.
- Хилоперитонеум. Производят аспирацию лимфы путем лапароцентеза. Неэффективность лечения является показанием к лапаротомическому или лапароскопическому хирургическому вмешательству.
- Хилоперикард. Осуществляют пункции перикарда. При упорном течении необходима торакоскопия или торакотомия для перевязки лимфатического сосуда.
План лечения экссудативной энтеропатии и хилурии определяют с учетом характера и распространенности патологии сосудов. Консервативное лечение всех видов лимфореи предполагает инфузионную терапию с возмещением недостатка жидкости, питательных веществ и микроэлементов. При рецидивирующей лимфорее вследствие блокировки лимфооттока проводят реконструктивные вмешательства.
Прогноз
При незначительных повреждениях и быстрой остановке лимфореи в случае острых состояний прогноз благоприятный. Лимфоррагия, развившаяся на фоне хронических патологий лимфатической системы, труднее поддается лечению, особенно в случае распространенных поражений сосудов. При стойкой массивной лимфорее прогноз серьезный, возможна гибель пациента вследствие истощения и обменных нарушений.
Профилактика
Предупреждение операционных повреждений предусматривает соблюдение техники вмешательств, аспирационное дренирование раны или наложение давящей повязки после удаления регионарных лимфоузлов в ходе онкологических операций. Необходимо своевременное выявление и лечение состояний, которые могут привести к развитию лимфореи.
Источник
Операция по удалению лимфоузлов в паху чаще всего проводится в рамках лечения рака вульвы и рака полового члена. Кроме того, показанием к паховой лимфодиссекции могут быть и другие онкологические заболевания, при которых происходит метастазирование в лимфоузлы данной области.
Зачем нужно удалять лимфоузлы
Подавляющее большинство злокачественных опухолей дает метастазы лимфогенным путем, и это происходит следующим образом. На определенной стадии развития злокачественные клетки начинают терять связь с первичной опухолью. Затем с током тканевой жидкости (лимфы) они попадают в лимфатические капилляры, а оттуда и в ближайшие лимфатические узлы. Узел, который располагается первым на пути опухоли, называется сторожевым.
Часть опухолевых клеток в лимфоузлах погибает, а другая часть преодолевает иммунный барьер и начинает размножаться. Таким образом образуется метастаз. Он постепенно растет, что приводит к увеличению размера лимфоузла. Какое-то время иммунные клетки сдерживают развитие метастаза и не дают ему распространиться дальше. В зависимости от степени злокачественности, этот этап может занять от нескольких месяцев до нескольких лет. Затем раковые клетки мигрируют дальше, в следующие коллекторы лимфы и со временем разносятся по всему организму.
Целью паховой лимфаденэктомии является удаление регионарных лимфатических узлов – тех, которые собирают большую часть лимфы из места, где расположена опухоль, а значит в них наиболее вероятно могут находиться раковые клетки. Это не может полностью предотвратить риск метастазирования опухоли, но снизит вероятность его развития, а также ограничит возможность распространения раковых клеток по лимфатической системе. Кроме того, удаленные лимфоузлы обязательно отправляются на морфологическое исследование, результаты которого позволяют более точно определить стадию опухоли и при необходимости скорректировать лечение.
Зачастую данная операция имеет жизненно важное значение, и выполняется во всех необходимых случаях, когда пациент способен перенести хирургическое вмешательство. Но с другой стороны, она сопряжена с рядом серьезных осложнений, как в послеоперационном, так и в отдаленном периоде, даже через несколько лет после ее проведения. Поэтому в научно-медицинском сообществе постоянно проводятся исследования, направленные на поиск оптимального объема удаления тканей.
Например, онкологи могут прогнозировать, в какие узлы рак пойдет в первую очередь, их называют сигнальными или сторожевыми. При некоторых видах опухолей первым этапом проводят удаление сторожевых лимфоузлов. Их отправляют в лабораторию и исследуют на наличие злокачественных клеток. Если результат оказывается отрицательным, то с высокой долей вероятности другие лимфоузлы также не вовлечены в процесс, и удалять их нет необходимости.
Для того чтобы определить сигнальные лимфоузлы, проводят их картирование. С этой целью в опухоль вводят красящее вещество, или индикатор. Чаще всего это радиоактивный изотоп, который позволяет отследить путь движения лимфы и определить, где находится сторожевой лимфатический узел.
Биопсия сторожевого лимфоузла позволяет избежать удаления подмышечных лимфоузлов у 60-65% пациенток со второй стадией рака груди. Раньше такая операция считалась обязательной, что увеличивало риски развития лимфедемы — слоновости или сильной отечности руки, в тяжелых случаях приводящей к инвалидизации таких пациенток.
Подготовка к удалению лимфоузлов
Поскольку операция проводится в рамках специального лечения, пациенты предварительно проходят полных комплекс диагностических процедур для постановки диагноза и определения стадии процесса. План обследования определяется индивидуально для каждого пациента с учетом специфики опухоли. В ряде случаев достаточно таких рутинных исследований как УЗИ, КТ или МРТ. В других требуется проведение радиоизотопного сканирования или ПЭТ-КТ.
Как проходит операция
Паховая лимфаденэктомия может выполняться во время хирургического удаления первичной опухоли. Чаще всего лимфоузлы в этом случае удаляются единым блоком вместе со злокачественным новообразованием. Другим вариантом является отсроченное вмешательство. Удаление лимфоузлов в этом случае проводится вторым этапом либо после проведения дополнительных методов диагностики (морфологическое исследование краев отсечения, биопсия сторожевого лимфоузла), либо в отдаленном периоде, когда уже происходит прогрессирование патологии.
Сама процедура по удалению паховых лимфоузлов может выполняться двумя методами – открытым, или традиционным, и закрытым – эндоскопическим. При открытой операции производится обширный разрез тканей, после которых остаются протяженные рубцы. При эндоскопическом вмешательстве все манипуляции выполняются через небольшие проколы. Этот метод дает меньшее повреждение тканей, не оставляет после себя больших рубцов, а также реже вызывает такие осложнения как лимфедема, некроз кожных лоскутов, отек мошонки или вульвы и раневую инфекцию.
Сама по себе такая операция технически очень сложная и, как правило, занимает времени больше, чем удаление первичного очага. Разумеется, она требует высокой квалификации хирурга.
На этапе заживления после удаления паховых лимфоузлов необходим постоянный контроль за состоянием раны. Повязки нужно менять согласно рекомендациям врача. Возможно первое время будет необходимо выполнять пункцию области операции, чтобы эвакуировать скопившуюся жидкость. Постепенно необходимость в процедуре пропадет.
Также необходимо следить за тем, чтобы рана не инфицировалась. При появлении покраснения, отечности, припухлости, при усилении болезненности, неприятного запаха или гнойных выделений необходимо срочно обратиться к врачу.
После операции возможно локальное онемение кожи. Оно развивается из-за того, что во время вмешательства пересекаются нервные окончания. У части пациентов чувствительность со временем восстанавливается.
Возможные осложнения
Паховая лимфаденэктомия является неприятной операцией и сопровождается риском развития некоторых осложнений:
- Лимфорея и серомы – скопление лимфы в ране. В среднем это продолжается около 2 недель, но может сохраняться до 1 месяца. Скопление лимфы в ране является фактором риска вторичного инфицирования и некроза кожи. Если серома обширна, она может вызвать бурный рост соединительной ткани и образование келоидных рубцов.
- Отек вульвы или мошонки.
- Отеки ног, вплоть до развития лимфедемы (слоновости конечности). Отеки могут быть локальными, когда страдает, например, только стопа или кисть, или обширными, когда в процесс вовлекается вся конечность и ткани нижней половины туловища. Отеки сопровождаются болью и потерей мышечной силы.
В рамках лечения лимфедемы проводится комплексная терапия, включающая в себя компрессию, дренирующий массаж, комплекс лечебной физкультуры и уход за кожей пораженной конечности.
Для того чтобы предотвратить или минимизировать риски развития данной патологии, необходимо строго придерживаться ряда правил:
- Не допускать образования отеков, даже незначительных, на пораженной конечности. При их образовании необходимо носить компрессионный трикотаж.
- Следует избегать любых манипуляций, которые могут привести к локальному повышению давления на заинтересованной конечности – долго стоять, носить неудобную обувь, в том числе модельную обувь на каблуках.
- Тщательно следить за тем, чтобы кожа на ногах не была повреждена, избегать образования мозолей, травм, мацерации. Не ходить босиком даже дома по полу и др.
- Следует избегать резких температурных колебаний – бани, сауны, бассейны и др.
Прогноз и клиническая эффективность удаления паховых лимфоузлов
Паховая лимфаденэктомия не всегда полностью предотвращает прогрессирование рака или его дальнейшее распространение. Однако она может существенно увеличить продолжительность жизни онкопациентов, а в ряде случаев даже добиться полного их выздоровления.
Источник
В помощь практическому врачу
А.А. Фокин, А.Г. Кузнецов, Л.А. Орехова, А.А. Федин
Кафедра госпитальной хирургии Челябинской Медицинской академии,
Областной центр хирургии сосудов, Челябинск, Россия
За период с марта 1996 г. по декабрь 1999 г. у 751 больного выполнены реконструктивные вмешательства преимущественно по поводу окклюзионных изменений в аорто-подвздошном регионе и артериях нижних конечностей. Во всех случаях производилось одно- или двустороннее рассечение тканей с обнажением сосудов в области бедренного треугольника. Лимфорея из раны в паховой области возникла у 21 больного (2,8%). У 19 из них в этой зоне имелся синтетический сосудистый протез. Частота лимфореи по отношению к общему числу ран составила 2,3%. Истечение лимфы появлялось на 3–6-й послеоперационный день и было значительным. Нагноения ран, полного расхождения их краев и обнажения протеза не было. Однократное бактериологическое исследование лимфы из раны не выявило роста микроорганизмов.
Для лечения применялись от 2 до 7 сеансов рентгенотерапии. Общая доза облучения колебалась от 52 до 448 Грей. В послеоперационном периоде больные получали антибиотики.
У всех пациентов удалось купировать лимфорею и добиться заживления раны. Трансплантат остался проходимым, инфицирования его не произошло. Изменений в анализе крови, обусловленных лучевым воздействием, не наблюдалось. В отдаленном периоде при наблюдении от 3 до 40 мес. у двоих пациентов произошел тромбоз протеза. Хроническая лимфатическая недостаточность нижней конечности на стороне лимфореи не зарегистрирована.
Введение
Лимфорея является одним из специфических ранних осложнений артериальной хирургии. Возникает она преимущественно при операциях, связанных с рассечением тканей и выделением артерий в области бедренного треугольника. Частота лимфореи, по данным различных ангиохирургов, колеблется в пределах 1,5–8,6% [1–4]. Лимфорея в паховой области, осложняющая артериальную реконструкцию, может приводить к нагноению раны, нарушению ее заживления и удлинению времени пребывания больного в стационаре. Не исключается также развитие в дальнейшем лимфатического отека конечности. Опасность лимфореи резко возрастает, если в паховой ране располагается синтетический сосудистый протез. Создается реальная угроза его инфицирования с последующими тяжелыми осложнениями.
Существует довольно много методов лечения лимфореи. Консервативная терапия не всегда эффективна. В связи с этим предложены разнообразные хирургические операции. Они более радикальны, но каждая из них представляет дополнительное, нежелательное вмешательство, которое также не всегда обеспечивает успех. Мы предлагаем для борьбы с лимфореей, развившейся после реконструктивных вмешательств на артериях, рентгенотерапию. На определённой стадии развития осложнения лучевое лечение может оказаться весьма действенным и недорогим средством. В литературе на эту тему имеются только единичные сообщения [5]; обобщающие материалы отсутствуют.
Материал и методы
За период с марта 1996 г. по декабрь 1999 г. у 751 больного выполнены реконструктивные вмешательства по поводу патологических изменений в аорто-подвздошном регионе и артериях нижних конечностей.
За исключением отдельных больных с аневризмой, основным показанием к операции явились окклюзионно-стенотические изменения аорто-артериальной системы. Применялись различные шунтирующие операции и реже – тромбэндартерэктомия. Во всех случаях производилось одно- или двустороннее обнажение сосудов в верхнем отделе бедра и паховой области. Общее число ран в указанной зоне составило 972. Как правило, использовали продольный разрез несколько кнаружи от проекции бедренной артерии. В ходе операции в ране широко использовали электрокоагуляцию и реже – перевязку отдельных участков клетчатки. В конце операции через отдельный прокол, выполняемый книзу и кнаружи от разреза, с помощью пластиковой трубки дренировали рану. После чего её ушивали, начиная с широкой фасции бедра.
Лимфорея из раны в паховой области возникла у 21 больного (2,8%). Возраст этих больных колебался от 43 до 67 лет. У 19 человек производилась реконструкция аорто-илиакального и у двух – бедренно-подколенного региона. У 19 из них в этой зоне использован синтетический сосудистый трансплантат. Следует отметить, что 7 больных в прошлом подвергались операции с обнажением бедренных сосудов. В связи с ранним тромбозом 2 пациента в первый день после вмешательства оперированы повторно. Рана в паховой области в этих случаях, естественно, расшивалась. В наших наблюдениях частота лимфореи по отношению к общему числу ран составила 2,3%, в других сообщениях она оценивается в 2–5% [4,5].
Истечение лимфы появлялось на 3-6-й послеоперационный день. Выделение лимфы было значительным, но точно оценить её количество трудно. Толстую давящую повязку, накладываемую на рану, из-за промокания приходилось менять 2–3 раза в течение суток. Лимфа обычно поступала через небольшой дефект по линии раны, иногда через дренажное отверстие, оставшееся после удаления дренажа. У большей части больных развивалась инфильтрация тканей в области раны. Лимфа представляла собой прозрачную жидкость. Бактериологическое исследование её проводилось однократно и не выявило роста микроорганизмов.
Рентгенотерапию начинали с первого или второго дня с момента появления лимфоистечения. Сеансы её проводили через день. Для лечения использовали рентгенотерапевтический аппарат отечественного производства РУМ-17. В зависимости от результативности число сеансов колебалось от 2 до 7 (в среднем 5) с общей дозой облучения от 52 до 448 Грей. Разовая доза на поверхности кожи составляла 0,5–0,6 Грей, а размер поля – 10×15 см. В послеоперационном периоде, в том числе во время лучевой терапии, больные получали антибиотики. Физическую активность их ограничивали.
Результаты
Края раны в месте истечения лимфы обычно расходились на протяжении 2–3 см, и заживление её на этом участке происходило вторичным натяжением. Рана захватывала кожу и частично подкожную клетчатку. Швы держали до двух недель и снимали их в 2–3 приёма. Рана окончательно заживала спустя 3 недели после операции. В процессе лучевой терапии лимфорея у двух больных осложнилась образованием кисты (лимфоцеле), которая располагалась вблизи верхнего угла раны и представляла собой мягко-эластическое образование с нечёткой флюктуацией диаметром 4 см. После однократной пункции с аспирацией 3 мл прозрачной жидкости желтоватого цвета кисты исчезли. У всех больных удалось купировать лимфоистечение без инфицирования протеза с сохранением его проходимости. Специфических изменений в анализах крови, обусловленных лучевой терапией, не зарегистрировано. В отдаленные сроки (от 3 до 40 мес.) у двоих произошёл тромбоз протеза; позднее инфицирование его отсутствовало. Один больной скончался от инфаркта миокарда. Ни у одного пациента не возникло хронической лимфатической недостаточности нижней конечности на стороне перенесенной лимфореи.
Обсуждение
Как известно, в области бедренного треугольника находится множество поверхностных и глубоких лимфатических сосудов, а также лимфатических узлов. Глубокие лимфатические коллекторы сопровождают артерии и вены и вместе с ними заключены в фасциальные влагалища. Следовательно, имеются анатомические предпосылки для повреждения лимфатической системы при вмешательстве на кровеносных сосудах в паховой области и верхнем отделе бедра. Это подтверждается литературными данными [6,7].
Общепризнанно, что лимфорея при вмешательствах на аорте и артериях наиболее часто возникает после реконструктивных операций, сопровождающихся рассечением тканей и обнажением сосудов в зоне скарповского треугольника. Главная опасность лимфоистечения связана с большой возможностью инфицирования синтетического сосудистого трансплантата, расположенного здесь [3,4,6,8,9]. Бактериальное загрязнение протеза в этих случаях может происходить вследствие воздействия инфицированной лимфы [10]. Однако, по нашему мнению, совсем нередко вытекающая лимфа в первые дни стерильна, а инфицирование ее и протеза наступает вследствие нарушения заживления послеоперационной раны.
При обильном лимфоистечении рекомендуются различные хирургические вмешательства. Следует назвать миопластику с использованием портняжной мышцы, наложение лимфо-венозных или лимфо-лимфатических анастомозов, перевязку лимфатических путей в ране и на протяжении [1–3,7,8].
Перечисленные операции приходится делать вынужденно, и они являются не самым лучшим способом борьбы с лимфореей. Целесообразно использовать более простой и безопасный путь её лечения, которым, по нашему убеждению, в определенных условиях может стать рентгенотерапия. Мы считаем необходимым высказаться кратко в защиту этого лечебного метода. До середины 50-х годов рентгенотерапию широко использовали для лечения многих заболеваний [11]. Затем в силу ряда обстоятельств произошёл необоснованный отказ от неё и была преувеличена её опасность. Накопленный в последствии большой клинический опыт, экспериментальные данные, усовершенствование аппаратуры, новые взгляды на биологическое и терапевтическое действие излучения позволяют вернуться к лучевой терапии. В настоящее время доказана ее высокая эффективность при многих острых и хронических воспалительных процессах. Основным методом принято считать классическую рентгенотерапию [12]. Исходя из указанных сведений, мы решились на применение рентгенотерапии для устранения лимфореи после артериальной реконструкции.
Лучевую терапию лимфореи следует проводить в соответствии с определенными показаниями; только тогда она окажется результативной. При её назначении необходимо соблюдать некоторые условия. Это лечение подходит для больных, у которых лимфоистечение появилось в первые послеоперационные дни и является асептическим. Не должно быть нагноения в ране и расхождения её краёв с обнажением протеза. Следует изначально проводить бактериологическое исследование лимфы для подтверждения её стерильности. Перечисленным требованиям полностью отвечали наши пациенты, и именно поэтому рентгенотерапия у них привела к излечению.
Для обнажения бедренных артерий мы использовали только продольное рассечение тканей. При нём вероятность повреждения лимфатических сосудов меньше, чем при другом направлении разреза [12,13,14]. Опасна чрезмерная травматизация тканей в ране. При отсепаровке лимфатических узлов пересечённые ткани вблизи них лучше всего перевязывать. Оправдано широкое использование электрокоагуляции. Рана должна быть аккуратно послойно ушита. Дренаж в ране, по нашему мнению, необходим, но дренажные трубки нельзя вводить по передне-внутренней поверхности бедра.
Реоперация в паховой области, по мнению ряда авторов, увеличивает вероятность возникновения лимфореи [1,4]. Мы согласны с этим мнением. Из 21 больного с лимфореей, наблюдавшегося нами, двое были оперированы повторно в связи с тромбозом в первый послеоперационный день, а семеро подверглись в прошлом операции с обнажением бедренных сосудов. Применение антибиотиков в случае возникновения лимфореи позволяет снизить опасность инфицирования.
Литература / Refernces
- Tyndall S.H., Shepard A.D., Wilczewski J.V. et al. Groin lymphatic complications after arterial reconstruction. Vasc. Surg. 1994; 19; 5:858–863.
- al-Salman M. M., Rabee H., Shibli S. Groin lymphorrhea postoperative nuisance. Int. Surg. 1997; 82; 1:60–62.
- Абалмасов К.Г., Малинина А.А., Морозов К.М. и др. Повреждение регионарных лимфатических коллекторов в сосудистой хирургии. Грудная и сердечно-сосудистая хирургия. 1997; 2:129.
- Roberts J.R., Walters G.K., Zenilman M.E., Jones С.Е. Groin lymphorrhea complicating revascularization involving the femoral vessels. Amer. J. Surg. 1993; 165; 3:341–344.
- Groft R. J. Lymphatic fistula: a complication of arterial surgery (letter). Br. med. J. 1978; 15; 2(6131):205.
- Skudder P.A., Geary J. Lymphatic drainage from the groin following surgery of the femoral artery. J. Cardiovasc. Surg. (Torino). 1987; 28: 4:460–463.
- Rubin J.R., Malone J.N., Goldstone J. The role of the lymphatic system in acute arterial prosthetic graft infections. J. Vasс. Surg. 1985; 2; 1:92–98.
- Sandmann W., Kremer K., Kleinschmitd F., Gunter D. LymphabfluBstorungen nach Arterienoperationen am Bein. Chirurg. 1976; 47; 4:198–204.
- Kwaan J.H., Bernstein J.M., Connolly J. Management of lymph fistula in the groin after arterial reconstruction. Arch. Surg. 1979; 114: 12:1416–1418.
- Haaverstad R., Umcs О., Dahl Т., Myhre H.D. Lymfekomplikajoner etter karkirurgi pa underekstremitetene. Bratisl. Lek. Listy. 1995; 96: 8:447–449.
- Soots G., Mikati A., Warenbourg Jr. et al. Treatment of lymphorrhea with exposed or infected vascular prosthetic grafts in the groin using sartorius myoplasty. J. Cardiovasc. Surg. 1988; 29: 1:42–45.
- Кишковский А.Н., Дударев А.Л. Лучевая терапия неопухолевых заболеваний. М.: Медицина. 1977; 175.
- Переслегин И.А., Переслегин О.И. В защиту лучевой терапии неопухолевых заболеваний. Вестник рентгенологии и радиологии. 1994; 5:48–52.
- Chester J.F., Butler С.М., Taylor R. S. Vascular reconstruction at the groin: oblique or vertical incisions. Ann. R. Coll. Surg. Engl. 1992; 74: 2:112–114.
Источник