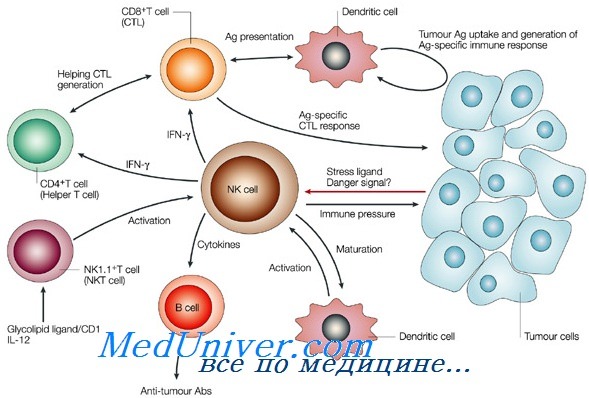
Лимфопоэз nk лимфоцитов происходит
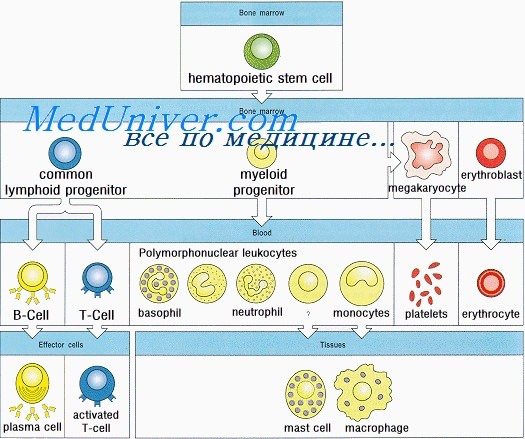
Гематология: Лимфопоэз
Предшественники, коммитированные к В- и Т-клеточному пути развития, являются прямыми потомками плюрипотентной стволовой клетки (CD34+).
Лимфопоэз у эмбриона и плода происходит транзиторно в различных эмбриональных тканях. Лимфоидные предшественники присутствуют уже в желточном мешке. К 5-6-й неделе гестации предшественники В- и Т-клеток появляются в печени, где формируются участки В-лимфопоэза. Формирование большинства Т-клеток происходит в вилочковой железе.
На 7-й-8-й неделе эмбрионального развития формируется вилочковая железа, которая заселяется принесенными с кровью предшественниками. С третьего триместра беременности до рождения очагом гемопоэза и В-лимфопоэза является селезенка.
После рождения основным местом развития миелоидных клеток и В-лимфоцитов становится костный мозг. Т-лимфоциты развиваются в вилочковой железе, куда перемещаются костномозговые предшественники, и происходит процесс, называемый Т-лимфопоэзом. Селезенка у взрослых функционирует как вторичный лимфоидный орган, в котором располагаются зрелые Т- и В-клетки.
Развитие В-лимфоцитов при лимфопоэзе
Развитие лимфоцита у взрослого проходит две различные фазы. Первая фаза — антигеннезависимая, когда В-лимфоциты развиваются до стадии, в которой они экспрессируют на поверхности иммуноглобулин IgM, — происходит в костном мозге. Вторая фаза — антигензависимая, протекает во вторичных лимфоидных органах (селезенка и лимфатические узлы) в ответ на клеточные и гуморальные сигналы, поступающие от Т-клеток, макрофагов и других популяций акцессорных клеток.
При использовании специфических моноклональных антител, которые распознают иммуноглобулины и другие поверхностные и цитоплазматические детерминанты, можно различать промежуточные степени развития В-клеток.
Клетки-предшественники, коммитированные к дифференцировке в В-лимфоциты, имеют иммуноглобулиновые гены в зародышевой конфигурации и называются про-В-клетки. Затем в цитоплазме появляется белок тяжелой цепи иммуноглобулина М (ц), и с этого момента клетка обозначается как пре-В-клетка. Как только в клетке происходит экспрессия белков легкой цепи, начинается сборка молекул иммуноглобулинов, и после их появления на поверхности клетки определяются как В-лимфоциты.

Популяции В-клеток при лимфопоэзе
Предполагается, что существуют три различные линии В-клеток, определяемые по фенотипическим и функциональным свойствам: Bla, B1b и В2. Bla-клетки экспрессируют CD5; Bib-клетки не экспрессируют CD5, характеризуются высокими уровнями поверхностного IgM и низкими уровнями мембранного IgD. Распространение этих популяций у взрослых в основном ограничено перитонеальной и плевральной полостями.
Этим они отличаются от стандартных (или В2) В-клеток, которые преобладают во вторичных лимфоидных органах, таких как лимфоузлы и селезенка.
Характерной особенностью Bl-клеток является их способность продуцировать аутоантитела класса IgM (среди которых наиболее частыми являются антитела к ДНК и ревматоидный фактор). Это делает понимание природы данных клеток клинически важным вопросом. Популяция Bl-клеток является, вероятно, основным источником естественных ауто-антител, представленных в сыворотке крови здоровых лиц.
Естественные аутоантитела встречаются в крови взрослых, детей, новорожденных и даже у плода. Они присутствуют в малых количествах, почти всегда связываются со многими антигенами (мультиреактивные аутоантитела) и имеют низкую аффинность к их лигандам. Пока неизвестно, продуцируются ли естественные аутоантитела только Bl-клетками или их способны производить также девственные В2-клетки.
– Также рекомендуем “CD-антигены лейкоцитов – дифференцировочные кластеры — CD”
Оглавление темы “История гематологии”:
- История гематологии: становление, этап развития с 16-го по 19-й век
- История развития теорий кроветворения – второй этап развития гематологии с 19-го по 20-й век
- История клинической гематологии – учения о лейкемиях, лейкозах, лимфомах
- История изучения анемий – второй этап развития гематологии с 19-го по 20-й век
- Третий этап развития гематологии – изучение биологических полимеров (ДНК, белков) клеток крови
- История иммуногематологии – третий этап развития гематологии 20-го по 21-й века
- Отечественные гематологические школы 20-го века. История российской гематологии
- Нормальные показатели крови. Интенсивность обновления крови
- Гематология: стволовые кроветворные клетки (СКК) – свойства, функции, типы
- Гематология: Лимфопоэз
Источник
Формирование иммунитета у плода. Неонатальный лимфопоэзЗащиту организма от инфекционных агентов обеспечивают физические барьеры (кожа, слизистые оболочки и реснитчатый эпителий) и различные компоненты иммунной системы. Последняя состоит из Т- и В-лимфоцитов, NK-клеток, дендритных и фагоцитирующих клеток, а также белков комплемента. Иммунная система защищает организм также от аутоиммунных заболеваний и развития злокачественных опухолей. Иммунная система человека развивается из ткани первичной кишки. Полипотентные кроветворные стволовые клетки впервые появляются в желточном мешке на 2,5-3-й неделе внутриутробного развития и на 5-й неделе мигрируют в печень плода. Позднее они попадают в костный мозг, где и остаются на протяжении всей жизни. Из этих клеток образуются лимфоидные стволовые клетки, которые в зависимости от локализации дифференцируются в Т-, В- и NK-клетки. В середине I триместра беременности у плода образуются первичные лимфоидные органы (тимус и костный мозг), а вскоре и вторичные — селезенка, лимфатические узлы, миндалины, пейеровы бляшки и lamina propria. В этих органах дифференцировка Т-, В- и NK-лимфоцитов из стволовых клеток продолжается в течение всей жизни. Как для органогенеза, так и для клеточной дифференцировки необходимо взаимодействие поверхностных молекул лимфоидных клеток с их микроокружением. Многочисленность и разнообразие этих поверхностных молекул отражена в международной классификации дифференцировочных антигенов, которые носят название кластеров дифференцировки (CD). Т- и В-лимфоциты — единственные компоненты иммунной системы, способные распознавать специфические антигены; именно из них образуются клетки памяти (адаптивный иммунитет). Из кроветворных стволовых клеток образуются и NK-клетки, которые также являются лимфоцитами. Они защищают организм от вирусных инфекций, уничтожают опухолевые клетки и участвуют в регуляции иммунных реакций. Белки, синтезируемые и секретируемые Т- и В-лимфоцитами и NK-клетками, а также взаимодействующими с ними клетками, называются цитокинами. Некоторые из этих белков получили название интерлейкинов (ИЛ). На 4-й неделе внутриутробной жизни из эктодермы третьей жаберной дуги и эндодермы третьего глоточного кармана образуется первичная закладка тимуса. На 7-8-й неделе правая и левая его части перемещаются каудально и сливаются друг с другом. На 8-й неделе предшественники Т-лимфоцитов из печени плода через кровь начинают поступать в окружающую тимус мезенхиму. Эти про-Т-лимфоциты идентифицируют по поверхностным белкам CD7 и CD34. К 8-8,5 нед. гестации СD7-клетки обнаруживаются уже в самом тимусе, причем на некоторых из них экспрессируются также CD4 и CD8.
Первый из этих маркеров характерен для зрелых Т-лимфоцитов-хелперов (Th), a CD8 — для зрелых цитотоксических Т-лимфоцитов и NK-клеток. Кроме того, на некоторых клетках присутствуют одиночные цепи антигенраспознающих рецепторов Т-лимфоцитов (TCR, Ti), но не полные TCR. Зрелые TCR представляют собой гетеродимеры, состоящие из двух цепей — либо а и b, либо у и 8. TCR экспрессируются на клеточной поверхности вместе с CD3, образуя комплекс из пяти полипептидных цепей). Рекомбинация гена TCR осуществляется путем слияния крупных отдаленных друг от друга сегментов ДНК. Эти сегменты называются V (вариабельным), D (дополнительным) и J (соединяющим), причем каждый из них имеет ряд вариантов. Сегменты VDJ присоединяются к константной области а-гена, а сегменты VJ — к р-гену, завершая строение генов, кодирующих TCR. Случайная комбинация сегментов и определяет, в основном, огромное разнообразие TCR, придавая им способность распознавать миллионы различных антигенов. Рекомбинация генов TCR регулируется ферментами RAG-1 и RAG-2 (рекомбиназы, активирующие гены), а также другими ферментами. При тяжелом комбинированном иммунодефиците у мышей и некоторых людей процесс рекомбинации нарушен. Рекомбинация генов TCR знаменует собой превращение про-Т-лимфоцитов в пре-Т-лимфоциты. Этот процесс начинается вскоре после заселения тимуса стволовыми клетками. На 8-10-й неделе внутриутробной жизни начинают формироваться Т-лимфоциты с разной функцией. На 9,5-10-й неделе более 95% тимоцитов экспрессирует CD7, CD2, CD4, CD8 и цитоплазматический CD3, а примерно 30% — внутренний антиген клеток коркового вещества тимуса. К 10-й неделе 25% тимоцитов обладают TCRaP. Число таких тимоцитов в ходе эмбрионального развития постепенно увеличивается и после рождения превышает 95 %. По мере экспрессии TCR начинаются процессы позитивной и негативной селекции клеток коркового вещества тимуса. Позитивная селекция происходит путем взаимодействия незрелых тимоцитов (слабо экспрессирующих TCR) с МНС на эпителиальных клетках тимуса. В результате активируются и созревают только те тимоциты, рецепторы которых способны взаимодействовать с чужеродными антигенами, представляемыми им антигенами МНС. Зрелые тимоциты, прошедшие процесс селекции, экспрессируют либо CD4, либо CD8. Первые способны взаимодействовать с чужеродными антигенами, представляемыми молекулами HLA класса II, а вторые — с антигенами, представляемыми классом I HLA. Затем начинается негативная селекция, обусловленная взаимодействием выживших тимоцитов, экспрессирующих значительно большее количество TCR, с пептидами хозяина, представляемыми HLA классов I и II, которые присутствуют на поступивших из костного мозга макрофагах, дендритных клетках и, возможно, В-лимфоцитах. Взаимодействие с этими антигенами включает программу апоптоза (запрограммированной гибели) аутореактивных тимоцитов. Клетки коркового вещества тимуса плода относятся к числу наиболее быстро делящихся клеток организма; их количество за 2 нед. после заселения тимуса стволовыми клетками возрастает в 100 000 раз. По мере их созревания происходят процессы селекции, в результате которых 97 % этих клеток погибает. Выжившие клетки несут на своей поверхности либо только CD4, либо только CD8, но не оба этих антигена и мигрируют в мозговое вещество тимуса. Одновременно с появлением тимоцитов, обладающих только одним дифференцировочным антигеном, развиваются и функции Т-лимфоцитов, но до их выхода из тимуса эти клетки остаются незрелыми. Одна стволовая клетки дает начало примерно 3000 зрелых клеток мозгового вещества тимуса. Они устойчивы к лизирующему эффекту кортикостероидов. На 11—12-й неделе внутриутробной жизни Т-лимфоциты начинают покидать тимус, заселяя селезенку, лимфатические узлы и аппендикс, а на 14-15-й неделе — и миндалины. Наибольшее их количество скапливается в корковом веществе лимфатических узлов, вокруг артериол селезенки и в лимфе грудного лимфатического протока. Клетки, недавно покинувшие тимус, одновременно экспрессируют изоформы CD45RA и CD62L (L-селектин). Рекомбинация генов TCR в ходе этого процесса приводит к образованию в качестве побочного продукта круговых эписом, которые обнаруживаются в Т-лимфоцитах, недавно покинувших тимус. В Т-лимфоцитах, созревающих вне тимуса, эписомы отсутствуют. Молекула адгезии, L-селектин, взаимодействует с углеводными компонентами специфических участков кровеносных сосудов. Такие участки (венулы с высоким эпителием) присутствуют в периферических лимфоидных органах, что и определяет задержку лимфоцитов в них. К 12-й неделе внутриутробной жизни Т-лимфоциты приобретают способность к пролиферации под действием растительных лектинов, таких как ФГА и КонА, и аллогенных клеток; антигенсвязывающие Т-лимфоциты появляются на 20-й неделе. – Также рекомендуем “Созревание и дифференцировка В-лимфоцитов у плода. Синтез иммуноглобулинов в утробе матери” Оглавление темы “Иммунитет плода”:
|
Источник
Формирование NK-клеток иммунитета плода. Функции Т-лимфоцитов иммунитетаАктивные NK-клетки обнаруживаются в печени плода на 8-11-й неделе беременности. Их созревание происходит в костном мозге и не требует дифференцировки в тимусе, хотя они и присутствуют в этом органе. От цитотоксических Т-лимфоцитов их отличает способность лизировать клетки-мишени без участия молекул HLA (неклассическая цитотоксичность). NK-клетки имеют также на своей поверхности рецепторы, ингибирующие их киллерную активность. Эти рецепторы узнают определенные HLA и тормозят гибель нормальных аллогенных клеток по четырем специфическим механизмам. Генетический локус, контролирующий эти механизмы, отличается от обычных аллоантигенных локусов HLA, хотя и локализуется на той же хромосоме 6. В отличие от Т- и В-лимфоцитов, в процессе созревания NK-клеток гены их рецепторов не перестраиваются. Практически все NK-клетки экспрессируют CD56, более 90% несут на поверхности CD16 (FcyRIII). К другим поверхностным молекулам NK-клеток относятся CD57 (50-60% клеток), CD7 и CD2 (70-90%), а также CD8 (30-40%). Хотя NK-клетки частично разделяют общие поверхностные антигены с Т-лимфоцитами и клетками миелоидного ростка, взаимосвязь между этими клетками в процессе созревания остается неясной. У больных с тяжелым комбинированным иммунодефицитом и резко сниженным уровнем Т- и В-лимфоцитов может быть избыток NK-клеток, а у некоторых больных, у которых полностью отсутствую NK-клетки, созревание Т- и В-лимфоцитов может протекать нормально. Поступающие из костного мозга в кровь NK-клетки попадают в селезенку; в лимфатических узлах их очень мало. В норме на их долю приходится 10% лимфоцитов крови. В крови пуповины их процент несколько ниже. Взаимодействие иммунокомпетентных клеток играет ключевую роль на всех этапах иммунного ответа. В отличие от рецепторов В-лимфоцитов (иммуноглобулинов), распознающих нативные антигены, TCR способны распознавать только переработанные антигенные пептиды, представляемые им молекулами HLA класса I, такими как HLA-A, -В и -С, и класса II (HLA-DR, -DP и DQ), присутствующими на антигенпредставляющих клетках (АПК). В белковых молекулах HLA имеются углубления, по форме соответствующие переработанным пептидам.
Молекулы HLA класса I экспрессируются большинством ядерных клеток организма, а молекулы HLA класса II — макрофагами, дендритными клетками и В-лимфоцитами. В углубления молекул HLA класса I попадают пептиды, образующиеся при деградации внутриклеточных белков, а также вирусные пептиды, если клетка поражена вирусом. В углублениях молекул HLA класса II располагаются пептиды из экзогенных антигенов, таких как белки вакцин и бактерий. АПК (макрофаги, дендритные клетки и В-лимфоциты) захватывают эти белки, разрушают их и выставляют на клеточной поверхности в углублениях молекул HLA класса II. Т-лимфоциты обладают двумя основными функциями: 1) вьщеляемые ими цитокины, а также находящиеся на их мембране молекулы, взаимодействуя с поверхностными молекулами В-лимфоцитов, индуцируют продукцию антител В-лимфоцитами; 2) Т-лимфоциты уничтожают зараженные вирусом или опухолевые клетки. Выполнение этих функций требует связывания Т-лимфоцитов с АПК или клетками-мишенями. В таком высокоаффинном связывании участвуют не только TCR но и другие поверхностные молекулы Т-лимфоцитов. Так, CD4 Th-клеток прямо связывается с молекулами HLA класса I на АПК a CD8 цитотоксических Т-лимфоцитов — на клетках-мишенях. Белки CD4 и CD8 непосредственно участвуют в активации Т-лимфоцитов, так как сопряжены с внутриклеточной тирозинкиназой p56-lck. Проведение сигнала в Т-лимфоцит регулируется тирозинфосфатазной активностью цитоплазматического домена CD45, поскольку p56-lck служит субстратом для этого фермента. Усиление или ослабление активности Т-лимфоцитов зависит от изоформы CD45 на их поверхности (CD45RO на Т-клетках памяти, CD45RA на девственных Т-лимфоцитах). Мембранная молекула Т-лимфоцитов LFA-1 связывается с молекулой ICAM-1, теперь обозначаемой как CD54, а CD2 — с LFA-3 (CD58) на поверхности АПК. После адгезии с АПК Th-клетки начинают продуцировать интерлейкины и усиливается экспрессия их поверхностных молекул, таких как лиганд CD40 (CD 154). Эти процессы приводят к стимуляции В-лимфоцитов и цитотоксических Т-лимфоцитов. – Также рекомендуем “Механизмы первичного иммунного ответа у плода” Оглавление темы “Иммунитет плода”:
|
Источник