Лимфоциты созревание которых происходит в вилочковой железе называются
Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 4 апреля 2020; проверки требуют 12 правок.
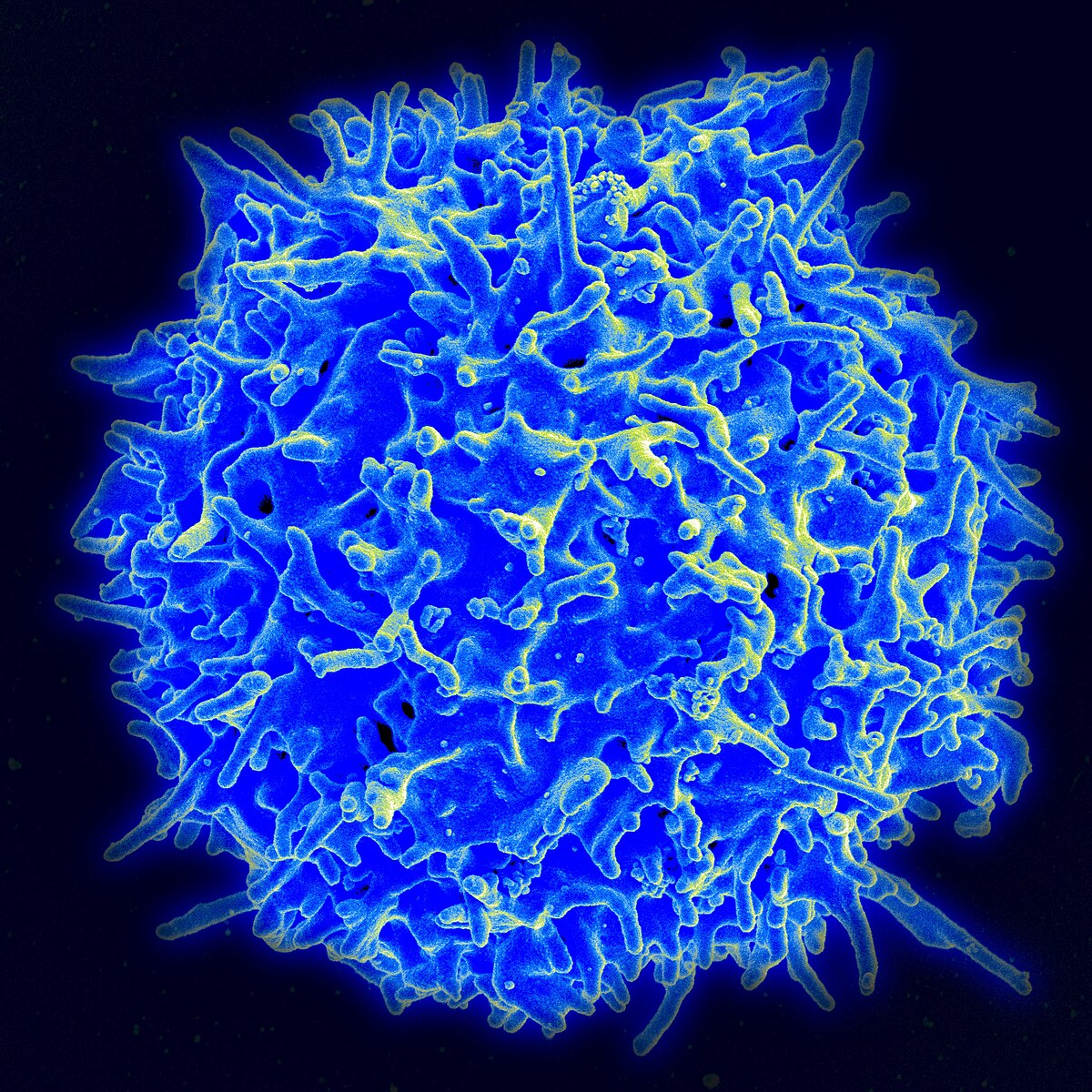
T-лимфоциты, или Т-клетки (от лат. thymus «тимус») — лимфоциты, развивающиеся у млекопитающих в тимусе из предшественников — претимоцитов, поступающих в него из красного костного мозга. В тимусе T-лимфоциты дифференцируются, приобретая Т-клеточные рецепторы (ТКР, англ. TCR) и различные корецепторы (поверхностные маркеры)[1]. Играют важную роль в приобретённом иммунном ответе. Обеспечивают распознавание и уничтожение клеток, несущих чужеродные антигены, усиливают действие моноцитов, NK-клеток, а также принимают участие в переключении изотипов иммуноглобулинов (в начале иммунного ответа B-клетки синтезируют IgM, позже переключаются на продукцию IgG, IgE, IgA).
Типы Т-лимфоцитов[править | править код]
Т-клеточные рецепторы являются основными поверхностными белковыми комплексами Т-лимфоцитов, ответственными за распознавание процессированных антигенов, связанных с молекулами главного комплекса гистосовместимости (ГКГ, англ. major histocompatibility complex (MHC)) на поверхности антигенпредставляющих клеток[2]. Т-клеточный рецептор связан с другим полипептидным мембранным комплексом, CD3. В функции комплекса CD3 входит передача сигналов в клетку, а также стабилизация Т-клеточного рецептора на поверхности мембраны. Т-клеточный рецептор может ассоциироваться с другими поверхностными белками, его корецепторами. В зависимости от корецептора и выполняемых функций различают два основных типа Т-клеток.
Т-хелперы[править | править код]
Антигенраспознающий рецепторный комплекс Т-хелперов
Т-хелперы (от англ. helper — помощник) — Т-лимфоциты, главной функцией которых является усиление адаптивного иммунного ответа. Активируют Т–киллеры, B-лимфоциты, моноциты, NK–клетки при прямом контакте, а также гуморально, выделяя цитокины. Основным признаком Т–хелперов служит наличие на поверхности клетки молекулы корецептора CD4. Т-хелперы распознают антигены при взаимодействии их Т-клеточного рецептора с антигеном, связанным с молекулами главного комплекса гистосовместимости II класса (англ. major histocompatibility complex II (MHC-II)).
Т-киллеры[править | править код]
Т-киллеры (от англ. killer «убийца»), цитотоксические T-лимфоциты, CTL — Т-лимфоциты, главной функцией которых является уничтожение повреждённых клеток собственного организма. Мишени Т-киллеров — это клетки, поражённые внутриклеточными паразитами (к которым относятся вирусы и некоторые виды бактерий), опухолевые клетки. Т-киллеры являются главным компонентом антивирусного иммунитета. Основным признаком Т-киллеров служит наличие на поверхности клетки молекулы корецептора CD8. Т-киллеры распознают антигены при взаимодействии их Т-клеточного рецептора с антигеном, связанным с молекулами главного комплекса гистосовместимости I класса (англ. major histocompatibility complex I (MHC-I)).
Т-хелперы и Т-киллеры образуют группу эффекторных Т-лимфоцитов, непосредственно ответственных за иммунный ответ. В то же время существует другая группа клеток, регуляторные Т-лимфоциты, функция которых заключается в регулировании активности эффекторных Т-лимфоцитов. Модулируя силу и продолжительность иммунного ответа через регуляцию активности Т-эффекторных клеток, регуляторные Т-клетки поддерживают толерантность к собственным антигенам организма и предотвращают развитие аутоиммунных заболеваний. Существуют несколько механизмов супрессии: прямой, при непосредственном контакте между клетками, и дистантный, осуществляющийся на расстоянии — например, через растворимые цитокины.
γδ Т-лимфоциты[править | править код]
Т-лимфоциты представляют собой небольшую популяцию клеток с видоизменённым Т-клеточным рецептором[3]. В отличие от большинства других Т-клеток, рецептор которых образован и субъединицами, Т-клеточный рецептор -лимфоцитов образован и субъединицами. Данные субъединицы не взаимодействуют с пептидными антигенами, презентированными белками ГКГ. Предполагается, что Т-лимфоциты участвуют в узнавании липидных антигенов.
Т-супрессоры[править | править код]
Т-лимфоциты, обеспечивающие центральную регуляцию иммунного ответа.
Дифференциация в тимусе[править | править код]
Стадии дифференциации Т-лимфоцитов
Все Т-клетки берут своё начало от гемопоэтических стволовых клеток красного костного мозга, которые мигрируют в тимус и дифференциируются в незрелые тимоциты[4]. Тимус создаёт микросреду, необходимую для развития полностью функционального репертуара Т-клеток, который является ГКГ-ограниченным и толерантным к самому себе.
Дифференциация тимоцитов разделяется на разные стадии в зависимости от экспрессии различных поверхностных маркеров (антигенов). На самой ранней стадии тимоциты не экспрессируют корецепторы CD4 и CD8 и поэтому классифицируются как двойные негативные (англ. double negative (DN)) (CD4-CD8-). На следующей стадии тимоциты экспрессируют оба корецептора и называются двойными позитивными (англ. double positive (DP)) (СD4+CD8+). Наконец на финальной стадии происходит селекция клеток, которые экспрессируют только один из корецепторов (англ. single positive (SP)): или (CD4+), или (CD8+).
Раннюю стадию можно разделить на несколько подстадий. Так, на подстадии DN1 (англ. double negative 1) тимоциты имеют следующую комбинацию маркеров: CD44+CD25-CD117+. Клетки с данной комбинацией маркеров ещё называют ранними лимфоидными предшественниками (англ. early lymphoid progenitors (ELP)). Прогрессируя в своей дифференциации, ELP активно делятся и окончательно теряют способность трансформироваться в другие типы клеток (например, В-лимфоциты или миелоидные клетки). Переходя на подстадию DN2 (англ. double negative 2), тимоциты экспрессируют CD44+CD25+CD117+ и становятся ранними Т-клеточными предшественниками (англ. early T-cell progenitors (ETP)). В течение DN3 подстадии (англ. double negative 3) ETP клетки имеют комбинацию CD44-CD25+ и вступают в процесс β-селекции.
β-селекция[править | править код]
Гены Т-клеточного рецептора состоят из повторяющихся сегментов, принадлежащих к трём классам: V (англ. variable), D (англ. diversity) и J (англ. joining). В процессе соматической рекомбинации генные сегменты, по одному из каждого класса, соединяются вместе (V(D)J-рекомбинация). Случайное объединение последовательностей сегментов V(D)J приводит к появлению уникальных последовательностей вариабельных доменов каждой из цепей рецептора. Случайный характер образования последовательностей вариабельных доменов позволяет генерировать Т-клетки, способные распознавать большое количество различных антигенов, и, как следствие, обеспечивать более эффективную защиту против быстро эволюционирующих патогенов. Однако этот же механизм зачастую приводит к образованию нефункциональных субъединиц Т-клеточного рецептора. Гены, кодирующие β-субъединицу рецептора, первыми подвергаются рекомбинации в DN3-клетках. Чтобы исключить возможность образования нефункционального пептида, β-субъединица образует комплекс с инвариабельной α-субъединицей пре-T-клеточного рецептора, формируя т. н. пре-T-клеточный рецептор (пре-ТКР)[5]. Клетки, неспособные образовывать функциональный пре-ТКР, погибают в результате апоптоза. Тимоциты, успешно прошедшие β-селекцию, переходят на подстадию DN4 (CD44-CD25-) и подвергаются процессу позитивной селекции.
Позитивная селекция[править | править код]
Клетки, экспрессирующие на своей поверхности пре-ТКР, все ещё не являются иммунокомпетентными, так как не способны связываться с молекулами главного комплекса гистосовместимости. Для узнавания молекул ГКГ T-клеточным рецептором необходимо наличие корецепторов CD4 и CD8 на поверхности тимоцитов. Образование комплекса между пре-ТКР и корецептором CD3 приводит к ингибированию перестроек генов β-субъединицы и в то же время вызывает активацию экспрессии генов CD4 и CD8. Таким образом тимоциты становятся двойными позитивными (DP) (CD4+CD8+). DP-тимоциты активно мигрируют в корковое вещество тимуса, где происходит их взаимодействие с клетками кортикального эпителия, экспрессирующими белки обоих классов ГКГ (MHC-I и MHC-II). Клетки, неспособные взаимодействовать с белками ГКГ кортикального эпителия, подвергаются апоптозу, в то время как клетки, успешно осуществившие такое взаимодействие, начинают активно делиться.
Негативная селекция[править | править код]
Тимоциты, прошедшие позитивную селекцию, начинают мигрировать к кортикомедуллярной границе тимуса. Попадая в медуллу, тимоциты взаимодействуют с собственными антигенами организма, презентированными в комплексе с белками ГКГ на медуллярных тимических эпителиальных клетках (мТЭК). Тимоциты, активно взаимодействующие с собственными антигенами, подвергаются апоптозу. Негативная селекция предотвращает появление самоактивирующихся Т-клеток, способных вызывать аутоиммунные заболевания, являясь важным элементом иммунологической толерантности организма.
Активация[править | править код]
Механизм действия Т-хелперов и Т-киллеров
Т-лимфоциты, успешно прошедшие позитивную и негативную селекцию в тимусе, попавшие на периферию организма, но не имевшие контакта с антигеном, называются наивными Т-клетками (англ. Naive T cells). Основной функцией наивных Т-клеток является реакция на патогены, прежде не известные иммунной системе организма. После того как наивные Т-клетки распознают антиген, они становятся активированными. Активированные клетки начинают активно делиться, образуя клон. Некоторые из клеток этого клона превращаются в эффекторные Т-клетки, которые выполняют функции, специфичные для данного типа лимфоцита (например, выделяют цитокины в случае Т-хелперов или же лизируют поражённые клетки в случае Т-киллеров). Другая часть активированных клеток трансформируется в Т-клетки памяти. Клетки памяти сохраняются в неактивной форме после первичного контакта с антигеном до тех пор, пока не наступает повторное взаимодействие с тем же антигеном. Таким образом, Т-клетки памяти хранят информацию о ранее действовавших антигенах и обеспечивают вторичный иммунный ответ, осуществляющийся в более короткие сроки, чем первичный.
Взаимодействие Т-клеточного рецептора и корецепторов (CD4, CD8) с главным комплексом гистосовместимости важно для успешной активации наивных Т-клеток, однако его самого по себе недостаточно для дифференциации в эффекторные клетки. Для последующей пролиферации активированных клеток необходимо взаимодействие т. н. костимулирующих молекул. Для Т-хелперов такими молекулами являются рецептор CD28 на поверхности Т-клетки и иммуноглобулин B7 на поверхности антигенпрезентирующей клетки.
Примечания[править | править код]
- ↑ Murphy K., Travers P., Walport M. Janeway’s Immunobiology. — New York: Garland Science, 2011. — 888 p. — ISBN 0-8153-4123-7. Архивная копия от 20 октября 2014 на Wayback Machine
- ↑ Alberts B., Johnson A., Lewis J., Raff M., Roberts K., Walter P. Molecular Biology of the Cell. — New York: Garland Science, 2002. — 1367 p. — ISBN 0-8153-3218-1.
- ↑ Holtmeier W., Kabelitz D. Gammadelta T cells link innate and adaptive immune responses // Chemical immunology and allergy. — 2005. — Т. 86. — С. 151–83. — ISBN 978-3-8055-7862-2. — doi:10.1159/000086659. — PMID 15976493.
- ↑ Schwarz B. A., Bhandoola A. Trafficking from the bone marrow to the thymus: a prerequisite for thymopoiesis (англ.) // Immunol. Rev.. — 2006. — Vol. 209. — P. 47–57. — doi:10.1111/j.0105-2896.2006.00350.x. — PMID 16448533.
- ↑ Sleckman B. P. Lymphocyte antigen receptor gene assembly: multiple layers of regulation (англ.) // Immunol Res. — 2005. — Vol. 32. — P. 153-8. Архивировано 27 января 2008 года.
Источник
Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 29 ноября 2020; проверки требуют 4 правки.
У этого термина существуют и другие значения, см. Зоб.
Ти́мус (лат. thymus, ви́лочковая железа, зо́бная железа[2][3]) — лимфоэпителиальный орган лимфопоэза человека и многих видов животных, в котором происходит созревание, дифференцировка и иммунологическое «обучение» T-клеток иммунной системы.
У человека редуцирован, развит у птиц, название происходит от кости — вилочка.
Строение[править | править код]
Анатомия[править | править код]
Тимус в центре. Изображение 1906 г.
Вилочковая железа — небольшой орган розовато-серого цвета, мягкой консистенции, поверхность её дольчатая. У новорождённых его размеры составляют в среднем 5 см в длину, 4 см в ширину и 6 мм в толщину, масса — около 15 граммов. Рост органа продолжается до начала полового созревания (в это время его размеры максимальны — до 7,5—16 см в длину, а масса достигает 20—37 граммов). С возрастом тимус подвергается атрофии и в старческом возрасте едва отличим от окружающей его жировой ткани средостения; в 75 лет средняя масса тимуса составляет всего 6 граммов. По мере инволюции он утрачивает белый цвет и за счёт увеличения в нём доли стромы и жировых клеток становится более жёлтым[4].
У представителей женского пола, размеры железы больше, что связано с разным воздействием на неё половых гормонов[5].
Топография
Тимус расположен в верхней части грудной клетки, сразу за грудиной (верхнее средостение). Спереди к нему прилежит рукоятка и тело грудины до уровня IV реберного хряща; сзади — верхняя часть перикарда, покрывающего начальные отделы аорты и лёгочного ствола, дуга аорты, левая плечеголовная вена; с боков — медиастинальная плевра.
Отдельные группы долек тимуса встречаются вокруг или в толще ткани щитовидной железы, в мягких тканях шеи, в области миндалин, в жировой клетчатке переднего, реже заднего средостения. Частота выявления аберрантного тимуса достигает 25 %. Такие аномалии чаще наблюдаются у женщин, в основном с левой стороны шеи и средостения. В литературе имеются единичные сообщения об эктопии ткани тимуса у детей грудного возраста. Такая патология сопровождалась у них одышкой, дисфагией, дыхательной недостаточностью. По данным P. Nowak и соавт., из 91 случая эктопии вилочковой железы в 76 определяется шейная локализация, преимущественно у лиц мужского пола и слева. Отмечается также связь эктопии тимуса со врождёнными пороками сердца в 71 % случаев[6].
передняя поверхность
задняя поверхность
Внешний вид на фото тимуса человека
Внешний вид
У человека тимус состоит из двух долей, которые могут быть сращены или же просто плотно прилегать друг к другу. Нижняя часть каждой доли широкая, а верхняя узкая; таким образом, верхний полюс может напоминать двузубую вилочку (отсюда и название).
Орган покрыт капсулой из плотной соединительной ткани, от которой в глубину отходят перемычки, делящие его на дольки.
У животных (зобная железа) развита у плодов и молодых животных[7]. Она состоит из непарного грудного отдела, лежащего впереди сердца, и парного шейного отдела, проходящего в виде выростов по бокам трахеи. С возрастом железа начинает рассасываться, а затем исчезает.
Кровоснабжение, лимфоотток и иннервация
Кровоснабжение тимуса происходит из тимических, или тимусных ветвей внутренней грудной артерии, (rami thymici arteriae thoracicae internae), тимических ветвей дуги аорты и плечеголовного ствола и ветвей верхней и нижней щитовидных артерий. Венозный отток осуществляется по ветвям внутренних грудных и плечеголовных вен.
Лимфа от органа оттекает в трахеобронхиальные и парастернальные лимфатические узлы.
Иннервирована вилочковая железа ветвями правого и левого блуждающих нервов, спинномозговыми нервами C4-C7, а также симпатическими нервами, происходящими из верхнего грудного и звездчатого узлов симпатического ствола, находящимися в составе нервных сплетений, которые окружают питающие орган сосуды[8][9][10]. Капсула тимуса иннервируется ветвями диафрагмальных нервов[en][11].
Гистология[править | править код]
Микроскопическое строение вилочковой железы
Окрашенный гистологический препарат — видны концентрические тельца мозгового вещества тимуса
Вилочковая железа имеет дольчатое строение, в ткани дольки различают корковое и мозговое вещество. Корковое вещество расположено на периферии дольки и в гистологическом микропрепарате выглядит тёмным (в нём много лимфоцитов — клеток с крупными ядрами). В корковом веществе расположены артериолы и кровеносные капилляры, имеющие гемато-тимусный барьер, препятствующий заносу антигенов из крови.
Корковое вещество содержит клетки:
- эпителиального происхождения:
- опорные клетки: формируют «каркас» ткани, образуют гемато-тимусный барьер;
- звездчатые клетки: секретируют растворимые тимические (или тимусные) гормоны — тимопоэтин, тимозин и другие, регулирующие процессы роста, созревания и дифференцировки Т-клеток и функциональную активность зрелых клеток иммунной системы.
- клетки-«няньки»: имеют инвагинации, в которых развиваются лимфоциты;
- гематопоэтические клетки:
- лимфоидного ряда: созревающие T-лимфоциты;
- макрофагального ряда: типичные макрофаги, дендритные и интердигитирующие клетки.
Непосредственно под капсулой в клеточном составе преобладают делящиеся Т-лимфобласты. Глубже находятся созревающие Т-лимфоциты, постепенно мигрирующие к мозговому веществу. Процесс созревания занимает примерно 20 суток. В ходе созревания их происходит реаранжировка генов и формирование гена, кодирующего TCR (Т-клеточный рецептор).
Далее они претерпевают положительную селекцию: во взаимодействии с эпителиальными клетками отбираются «функционально пригодные» лимфоциты, которые способны взаимодействовать с HLA; в ходе развития лимфоцит дифференцируется в хелпер или киллер, то есть на его поверхности остаётся либо CD4, либо CD8. Далее в контакте с эпителиальными клетками стромы отбираются клетки, способные к функциональному взаимодействию: CD8+ лимфоциты, способные к рецепции HLA I, и CD4+ лимфоциты, способные к рецепции HLA II.
Следующий этап — отрицательная селекция лимфоцитов — протекает на границе с мозговым веществом. Дендритные и интердигитирующие клетки — клетки моноцитарного происхождения — отбирают лимфоциты, способные к взаимодействию с антигенами собственного организма, и запускают их апоптоз.
В мозговом веществе в основном содержатся дозревающие Т-лимфоциты. Отсюда они мигрируют в кровоток венул с высоким эндотелием и расселяются по организму. Предполагается также наличие здесь зрелых рециркулирующих Т-лимфоцитов.
Клеточный состав мозгового вещества представлен опорными эпителиальными клетками, звездчатыми клетками, макрофагами. Имеются также выносящие лимфатические сосуды и тельца Гассаля.
Физиология[править | править код]
Функции[править | править код]
Основная роль тимуса — дифференцировка и клонирование Т-лимфоцитов. В тимусе Т-лимфоциты проходят селекцию, в результате чего в кровоток и ткани выходят клетки, которые могут вовлекаться в иммунный ответ против определённых чужеродных антигенов, но не собственного тела. Вырабатывает гормоны: тимозин, тимулин, тимопоэтин, инсулиноподобный фактор роста-1 (ИФР-1), тимусный гуморальный фактор — все они являются белками (полипептидами). При гипофункции тимуса — снижается иммунитет, так как снижается количество Т-лимфоцитов в крови.
Рядом исследований продемонстрирован мнемотропный эффект пептидов тимуса: показано активирующее влияние интраназального введения тактивина и тимозина фракции 5 на процесс формирования условного рефлекса активного избегания, их стресспротекторные свойства и ноотропный эффект от введения в экспериментах на крысах[12]. Влияние пептидов тимуса на функциональную активность центральной нервной системы также заключается в снижении тревожности и увеличении исследовательской активности крыс[13]. Получены интересные результаты о связи состояния тимуса с долголетием человека: в ходе применения препаратов для продления деятельности вилочковой железы снизился биологический возраст девяти испытуемых[14].
Регуляция[править | править код]
Секреция тимических гормонов и функция тимуса регулируется глюкокортикоидами — гормонами коры надпочечников, а также растворимыми иммунными факторами — интерферонов, лимфокинов, интерлейкинов, которые вырабатываются другими клетками иммунной системы. Глюкокортикоиды угнетают иммунитет, а также многие функции тимуса, и приводят к его атрофии.
Пептиды шишковидной железы замедляют инволюцию тимуса[15]. Аналогичным образом действует её гормон мелатонин, способный даже вызывать «омоложение» органа[16]. «Омоложению» тимуса также может способствовать лимфопоэтический фактор роста интерлейкин 7[17], что в будущем может быть использовано для разработки методов восстановления иммунной функции у пожилых людей с помощью лечения рекомбинантным интерлейкином 7[18][19].
Морфогенез[править | править код]
Онтогенез[править | править код]
У эмбриона человека тимус закладывается на 6 неделе развития[20] в энтодерме третьего жаберного кармана. У новорождённого тимус развит до 15 г, к 15 годам увеличиваясь до 40 г. В дальнейшем, к 30 годам вес составляет около 25 г, к 70 годам — всего около 6 г. В исключительных случаях у взрослого человека может не происходить ярко выраженной инволюции вилочковой железы, такое состояние носит название лат. status thymicolymphaticus[11]. Инволюция железы задерживается также у кастрированных животных[21].
Строма тимуса имеет эпителиальное происхождение, происходит из эпителия передней части первичной кишки. Два тяжа (дивертикула) берут начало из третьей жаберной дуги и прорастают в переднее средостение. Иногда строма тимуса формируется также добавочными тяжами из четвёртой пары жаберных дуг. Лимфоциты происходят из стволовых клеток крови, мигрирующих в тимус из печени на ранних стадиях внутриутробного развития. Первоначально в ткани тимуса происходит пролиферация различных клеток крови, но вскоре его функция сводится к образованию Т-лимфоцитов.
Размеры тимуса максимальны в детском возрасте, но после начала полового созревания тимус подвергается значительной атрофии и инволюции. Дополнительное уменьшение размеров тимуса происходит при старении организма, с чем отчасти связывают понижение иммунитета у пожилых людей.
Филогенез[править | править код]
Заболевания тимуса[править | править код]
- Синдром MEDAC
- Синдром Ди Георга
- Миастения — может быть самостоятельным заболеванием, но часто ассоциирована с патологией тимуса и тимомой
Опухоли[править | править код]
- Тимома — из эпителиальных клеток вилочковой железы
- Т-клеточная лимфома — из лимфоцитов и их предшественников
- Пре-Т-лимфобластные опухоли в ряде случаев имеют первичную локализацию в тимусе и выявляются как массивный инфильтрат в средостении с последующей быстрой трансформацией в лейкоз.
- нейроэндокринные опухоли
- более редкие опухоли (сосудистого и нервного происхождения)
Опухоли вилочковой железы могут быть проявлением синдрома множественной эндокринной неоплазии I типа.[22]
Тимус в культуре[править | править код]
Тимус животных может употребляться в пищу человеком, к примеру в таких блюдах как: сладкое мясо, уйкулук[tr].
См. также[править | править код]
- Гемато-тимусный барьер
- Вилочка
- Сумка Фабрициуса
- Тимэктомия[en] — оперативное удаление тимуса[23]
Примечания[править | править код]
- ↑ 1 2 Foundational Model of Anatomy
- ↑ Ковальчук Л. В., Алёшин Б. В., Сорокин А. Ф., Юсфина Э. 3., Ивановская Т. Е., Кузин М. И., Пирогов A. И., Панов Н. А., Таболин B. А. Вилочковая железа // Большая медицинская энциклопедия : в 30 т. / гл. ред. Б. В. Петровский. — 3-е изд. — М. : Советская энциклопедия, 1977. — Т. 4 : Валин — Гамбия. — 576 с. : ил.
- ↑ Тимус // Большая российская энциклопедия : [в 35 т.] / гл. ред. Ю. С. Осипов. — М. : Большая российская энциклопедия, 2004—2017..
- ↑ Gray, H. 4c. The Thymus // (bartleby.com) Anatomy of the Human Body (неопр.). — Philadelphia: Lea & Febiger (англ.)русск., 1918.
- ↑ Миастенические расстройства: физиологииа, патофизиологииа, клиника / Под ред. Н. И. Гращенкова. Лаборатория по изучению нервных и гуморальных регуляции АН СССР // М.: Наука, 1965. — 308 с. (С. 56-60).
- ↑ Щербина В.И., Банина В.Б., Бородулина Л.Г., Полянская З.И., Степанова Е.А. ШЕЙНАЯ ЛОКАЛИЗАЦИЯ АБЕРРАНТНОЙ ВИЛОЧКОВОЙ ЖЕЛЕЗЫ // Детская хирургия.. — 2009. — № 1. — С. 52. — ISSN 1560-9510.
- ↑ Вилочковая железа // Ветеринарный энциклопедический словарь — М.: Советская энциклопедия, 1981. — 640 с.
- ↑ Parasympathetic innervation of the thymus: a histochemical and immunocytochemical study
- ↑ Noradrenergic and peptidergic innervation of lymph… [J Immunol. 1985] — PubMed — NCBI
- ↑ Innervation of the Human Thymus and Spleen — an Overview
- ↑ 1 2 Синельников Р. Д., Синельников Я. Р., Синельников А. Я. Атлас анатомии человека. Том 3: Учение о сосудах и лимфоидных органах / Изд. 7-е, перераб. В 4-х томах // М.: Новая волна, 2009. — 216 с. ISBN 978-5-7864-0201-9. С. 197, 201.
- ↑ Мнемотропный эффект интраназального введения пептидов тимуса. cyberleninka.ru. Дата обращения: 21 июня 2017.
- ↑ Medline.ru – Биомедицинский журнал | Влияние интраназального введения пептидов тимуса на поведение и обучение крыс. medline.ru. Дата обращения: 21 июня 2017.
- ↑ Gregory M. Fahy, Robert T. Brooke, James P. Watson, Zinaida Good, Shreyas S. Vasanawala. Reversal of epigenetic aging and immunosenescent trends in humans (англ.) // Aging Cell. — 2019. — Vol. 18, iss. 6. — P. e13028. — ISSN 1474-9726. — doi:10.1111/acel.13028.
- ↑ SpringerLink — Advances in Gerontology, Volume 1, Number 3 (недоступная ссылка)
- ↑ Rejuvenation of degenerative thymus by oral mel… [J Pineal Res. 2001] — PubMed — NCBI
- ↑ Aspinall, R., Pido-Lopez, J., Imami, N., Henson, S. M., Ngom, P. T., Morre, M., … & Heeney, J. L. (2007). Old rhesus macaques treated with interleukin-7 show increased TREC levels and respond well to influenza vaccination. Rejuvenation research, 10(1), 5-18. doi:10.1089/rej.2006.9098 PMID 17378748
- ↑ Aspinall, R., & Lang, P. O. (2018). Interventions to restore appropriate immune function in the elderly. Immunity & Ageing, 15(1), 5. doi:10.1186/s12979-017-0111-6 PMC 5785902
- ↑ Aspinall, R., & Lang, P. O. (2018). Interleukin-7 and Immunorejuvenation In: Fulop T., Franceschi C., Hirokawa K., Pawelec G. (eds) Handbook of Immunosenescence. Springer, Cham. https://doi.org/10.1007/978-3-319-64597-1_72-1
- ↑ Вилочковая железа // Вешин — Газли. — М. : Советская энциклопедия, 1971. — С. 60. — (Большая советская энциклопедия : [в 30 т.] / гл. ред. А. М. Прохоров ; 1969—1978, т. 5).
- ↑ Зобная железа // Земля — Индейцы. — М. : Советская энциклопедия, 1952. — С. 140. — (Большая советская энциклопедия : [в 51 т.] / гл. ред. Б. А. Введенский ; 1949—1958, т. 17).
- ↑ Simultaneous double thymic carcinoids: a rare initial manifestation of multiple endocrine neoplasia type 1 – Springer. Дата обращения: 29 марта 2013. (недоступная ссылка)
- ↑ Морозов Ю. И. Тимэктомия // Большая медицинская энциклопедия : в 30 т. / гл. ред. Б. В. Петровский. — 3-е изд. — М. : Советская энциклопедия, 1985. — Т. 25 : Тениус — Углекислота. — 544 с. : ил.
Литература[править | править код]
- Гистология, цитология и эмбриология (учебник для вузов). Кузнецов С. Л., Мушкамбаров Н. Н. — М.: МИА, 2007.
- Анатомия человека. В двух томах. Т.2/Авторы: М. Р. Сапин, В. Я. Бочаров, Д. Б. Никитюк и др./Под редакцией М. Р. Сапина. — 5-е издание, переработанное и дополненное. — М.: Медицина, 2001. — 640 с.: ил. ISBN 5-225-04586-3
- Курс лекций по патологической анатомии. Частный курс. Часть II, книги 1,2. / Под ред. академика РАН и РАМН, профессора М. А. Пальцева. — М.: ООО «Издательский дом „Русский врач“», 2003. — 210 с.
- Горлова А. В., Павлов Д. А., Ольховик А. Ю., и др. Мнемотропный эффект интраназального введения пептидов тимуса // Здоровье и образование в XXI веке. — 2016. — Т. 18. — № 1. — С. 1—5. [Gorlova AV, Pavlov DA, Olkhovik AYu, et al. Mnemotropic effect of intranasal administration of thymus peptides. Health and Education Millennium. — 2016. — 18(1): 1—5.]
- Ольховик А. Ю., Новоселецкая А. В. Влияние интраназального введения пептидов тимуса на поведение и обучение крыс // Medline.ru. — 2015. — Т. 16. — С. 1106—1117.
- Зобная железа // Энциклопедический словарь Брокгауза и Ефрона : в 86 т. (82 т. и 4 доп.). — СПб., 1890—1907.
Источник