Лимфоциты и нейтрофилы у спортсменов

- Авторы
- Резюме
- Файлы
Эберт Л.Я.
Колупаев В.А.
В работе представлены результаты наблюдения динамики лейкограммы и показателей фагоцитарной, лизосомальной и НСТ-активности нейтрофилов и моноцитов периферической крови, а также уровня Т- и В-лимфоцитов у спортсменов, использующих в своей подготовке физические нагрузки преимущественно анаэробной или аэробной направленности. Показано, что в период сезонного увеличения продолжительности дня вид двигательной активности оказывает существенное влияние на уровень и особенности динамики фагоцитарной и лизосомальной активности нейтрофилов. Изменения показателей функционального состояния моноцитов в меньшей степени зависели от специфики двигательной активности спортсменов, в то время как характер изменений уровня Т- и В-лимфоцитов существенно различался. Наличие реципрокных влияний на состояние лейкоцитов крови со стороны физических нагрузок и сезонных факторов среды имеет существенное значение для рациональной организации тренировочного процесса анаэробной и аэробной направленности в различных видах спорта.
Уровень адаптационных возможностей индивида обусловлен ритмикой функционального состояния организма, которое модулируется влиянием регулярно повторяющихся и действием внезапных изменений факторов внешней среды [1, 8, 9]. В настоящее время активно обсуждаются механизмы участия клеток иммунной системы в регуляции состояния организма посредством секретируемых ими цитокинов при распознавании и нейтрализации микроорганизмов, опухолевых клеток, тканевых метаболитов и флогогенных агентов [5, 7]. Предполагается, что участие клеток иммунной системы в регуляции функционального состояния организма осуществляется как путем каскадного усиления нейроэндокринной регуляции деятельности соматических клеток и тканей, так и путем секреции пептидных гормонов и нейротрансмиттеров, влияющих на состояние нервной и эндокринной систем [5, 7 и др.].
Как известно, влияние сезонных изменений условий среды на функциональное состояние организма модулируется динамикой физиологических, биохимических и иммунологических процессов [3, 4, 9, 11]. Двигательная активность является одним из важнейших факторов, влияющих как на состояние иммунной системы [10, 12], так и на функциональное состояние организма [1, 2]. Механизм иммунорегуляции функционального состояния организма в процессе адаптации к физическим нагрузкам в изменяющихся условиях среды в настоящее время изучен недостаточно [5, 12]. Можно не сомневаться, что характер сочетания физических нагрузок и изменений условий среды оказывает существенное влияние на степень напряженности адаптационных механизмов, обусловливая, тем самым, «цену адаптации».
Цель работы состояла в изучении динамики показателей функционального состояния лейкоцитов периферической крови у спортсменов, использующих упражнения преимущественно анаэробной или аэробной направленности, в сочетании с сезонными изменениями условий среды.
Организация и методы исследования. Для изучения влияния на организм анаэробных и аэробных физических нагрузок в условиях сезонных изменений условий внешней среды под наблюдением находились дзюдоисты и лыжники, использующие в своей подготовке упражнения соответствующей направленности. В динамике на протяжении трех лет было обследовано 67 борцов и 77 лыжников в возрасте от 16 до 24 лет.
Интерпретацию показателей осуществляли с учётом сезонных условий естественного освещения. В годовом цикле в зависимости от характера изменений длительности дня выделяли восемь качественно своеобразных периодов различной продолжительности. Первому и пятому периодам (декабрь и июнь – соответственно) с минимальной и максимальной длительностью дня присущи малые величины их суточных изменений. Второй и шестой периоды (январь – начало февраля и июль – первая половина августа) характеризуются прогрессивным увеличением и уменьшением длительности дня. Третьему и седьмому периодам (середина февраля – конец апреля и конец августа – октябрь) свойственно стабильное увеличение или уменьшение фотопериода. Четвертый и восьмой периоды (май и ноябрь – соответственно) характеризуются регрессивным увеличением и уменьшением длительности дня. Наши исследования охватывали семь сезонов, исключая период с июля по август, что было обусловлено подготовкой спортсменов вне города.
У спортсменов определяли лейкоцитарную формулу крови и характеристики функционального состояния субпопуляций лейкоцитов (фагоцитарную, лизосомальную и НСТ-активность нейтрофилов и моноцитов, уровень Т- и В-лимфоцитов). Методика исследования функционального состояния лейкоцитов крови подробно описана нами ранее [10, 12]. Результаты исследования были обработаны общепринятыми методами вариационной статистики с применением методов дисперсионного и корреляционного анализа.
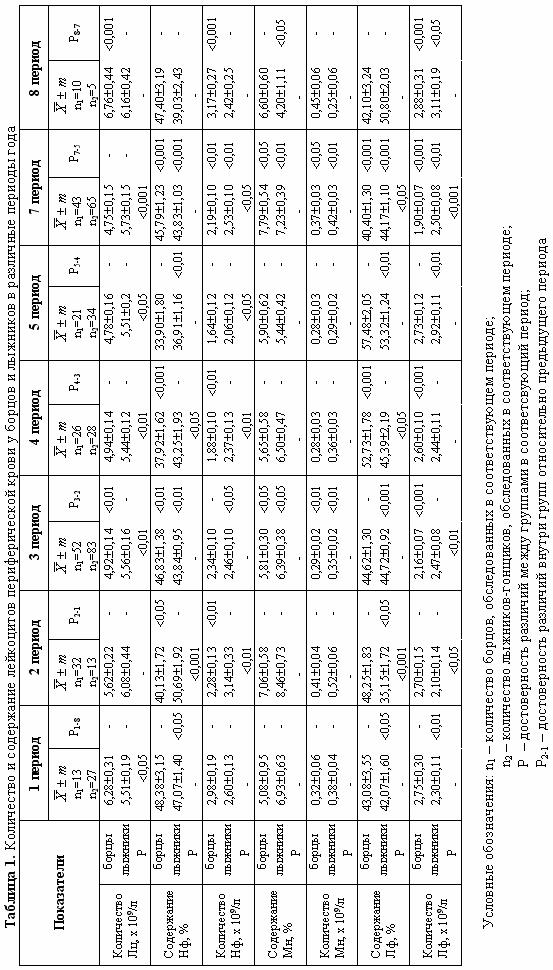
Результаты исследования. Количество и содержание основных субпопуляций лейкоцитов периферической крови у лыжников и борцов в различные периоды годового цикла представлены в таблице 1. Как видно из таблицы, общая тенденция изменения количества нейтрофилов у спортсменов заключалась в снижении уровня циркулирующих клеток в весенне-летний период и повышении их количества в осенне-зимний. На этом фоне наблюдавшиеся отличия динамики уровня нейтрофилов у борцов и лыжников могли быть связаны с различным характером нейроэндокринной регуляции функционального состояния спортсменов в связи с разной динамикой напряженности их спортивной подготовки. При этом менее выраженные изменения среднего уровня нейтрофилов у лыжников по сравнению с борцами, вероятно, связаны с явлением перекрестной адаптации механизмов терморегуляции при регулярных физических нагрузках, отражая более высокий уровень их резистентности у спортсменов, двигательная активность которых осуществляется в условиях естественной среды.
Отсутствие различий в динамике уровня моноцитов у спортсменов обеих специализаций, позволяет предположить, что основной причиной наблюдавшихся изменений являлись известные гормональные сдвиги в организме, инициируемые сезонными колебаниями условий среды [3, 4, 6].
Реципрокные изменения уровня лимфоцитов у спортсменов: снижение их количества у борцов в 3-м и 7-м периодах и повышение у лыжников в 5-м и 8-м периодах, вероятно, были обусловлены влиянием механизмов нейроэндокринной регуляции функционального состояния организма при использовании физических нагрузок анаэробной и аэробной направленности. Следовательно, можно полагать, что характер двигательной активности способен оказывать модифицирующее влияние на сезонный ритм уровня лимфоцитов.
Динамика показателей функционального состояния лейкоцитов крови у спортсменов в различные периоды года представлена в таблице 2. Как видно из таблицы, на протяжении первой половины года динамика и уровень абсолютного показателя фагоцитоза нейтрофилов (АПФН) у борцов и лыжников достоверно различались. Во время исследований, проводившихся во втором полугодии, различия между группами были недостоверны. Можно полагать, что в период увеличения длительности дня механизмы нейроэндокринной регуляции функционального состояния организма в режиме анаэробных и аэробных нагрузок оказывали модифицирующее действие на уровень фагоцитарной активности нейтрофилов.
Основным отличием динамики абсолютного показателя фагоцитоза моноцитов (АПФМн) у спортсменов являлся сдвиг экстремумов этого показателя в годовом цикле. У борцов максимум наблюдали в период регрессивного уменьшения длительности дня и в период его минимальных значений (8-й и 1-й – соответственно), а минимум – при регрессивном увеличении длительности дня (4-й период). У лыжников отмечался сдвиг акрофазы и батифазы этого показателя на более поздний период (2-й и 5-й – соответственно).
Специфика нейроэндокринной регуляции функционального состояния при использовании физических нагрузок анаэробной и аэробной направленности оказывала существенное влияние на характер изменений абсолютного показателя лизосомальной активности нейтрофилов (АПЛАН) во время наиболее интенсивного увеличения продолжительности дня (1-3 периоды). В период уменьшения длительности дня характер двигательной активности, как и в отношении поглотительной функции нейтрофилов, не оказывал существенного влияния на сезонную динамику лизосомальной активности этих клеток.
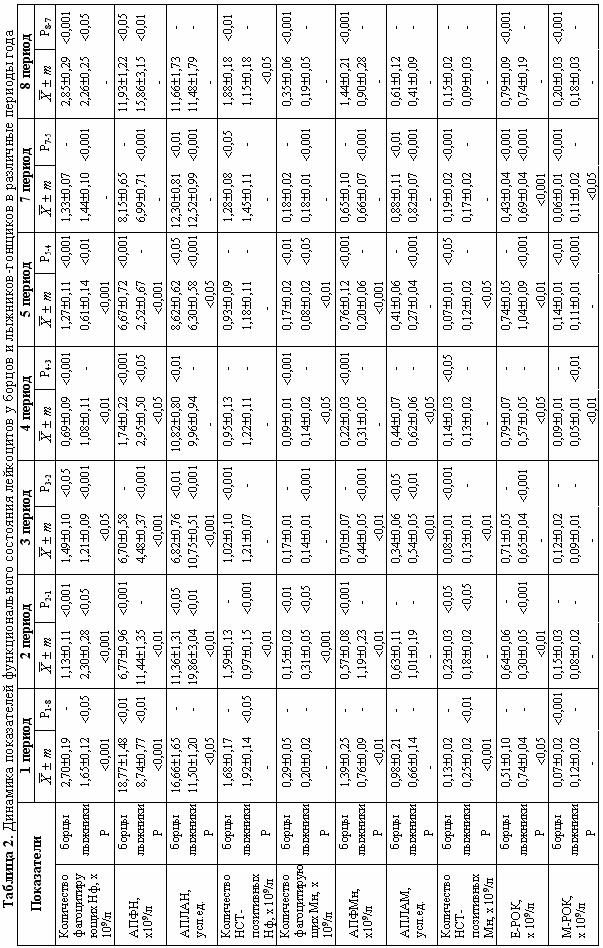
Динамика абсолютного показателя лизосомальной активности моноцитов (АПЛАМ) не зависила от специфики двигательной активности спортсменов и характеризовалась достоверным снижением уровня в весенне-летний период и повышением его в осенне-зимний. При этом в весенний период уровень этого показателя у лыжников был достоверно выше, чем у борцов.
Изменения количества НСТ-позитивных нейтрофилов у лыжников характеризовались наличием отчетливо выраженных экстремумов: максимум – в период минимальных значений длительности дня (1-й период), минимум – в период максимальной продолжительности дня (5-й период). У борцов средний уровень этого показателя повышался в осенне-зимний и понижался в весенне-летний период. При этом колебания среднего уровня НСТ-позитивных моноцитов у них были более выражены, чем у лыжников, у которых количество НСТ-активных моноцитов достоверно изменялось только в период минимальной длительности дня.
Особенностью изменения уровня Т-лимфоцитов являлось значительное снижение данного показателя у борцов в период стабильного уменьшения длительности дня (7-й период), а у лыжников в период прогрессивного увеличения длительности дня (2-й период). При этом у борцов уменьшение количества Т-лимфоцитов было обусловлено снижением уровня циркулирующих лимфоцитов, в то время как аналогичные сдвиги у лыжников были связаны с изменением доли Т-лимфоцитов в общей популяции лимфоцитов.
Существенные колебания уровня В-лимфоцитов у борцов отмечались в период сокращения длительности дня. В период увеличения длительности дня уровень этих клеток у них оставался стабильным. У лыжников динамика количества В-лимфоцитов была менее выражена и проявлялась достоверным их снижением в период регрессивного увеличения длительности дня, совпадавшего с периодом уменьшения уровня физических нагрузок.
Корреляционный анализ позволил выявить прямые связи между величиной используемых физических нагрузок и показателями функционального состояния фагоцитов крови у спортсменов. В тоже время между уровнем последних и параметрами суточной освещенности наблюдалась обратная зависимость. Наличие реципрокных влияний со стороны физических нагрузок и сезонных условий среды на состояние лейкоцитов крови, на наш взгляд, имеет существенное значение для рациональной организации тренировочного процесса анаэробной и аэробной направленности в различных видах спорта.
Список литературы
- Агаджанян Н.А., Шабатура Н.Н. Биоритмы, спорт, здоровье. – М.: Физкультура и спорт, 1989. – 208 с.
- Биоритмы и труд/ Под ред. А.Д. Слоним. – Л.: Наука, 1980. – 144 с.
- Голиков А.П., Голиков П.П. Сезонные ритмы в физиологии и патологии. – М.: Медицина, 1973. – 167 с.
- Деряпа Н.Р., Мошкин М.П., Посный В.С. Проблемы медицинской биоритмологии. – М.: Медицина, 1985. – 208 с.
- Долгушин И.И., Бухарин О.В. Нейтрофилы и гомеостаз. – Екатеринбург: УрО РАН, 2001. – 283 с.
- Комаров Ф.И., Малиновская Н.К., Рапопорт С.И. Мелатонин и биоритмы организма/ В кн. Хронобиология и хрономедицина. – М.: «Триада-Х», 2000. – С. 82-90.
- Маянский А.Н., Маянский Д.Н. Очерки о нейтрофиле и макрофаге. – Новосибирск: Наука, 1989. – 254 с.
- Моисеева Н.И., Любицкий Р.Е. Воздействие гелиогеофизических факторов на организм человека// Проблемы космической биологии: Т. 53. – Л.: Наука, 1986. – 136 с.
- Романов Ю.А., Чепурнов С.А., Клевезаль Г.А. и др. Биологические ритмы// Проблемы космической биологии: Т. 41. – М.: Наука, 1980. – 319 с.
- Рыбаков В.В., Куликов Л.М., Дятлов Д.А., Колупаев В.А., Долгушин И.И., Винантов В.В. Влияние тренировочных программ годичного макроцикла на состояние иммунитета и уровень заболеваемости квалифицированных лыжников-гонщиков// Т и ПФК. – 1995. – № 10. – С. 37-45.
- Теплова С.Н. Временная организация механизмов неспецифической защиты организма от инфекции: Автореф. дис. … д.м.н. – Томск: ТГМИ, 1981. – 32 с.
- Эберт Л.Я., Исаев А.П., Колупаев В.А. Состояние иммунного статуса как показатель степени адекватности тренировочных нагрузок функциональным возможностям спортсменов// Т и ПФК. – 1993. – № 11-12. – С. 20-23.
Библиографическая ссылка
Эберт Л.Я., Колупаев В.А. ВЛИЯНИЕ ФИЗИЧЕСКИХ НАГРУЗОК АНАЭРОБНОЙ И АЭРОБНОЙ НАПРАВЛЕННОСТИ НА СОСТОЯНИЕ ФАГОЦИТОВ ПЕРИФЕРИЧЕСКОЙ КРОВИ И УРОВЕНЬ ЦИРКУЛИРУЮЩИХ Т- И В-ЛИМФОЦИТОВ У СПОРТСМЕНОВ // Современные наукоемкие технологии. – 2004. – № 3. – С. 32-37;
URL: https://top-technologies.ru/ru/article/view?id=21748 (дата обращения: 03.01.2021).
Предлагаем вашему вниманию журналы, издающиеся в издательстве «Академия Естествознания»
(Высокий импакт-фактор РИНЦ, тематика журналов охватывает все научные направления)
Источник
Просмотров: 12773
Категория: Научный фитнес
Создано: 04 Январь 2015
Рубрика: “Спортивная медицина”. Иммунология является одной из наиболее быстро развитых участков биологии и медицины. Спортивная медицина не является исключением. В этой статье мы рассмотрим общие понятия о иммунитете, комплекс факторов неспецифической защиты. Бактерицидность кожи и слизистой оболочки. Фагоцитоз как важнейший фактор противоинфекционной защиты. Система специализированного иммунитета. Лимфоциты. Т-лимфоциты, В-лимфоциты. Иммуноглобулины.
Данные ряда авторов о иммунологические изменения у спортсменов показывают, что занятия физической культурой и спортом стимулируют иммунологическую реактивность, обусловливают снижение общих и инфекционных заболеваний, смертности, увеличивают долговременность жизни, повышают устойчивость к воздействиям неблагоприятных факторов внешней среды. Однако, современный спорт, который характеризуется исключительно высокими физическими нагрузками, может влиять на иммунитет неблагоприятно.
Изменения иммунологических показателей могут быть одним из самых ранних сигналов неблагоприятной реакции организма спортсмена на физические и психоэмоциональные перегрузки, использование иммунологических методов особенно необходимо при оценке состояния здоровья юных спортсменов, так как их организм более лабильный и чувствителен к действиям таких нагрузок. Кроме того, стимуляция иммунологической реактивности может быть признаком благоприятных сдвигов, повышение адаптационных возможностей.
Из сказанного ясно, что интересы “спортивной иммунологии” лежат, прежде всего, в области иммунологии инфекционной (но не исключительно в этой области). Действительно, спортивного врача и тренера интересует в первую очередь, здоровье спортсмена, его устойчивость к заболеваниям, особенно простудливих. Каковы причины такого заболевания, возможны ли какие-либо меры профилактики – это вопрос, который интересует спортивных врачей, тренеров и самих спортсменов.

ИММУНИТЕТ – это способ защиты внутренней устойчивости организма от живых тел и веществ, которые имеют в себе признаки генетически чужеродной информации (Р.В. Петров).
Его главная цель – это распознавание и отделения своего от чужого. Именно иммунитет объединяет численность клеток и тканей в единый организм, руководит сложной индивидуальностью, способствует зарождения жизни и ее сохранению, отодвигает старость и гаснет только тогда, когда исчерпаны все его энергетические ресурсы, обрекает на смерть организм, который хранил (В.И. Гавал).
При рассмотрении вопросов, связанных с иммунологической реактивностью, существенную заинтересованность придают проблеме обычному или неспецифическому иммунитету, который сейчас рассматривается как комплекс факторов неспецифической защиты.
Среди них различают:
- кожаные и слизистые барьеры,
- нормальную микрофлору организма,
- лизоцим,
- воспаление, фагоцитоз,
- барьерную функцию лимфоузлов,
- гуморальные факторы: комплемент, лейкин и лизина,
- клеточную реактивность.
Действительно, барьерные свойства кожи и слизистых оболочек, состояние подкожной соединительной ткани, их кислотно-щелочное равновесие, деятельность мерцательного эпителия дыхательных путей, бактерицидность желудочного сока в значительной степени осуществляют неспецифическую защиту организма против разного рода чужеродных веществ.
Кожа и слизистые оболочки являются для микроорганизмов не только механическим барьером, но они имеют ряд механизмов для их уничтожения. Так, если на кожу нанести некоторое количество кишечных палочек (Е. Соlи), то уже через 5 минут значительная их часть отомрет. Бактерицидность (т.е. способность убивать бактерии) кожи в значительной степени зависит от ее кислотности. Этот эффект связан с отделением потовыми и сальными железами молочной и жирной кислот. Бактерицидность кожи также обусловлена внеклеточными (комплемент, альфа- и бета лизин) и внутриклеточными (лизоцим, лейкин, ферменты) факторами. Следует отметить, что бактерицидность кожи не проявляется в отношении к нормальной аутомикрофлоры (стафилококков, негемолитических стрептококков, дифтероидов, дрожжеподобных грибков и т. д.), которые антагонистически влияют в отношении патогенных микроорганизмов, которые находятся на коже временно и легко отделяются с нее.
Ведущую роль среди факторов естественной защиты полости рта играют ферменты различного происхождения: протеазы, пероксидазы, нуклеазы и т. д. К ним относится лизоцим. Он содержится во всех органах и тканях, значительное его количество находится в селезенке, макрофагах и лейкоцитах. К лизоциму чувствительны стафилококки, стрептококки, дифтерийные и туберкулезные бактерии, дрожжи, а также энтерококки, дизентерийные и брюшнотифозные бактерии, сальмонеллы и т. д. В норме активность лизоцима слюны колеблется в пределах 70-80%.

Рис. 1 Лизоцим
У спортсменов отмечается повышенная активность лизоцима. Однако, высокие тренировочные нагрузки существенно снижают содержание лизоцима в слюне. Снижение активности этого фермента в полости рта и носоглотки может вызвать снижение сопротивляемости организма к респираторным инфекциям, ангин и т. д.
Фагоцитоз является важнейшим фактором противоинфекционной защиты. Основными типами фагоцитов являются нейтрофилы и макрофаги (моноциты), которые способны к миграции в зону инфицирования, поглощения и переваривания микроорганизмов. Нарушение функции фагоцитарных клеток осложняет течение инфекций и делает их хроническими.
Влияние занятий спортом на фагоцитоз зависит от интенсивности физической нагрузки, тренированности и утомление спортсмена. Занятия общей физической подготовкой повышают фагоцитарную активность клеток крови. Интенсивные физические нагрузки, превышающие функциональные возможности спортсмена вызывающие состояние перетренированности и перенапряжения, снижают способность нейтрофилов крови фагоцитоза.

Рис. 2 Фагоцитоз
Среди гуморальных факторов неспецифической защиты особую роль играет комплемент (ферментная система, которая относится к группе глобулинов – 10%), определяется – “С”. Для его активизации необходимы ионы кальция и магния. Он в большом количестве находится в бляшках кишечника и в селезенке. Даже при однократной физической нагрузке средней интенсивности, отмечается снижение титра комплемента. При интенсивной физической нагрузке снижается не только содержание комплемента, но и лизоцима, бактерицидной активности сыворотки крови.
Большое значение в неспецифическом и особенно противовирусной защиты уделяется интерферону. Интерферон поставляется рядом клеток под воздействием вирусов и других агентов. Клетка, которая связана с интерфероном, устойчива к воздействию живого вируса.
СРБ – С-реактивный белок – помогает инициированию реакции фагоцитоза.
Таким образом, практически во всех клетках, тканях и жидкостях организма существуют вещества, которые способны убивать или задерживать размножение микроорганизмов, оказывать бактерицидное или бактериостатическое действие. Они обусловливают естественную устойчивость организма к посторонних веществ. Эта устойчивость является неспецифической и проявляется в отношении очень большого количества веществ, независимо от их характера и свойств. Поэтому и говорят о неспецифичных факторах защиты. Эти механизмы филогенетически более древние. Однако, этих факторов нередко бывает недостаточно, чтобы обеспечить устойчивость организма против посторонних веществ. На некоторые микробы ни комплемент, ни лизоцим не влияют. Более мощное орудие – фагоциты, несмотря на их вседеятельность (кровь, стенки сосудов, соединительная ткань, легкие, печень и т. д.), также довольно часто оказываются неэффективными.
Организм имеет специализированную систему, функцией которой является борьба с посторонними веществами, охрана генетического постоянства соматических клеток, внутренней среды организма. Это система лимфоидных органов, тканей, клеток является- система специализированного иммунитета.
Под системой специализированного иммунитета понимают систему лимфоидных органов и тканей центральных (тимус – вилочковая железа, бурса – сумка Фабрициуса у кур, или костный мозг, и эмбриональная печень) и периферических (селезенка, лимфоузлы, лимфоидные накопления в носоглотке, аппендиксе и других участках кишечника, лимфоциты крови и лимфы и. т. д.).
Основу этой системы составляют лимфоциты, общее количество которых у человека достигает 1012, вес лимфоидной системы достигает 1% веса тела (обычно 700-800 г).
Эта система выполняет надзорную функцию, контролирует генетическую устойчивость организма, сохраняет его индивидуальность. Лимфоциты по кровеносным и лимфатическим сосудам, межтканевым щелям проникают в самые отдаленные участки тела, распознают и уничтожают инородные в генетическом отношении вещества, в том числе и микробные агенты нередко погибают при этом.

Рис. 3 Лимфоцит
Лимфоциты – это небольшие клетки (6-8 микрон), почти целиком состоят из ядра, осуществляют все специфические реакции иммунитета: как продукцию антител, так и реакции иммунитета клеточного типа. Велика их роль в противовирусной защиты: они разрушают пораженные вирусом клетки.
После первого контакта с посторонними антигенами, лимфоциты приобретают новые свойства – становятся как бы специфически направлены против этого антигена, сенсибилизированные к нему. Сенсибилизированные лимфоциты и антитела (at) – основное оружие системы иммунитета. Лимфоциты принимают участие не только в иммунологических реакциях, но и в физиологических механизмах поддерживания гомеостаза организма, процессах воспаления, заживления ран, регенерации тканей, регуляции их роста.
Одним из величайших достижений иммунологии является учение о Т – и В-лимфоциты, о двух формах иммунологического ответа: клеточную и гуморальный. Ответственными за первую из них Т-лимфоциты, за вторую – В-лимфоциты.
Дело в том, что так называемые стволовые клетки костного мозга являются родоначальниками не только кроветворных клеток эритроидного ряда, гранулоцитов, тромбоцитов, но и лимфоцитов. Попадая через кровоток в вилочковую железу – тимуса – они превращаются в тимоциты, а затем в Т-лимфоциты. Вторая часть лимфоцитов, попала в сумку Фабрициуса – бурса – превращается в В-лимфоциты (у человека развитие В-лимфоцитов происходит в костном мозге).


Т-лимфоциты разделяют на несколько видов:
- Т1 лимфоциты (что относительно коротко живущие, слабо рециркулирует, мигрируют к селезенке) и
- Т2-лимфоциты (живущих продолжалось, активно рециркулирует, они составляют основную массу лимфоцитов лимфоузлов, лимфы, крови).
Различают также субпопуляции Т-лимфоцитов:
- Т-лимфоциты, которые отвечают за аллергические реакции, гиперчувствительность замедленного типа (ГЗТ);
- Т-клетки-киллеры, которые вызывают отделение чужеродных трансплантатов, а также и раковых клеток;
- Т-лимфоциты-хелперы и супрессоры, которые играют важную роль в продукции антител (аt), ускоряют или тормозят ее.
В-лимфоциты – предшественники антителообразующих плазматических клеток, производящих до 2000 молекул антител в секунду.
При попадании в организм крупномолекулярных веществ – антигенов (АG) – способных вызвать иммунологические реакции, В-лимфоциты превращаются в плазматические клетки – фабрики, которые производят антитела (аt).
Антителами является крупномолекулярных белковые молекулы глобулинов (иммуноглобулинов). Антитела способны к специфическому соединению с антигенами, которые вызвали их образования. Эти белки составляют до 1% массы крови. Насчитывается огромное количество молекул антител – 1020.
Иммуноглобулины неоднородны по построению и функцией, которую они выполняют.
Различают пять классов иммуноглобулинов (Ig): Ig М, Ig G, Ig А, Ig D, Ig E.
- Прежде всего при введении в организм антигенов появляются Ig М, через несколько дней – Ig G.
- Ig М составляют основную массу антител против полисахаридных антигенов, 0-антигенов грамположительных бактерий и т. д. Они составляют примерно 10% от общего количества Ig (молекулярный вес 900000 Дальтон).
- Ig G составляют 70-75% от всех Ig. Их молекулярная масса 150000 дальтон.
- Ig А составляют 20% от всех Ig. Они есть не только в сыворотке крови, но и в слюне, кишечном соке, молозиве, мокроте. Имеют молекулярный вес 385000 Дальтон, играют большую роль в «местном» иммунитете.
- Ig D (1%) являются рецепторами В-лимфоцитов. Они определяются только в сыворотке человека и приматов. Молекулярный вес 170000-200000 Дальтон. Количество Ig D увеличивается с возрастом и достигает максимума в 10 лет, затем несколько снижается и в 15-летних подростков достигает концентрации взрослого человека.
- Ig E (200000 Дальтон) – количество их в сыворотке человека незначительна, но биологическая роль их очень велика. Они помогают возникновению аллергической реакции, играют некоторую роль в иммунном ответе на паразиты.
Следует отметить нестабильность системы иммунитета, состав клеток которой постоянно изменяется вследствие рециркуляции лимфоцитов и постоянного их обмена – перехода из органов в лимфу, из нее в крови, оттуда снова в лимфоидных органов, а также вследствие естественного обновления лимфоцитов.
В В-лимфоцитов наименьшая продолжительность жизни (примерно одну неделю), в различных Т-лимфоцитов – от одного до трех-четырех и более месяцев.
Автор: к. мед. н., проф. Пешкова О.В.
Дата публикации: 05.01.2015
Смотрим слайд
Источник