Клональная селекция в лимфоцитов


- Немного из истории
- Клональная селекция – что это?
- Суть клонально-селекционной теории иммунитета
- Главные принципы
- Подводим итоги
- Видео по теме
Что такое иммунитет? Это способность организма поддерживать свою целостность и активность благодаря распознаванию, а затем удалению чужеродных вредоносных веществ и клеток. Иммунитету человека посвящено много статей, научных работ, диссертаций. Множество ученых трудились над данной темой, выдвигая различные теории и проводя те или иные эксперименты. Так, большого резонанса набрала клонально-селекционная теория иммунитета, речь о которой пойдет в этой статье.
Немного из истории
Впервые о селекционной теории заговорил Пауль Эрлих. Еще в 1900 году он предположил, что в организме существуют клетки, на оболочке которых содержится большое количество различных молекул антител. Согласно его теории, данные клетки способны синтезировать любое из расположенных на поверхности антител. После связывания одного антитела с чужеродным антигеном, клетка начинает вырабатывать антитела такой же специфичности.
Позже выяснилось, что теория Пауля Эрлиха была не совсем верной. Но, начиная с 1950-х годов, ученые представляли более расширенные и приближенные к современной теории мысли. Так, весьма плодотворный вклад в эту тему сделал Нильсон Ерне в 1955 году. Благодаря его работе иммунологи в дальнейшем переместили интерес с инструктивной теории на селекционную. Отметим, что инструктивная теория основывалась на концепции, согласно которой лимфоциты под воздействием антигенов могут по несколько раз перенастраиваться, менять свои гены.
В 1957 году Дэвид Талмейдж, работая над вопросом иммунной системы человека, выразил мысль об отборе клеток. Но это была довольно краткая форма работы. И в том же году Фрэнк Макфарлейн Бернет развил эту мысль, предоставив более широкое и развернутое понятие данной теории. Причем, подтвердив ее правдивость экспериментально.

Клональная селекция – что это?
В основе данного понятия лежит идея дарвиновского отбора. То есть, если на поверхности незрелого лимфоцита рецептор вступает в связь с антигеном, поступает «отрицательный» сигнал, в результате чего клетка уничтожается. И, напротив, если рецептор, содержащийся на поверхности зрелого лимфоцита, начинает взаимодействовать с антигеном, выполняется продуцирование, секретирование и размножение антител. Данный процесс, происходящий в местах развития лимфоцитов, Бернет классифицировал как уничтожение «запрещенных» клонов.
Суть клонально-селекционной теории иммунитета
Итак, главная идея данной теории заключается в том, что в организме под воздействием тех или иных антигенов появляются так называемые клоны клеток. Далее антиген начинает контактировать с клоном, благодаря чему происходит стимуляция выработки антител. Контакт антигена с клоном клетки выполняется в избирательном порядке. Такая теория определяет функционирование всего иммунитета, который способен определять и распознавать огромнейшее число чужеродных элементов – антигенов. То есть, организм человека должен синтезировать тысячи и даже сотни тысяч различных молекул антител с соответствующими распознающими зонами.
Если говорить об этой же теории более простым языком, получается, что лимфоциты, выступающие в роли иммунных клеток организма, способны однажды изменить свой генотип, настраиваясь, отвечая и противодействуя какому-то одному чужеродному веществу, которым выступает обычно часть микроба или вируса. То есть, антиген. Происходит это только один раз, чаще всего у зародыша, и совершенно случайно, при том, до того, как клетка встретится с этим чужеродным элементом. Затем, когда контакта с антигенами уже не избежать, происходит селекция, то есть, отбор клеток, которые смогут противостоять микробам и защищать организм от вирусов. Помимо отбора таких клеток, происходит их интенсивное и масштабное размножение. Клетки, образовавшиеся в процессе размножения одного лимфоцита, называются клонами.
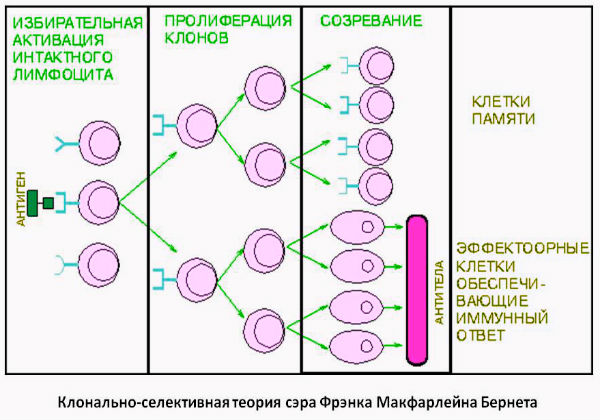
Главные принципы клонально-селекционной теории
Бернетом были приведены и доказаны следующие утверждения:
- В организме человека еще до первого контакта с антигенами уже существуют лимфоциты и антитела с нужной специфичностью;
- На поверхности лимфоцитов, принимающих участие в работе иммунной системы, расположены рецепторы антигенспецифического действия. При этом, если речь идет о B-лимфоцитах, в роли данных рецепторов выступают молекулы такой же специфичности, что и антитела, продуцируемые и секретируемые лимфоцитами;
- На поверхности лимфоцита расположены рецепторы исключительно одной специфичности;
- Лимфоциты, взаимодействующие с чужеродным элементом (антигеном), подвергаются нескольким этапам пролиферации. Также происходит масштабное клонирование плазматических клеток.

Подводим итоги
Клонально-селекционная теория иммунитета, представленная Бернетом в 1957 году, сыграла значимую роль уже в современных работах, касающихся функционирования иммунной системы человека. Некоторые ученые даже утверждают, что все учения и работы об иммунитете делятся на «до» и «после» возникновения и подтверждения клонально-селекционной теории. Позже были проведены сотни исследований на иммунологическую тему, в результате чего были выявлены различные классы клеток и их роль в противостоянии иммунитета вредоносным микробам, однако основные принципы теории Бернета до сих пор актуальны, справедливы и правдивы.
Видео по теме:
Источник
Суть клонально-селекционной теории
Ф.Бернета заключается в том, что в
процессе созревания лимфоцитов происходит
строгая выбраковка клеток по следующим
признакам:
Неспособность к распознаванию рецепторов
МНС 1 и МНС 2 клеток собственного
организма;Способность к распознаванию собственных
антигенов, презентируемых на МНС 1 и
МНС 2.
Клетки, имеющие вышеперечисленные
признаки, подлежат уничтожению. Остальные
лимфоциты продолжают дифференцировку
и становятся родоночальниками клонов
– групп лимфоцитов, имеющих
антигенраспознающий рецептор одинаковой
специфичности.
Селекция т-лимфоцитов
Незрелые T-лимфоциты мигрируют из
костного мозга в кору тимуса и начинают
интенсивно делиться. В коре тимуса в
процессе контакта с эпителиальными
клетками тимуса, которые экспрессируют
и MHC I и MHC II молекулы осуществляется
позитивная селекция. Лимфоциты, способные
взаимодействовать с молекулами МНС,
получают позитивный стимул – сигнал к
размножению, а клетки неспособные
взаимодействовать с МНС получают
негативный сигнал к самоликвидации
(апоптозу).
Далее прошедшие позитивную селекцию
лимфоциты мигрируют в мозговое вещество
тимуса и на границе коры и мозгового
вещества происходит негативная селекция
Т-лимфоцитов. Негативная селекция
осуществляется в процессе их взаимодействия
с дендритными клетками и макрофагами,
которые презентируют собственные
антигены организма.
Аутоагрессивные Т-лимфоциты получают
сигнал к самоликвидации (негативная
селекция), аутотолерантные – продолжают
размножаться и покидают мозговое
вещество тимуса, расселяются по
периферическим органам иммунной системы.
Было показано, что в процессе селекции
не проходит отбор и погибает около 95%
Т-лимфоцитов.
Лимфоциты, располагающиеся в корковом
слое тимуса вначале имеют на мембране
как CD4, так и CD8 – рецепторы. Далее клетки,
распознающие MHC I теряют CD4 и становятся
CD8+ , т.е. превращаются в ЦТЛ, а клетки,
распознающие MHC II – наоборот, теряют
CD8 и превращаются в CD4+, т.е. в Т-хелперы.
Т-лимфоциты, прошедшие дифференцировку
и отбор в тимусе называются «наивные»
Т-лимфоциты. После встречи с соответствующим
антигеном они превращаются в примированные
или эффекторные Т-лимфоцитами, готовые
воспринимать цитокиновые сигналы к
активации.
Селекция в-лимфоцитов
В костном мозге незрелые B-лимфоциты,
проходят негативную селекцию. Лимфоциты,
способные связывать собственные антигены
своим поверхностным антигенраспознающим
рецептором IgM, получают сигнал к
самоликвидации (апоптозу) и погибают.
Прошедшие негативный отбор В-лимфоциты
делятся, причем, каждый из них образует
группу потомков, клон, обладающих
одинаковой специфичностью. Зрелые
В-лимфоциты выходят из костного мозга
в кровоток и заселяют лимфоидные органы.
Лекция 6. Нарушения иммунитета
К нарушениям иммунитета относятся:
Реакции гиперчувствительности;
Аутоиммунные реакции;
Иммунодефицитные состояния.
Реакции гиперчувствительности.
Классификация Джелла и Кумбса – 4 типа
реакций гиперчувствительности.
РГЧ 1-го типа.
Астма, сенная лихорадка, экзема,
крапивница, пищевая аллергия.
Аллергены: лекарственные вещества,
гетерологичная сыворотка, пыльца
растений, фекалии микроклещей пыли,
пищевые продукты (яйца, молоко, крабы,
рыба и др).
Факторы, способствующие проникновению
аллергенов в слизистую оболочку являются
частицы дизельных выхлопов (ЧДВ),
содержащиеся в городской атмосфере.
Наследственная предрасположенность
к аллергическим реакциям 1-го типа
связана с аллелями HLA-B8
иDR3.
Диагностика: постановка кожных проб.
Лечение: гипосенсибилизация –
подкожное введение возрастающих доз
аллергена, в результате происходит
переключение на преимущественный синтез
IgG.
Профилактика: исключение контакта с
аллергеном; при необходимости введения
гетерологичной лечебной сыворотки –
дробное введение по Безредке. Назначение
антигистаминных препаратов.
РГЧ 2-го типа – цитотоксические реакции
с участием IgGи комплемента.
Наблюдаются в случае, если антитела
реагируют с антигеном, находящимся на
клеточной мембране. При этом к
образовавшемуся комплексу присоединяется
комплемент, последние фракции которого
(С5-С9) называются перфоринами. Белковые
молекулы этих фракций встраиваются в
клеточную мембрану, образуя крупную
пору, через которую в клетку поступает
вода. В результате происходит лизис
клетки. Этот тип гиперчувствительности
может развиться при длительном применении
лекарственных преператов, способных
адсорбироваться на эритроцитах;
пример-антиаритмический препарат
квинидин. Примером РГЧ 2-го типа является
гемолитическая болезнь новорожденных
при резус-конфликте (ретикулоцитоз).
Другой пример- тромбоцитопеническая
пурпура.
РГЧ 3-го типа связаны с образованием
большого количества иммунных комплексов
при поступлении в организм большого
количества чужеродного белка без
предварительной сенсибилизации, например
при введении лечебных или профилактических
гетерологичных антисывороток. В
результате временного дефицита
комплемента происходит отложение малых
иммунных комплексов в стенках сосудов,
суставах, почечных клубочках. После
восполнения дефицита комплемента он
фиксируется на малых иммунных комплексах
(МИК), находящихся в тканях. К образовавшимся
большим иммунным комплексам (БИК)
мигрируют макрофаги, которые поглощают
БИК и выделяют цитокины, вызывающие
воспалительную реакцию. Результатом
РГЧ 3-го типа является развитие сывороточной
болезнм, проявлениями которой являются
васкулит, артрит и гломерулонефрит.
РГЧ 3-го типа может проявляться в
форме так называемого феномена Артюса.
В отличие от сывороточной болезни,
феномен Артюса – это бурная местная
воспалительная реакция, которая
сопровождается некрозом тканей в месте
введения антигена. Обязательным условием
для развития реакции Артюса является
предварительная сенсибилизация организма
данным антигеном (чужеродным белком) и
наличие в сыворотке крови высокой
концентрации антител к этому антигену.
РГЧ 4-го типа происходят с участием
цитотоксических лимфоцитов.
Существуют 3 вида РГЧ 3-го типа: контактная,
туберкулиновая и гранулематозная.
Контактная гиперчувствительность
характеризуется экзематозной реакцией
в месте воздействия антигена.
Сенсибилизация организма происходит,
как правило соединениями никеля, хрома,
веществами, входящими в состав моющих
средств, т.е гаптенами. Основными АПК
при контактной гиперчувствительности
являются дендритные клетки кожи –
клетки Лангерганса. Реакция контактной
гиперчувствительности протекает в 2
стадии: сенсибилизации и проявления.
Период сенсибилизации длится около
2-х недель. Гаптен, проникнув в кожу,
соединяется с белком. Этот комплекс
поглощают дендритные клетки, которые
впоследствии презентируют гаптен-белковый
комплекс Т-лимфоцитам. В сенсибилизированном
организме после повторного контакта
с антигеном в течение 48-72 часов происходит
миграция Т-лимфоцитов к месту контакта
с антигеном и развивается местная
воспалительная реакция.Гиперчувствительность туберкулинового
типа. Туберкулин – это фильтрат убитой
культуры туберкулезной палочки,
содержащий бактериальные антигены.
Впервые был получен Р.Кохом.
Реакция гиперчувствительности на
туберкулин возникает только у лиц, в
организме которых присутствуют живые
возбудители туберкулеза. После
внутрикожного введения туберкулина к
месту введения мигрируют моноциты и
сенсибилизированные Т-лимфоциты, которые
выделяют цитокины (ФНО-альфа и бета).
Цитокины повышают проницаемость
сосудистой стенки и в месте введения
туберкулина образуется воспалительный
инфильтрат, который достигает максимальных
размеров через 48 часов.
Гранулематозная гиперчувствительность.
Гранулематозные реакции развиваются
в тех случаях, когда инфекционный
агент остается жизнеспособным в
макрофагах, например, при туберкулезе
и проказе. Активированный макрофаг,
внутри которого находятся живые
возбудители, трансформируется в
эпителиоидную клетку, которая активно
продуцирует цитокины – ФНО. Эпителиоидные
клетки сливаются друг с другом, образуя
гигантские клетки Лангганса. В центре
гранулемы располагаются эпителиоидные
клетки, клетки Лангганса и макрофаги.
Центр гранулемы окружают Т-лимфоциты.
Кнаружи от Т-лимфоцитов находится зона
пролиферирующих фибробластов, которые
отграничивают зону воспаления от
здоровых тканей.
Соседние файлы в предмете Микробиология
- #
- #
- #
- #
- #
- #
- #
- #
Источник
Механизм активации клона лимфоцитов. Формирование антител плазматическими клетками
Каждый клон лимфоцитов чувствителен только к одному типу антигена (или к нескольким сходным антигенам, имеющим практически те же стереохимические характеристики). Связано это с наличием особых белков на поверхности мембран этих клеток. Так, на поверхности клеточной мембраны каждого из В-лимфоцитов имеются около 100000 молекул антител, которые будут реагировать высокоспецифически только с определенным типом антигена.
Следовательно, при появлении соответствующего антигена он немедленно прикрепляется к антителу в клеточной мембране; это ведет к процессу активации, который мы опишем подробнее далее. На поверхности мембраны Т-лимфоцитов имеются молекулы, подобные антителам и называемые поверхностными рецепторными белками (или маркерами Т-клеток); они тоже высокоспецифичны для определенного активирующего антигена.
а) Роль макрофагов в процессе активации. Помимо лимфоцитов в лимфоидной ткани также присутствуют буквально миллионы макрофагов. Они выстилают синусоиды лимфатических узлов, селезенки и других лимфоидных тканей и контактируют со многими лимфоцитами лимфатических узлов. Большинство проникших в тело человека микроорганизмов сначала фагоцитируются и частично перевариваются макрофагами, причем антигенные продукты освобождаются в цитозоль макрофагов.
Макрофаги затем передают эти антигены путем клеточно-клеточных контактов непосредственно лимфоцитам, что ведет к активации определенных лимфоцитарных клонов. Макрофаги, кроме того, секретируют особое активирующее вещество, способствующее дальнейшему росту и размножению специфических лимфоцитов. Это вещество называют интерлейкином-1.
б) Роль Т-клеток в активации В-лимфоцитов. Большинство антигенов активируют одновременно и Т-, и В-лимфоциты. Некоторые Т-клетки, называемые Т-хелперами, секретируют специфические вещества (в совокупности называемые лимфокинами), которые активируют специфические В-лимфоциты. Действительно, без помощи Т-хелперов количество антител, формируемых В-лимфоцитами, обычно незначительно. Мы вернемся к обсуждению взаимодействия между Т- и В-клетками при изложении механизмов Т-клеточной системы иммунитета.
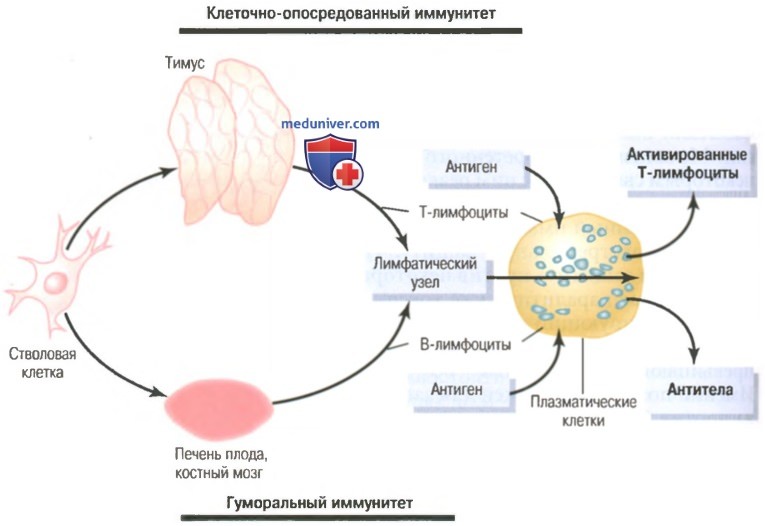
Формирование антител и активированных лимфоцитов в лимфатическом узле в ответ на действие антигенов.
Этот рисунок также демонстрирует происхождение лимфоцитов тимуса (Т-лимфоцитов) и бурсы (В-лимфоцитов), ответственных за клеточно-опосредованные и гуморальные иммунные процессы, соответственно
Специфические свойства В-лимфоцитарной системы: гуморальный иммунитет и антитела
а) Формирование антител плазматическими клетками. До воздействия специфического антигена клоны В-лимфоцитов находятся в лимфоидной ткани в состоянии покоя. При входе инородного антигена макрофаги лимфоидной ткани фагоцитируют антиген и затем представляют его прилежащим В-лимфоцитам. Кроме того, одновременно антиген представляется также Т-клеткам, и формируются активированные Т-лимфоциты. Эти Т-хелперы также вносят вклад в мощную активацию В-лимфоцитов, что мы обсудим подробно далее.
В-лимфоциты, специфичные для данного антигена, немедленно увеличиваются и принимают вид лимфобластов. Некоторые из них подвергаются дальнейшей дифференцировке, превращаясь в плазмобласты, которые являются предшественниками плазматических клеток. В плазмобластах увеличивается объем цитоплазмы, и очень сильно разрастается гранулярная эндоплазматическая сеть.
Плазмобласты затем начинают делиться со скоростью примерно один раз каждые 10 ч, производя около девяти делений, что через 4 сут приводит к появлению общей популяции примерно из 500 клеток на каждый исходный плазмобласт. Затем каждая зрелая плазматическая клетка синтезирует гамма-глобулиновые антитела с чрезвычайно высокой скоростью, примерно 2000 молекул в секунду. В свою очередь, антитела секретируются в лимфу и переносятся в циркулирующую кровь.
Этот процесс продолжается в течение нескольких дней или недель до тех пор, пока в итоге не произойдет истощение и гибель плазматических клеток.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
– Также рекомендуем “Формирование клеток памяти. Антитела и их специфичность”
Оглавление темы “Механизмы Т-клеточного иммунитета. Антигены клеток крови”:
1. Механизм активации клона лимфоцитов. Формирование антител плазматическими клетками
2. Формирование клеток памяти. Антитела и их специфичность
3. Механизмы действия антител. Система комплемента при активации антител
4. Активированные Т-клетки. Антиген-представляющие клетки
5. Т-хелперы. Функции лимфокинов
6. Цитотоксические Т-клетки. Супрессорные Т-клетки
7. Причины аутоиммунных заболеваний. Иммунизация путем введения антигенов
8. Аллергические реакции замедленного типа. Анафилаксия
9. Крапивница, поллиноз. Антигены клеток крови
10. Генетическое определение агглютиногенов. Агглютинины
Источник