Клон лимфоцитов что это

Роль лимфоцитарных клонов. Происхождение клонов лимфоцитова) Высокоспецифическая реакция Т-лимфоцитов и В-лимфоцитарных антител против определенных антигенов. Роль лимфоцитарных клонов. Когда специфические антигены вступают в контакт с Т- и В-лимфоцитами в лимфоидной ткани, происходит активация некоторых Т-лимфоцитов, формирующих активированные Т-клетки, и некоторых В-лимфоцитов, формирующих антитела. Активированные Т-клетки и антитела, в свою очередь, реагируют высокоспецифически против особых типов антигенов, которые инициировали их развитие. Механизм этой специфичности изложен далее. Миллионы специфических типов лимфоцитов хранятся в лимфоидной ткани. Как объяснялось ранее, в лимфоидной ткани хранятся миллионы разных типов, заранее сформированных В- и Т-лимфоцитов, способных образовывать высокоспецифические типы антител или Т-клеток. Каждый из этих лимфоцитов способен к формированию только одного типа антитела или одного типа Т-клетки с уникальной специфичностью. И только специфический антиген, с которым лимфоцит может реагировать, активирует его. Сразу после активации специфическим антигеном лимфоцит очень интенсивно размножается, образуя огромное количество своих копий. Если это В-лимфоцит, его потомство будет, в конце концов, секретировать антитела специфического типа, циркулирующие затем по телу. Если это Т-лимфоцит, его потомством являются специфически активированные Т-клетки, которые выделяются в лимфу, затем переносятся в кровь, а с нею попадают во все тканевые жидкости, откуда возвращаются снова в лимфу, иногда циркулируя по этому кругу в течение нескольких месяцев или лет. Лимфоциты, способные к формированию антител или Т-клеток уникальной специфичности, называют клоном лимфоцитов. Это значит, что в каждом клоне лимфоциты идентичны и происходят от одного или нескольких ранних лимфоцитов специфического для данного клона типа.
б) Происхождение многих клонов лимфоцитов. Количество генов, кодирующих миллионы разных типов антител и Т-лимфоцитов, гораздо меньше — от нескольких сотен до нескольких тысяч. Сначала было непонятно, как может такое небольшое число генов кодировать миллионы особенностей молекул антител или Т-клеток, создаваемых лимфоидной тканью, особенно если учесть, что для образования каждого особого типа белка обычно необходим один ген. В настоящее время ответ на этот вопрос получен. В исходных стволовых клетках, из которых формируются нормальные иммунные клетки, нет целого гена для формирования каждого типа Т- или В-клетки. Существуют лишь «сегменты генов», фактически сотни таких сегментов, но не целые гены. Во время предварительной обработки соответствующих Т- и В-лимфоцитов эти генные сегменты смешиваются друг с другом в случайных комбинациях, формируя в итоге целые гены. Поскольку существуют несколько сотен типов генных сегментов и миллионы различных комбинаций, в которые они могут быть собраны в отдельных клетках, легко понять возможность появления миллионов генетически различных клеточных типов. Генетическая структура каждого формирующегося в итоге функционально полноценного Т- или В-лимфоцита кодирует только одну антигенную специфичность. Зрелые Т- и В-лимфоциты являются высокоспецифичными клетками, которые распределяются по лимфоидной ткани и заселяют ее. – Также рекомендуем “Механизм активации клона лимфоцитов. Формирование антител плазматическими клетками” – Вернуться в оглавление раздела “Физиология человека.” Оглавление темы “Клетки иммунитета. Виды иммунитета”: |
Источник
Механизм активации клона лимфоцитов. Формирование антител плазматическими клетками
Каждый клон лимфоцитов чувствителен только к одному типу антигена (или к нескольким сходным антигенам, имеющим практически те же стереохимические характеристики). Связано это с наличием особых белков на поверхности мембран этих клеток. Так, на поверхности клеточной мембраны каждого из В-лимфоцитов имеются около 100000 молекул антител, которые будут реагировать высокоспецифически только с определенным типом антигена.
Следовательно, при появлении соответствующего антигена он немедленно прикрепляется к антителу в клеточной мембране; это ведет к процессу активации, который мы опишем подробнее далее. На поверхности мембраны Т-лимфоцитов имеются молекулы, подобные антителам и называемые поверхностными рецепторными белками (или маркерами Т-клеток); они тоже высокоспецифичны для определенного активирующего антигена.
а) Роль макрофагов в процессе активации. Помимо лимфоцитов в лимфоидной ткани также присутствуют буквально миллионы макрофагов. Они выстилают синусоиды лимфатических узлов, селезенки и других лимфоидных тканей и контактируют со многими лимфоцитами лимфатических узлов. Большинство проникших в тело человека микроорганизмов сначала фагоцитируются и частично перевариваются макрофагами, причем антигенные продукты освобождаются в цитозоль макрофагов.
Макрофаги затем передают эти антигены путем клеточно-клеточных контактов непосредственно лимфоцитам, что ведет к активации определенных лимфоцитарных клонов. Макрофаги, кроме того, секретируют особое активирующее вещество, способствующее дальнейшему росту и размножению специфических лимфоцитов. Это вещество называют интерлейкином-1.
б) Роль Т-клеток в активации В-лимфоцитов. Большинство антигенов активируют одновременно и Т-, и В-лимфоциты. Некоторые Т-клетки, называемые Т-хелперами, секретируют специфические вещества (в совокупности называемые лимфокинами), которые активируют специфические В-лимфоциты. Действительно, без помощи Т-хелперов количество антител, формируемых В-лимфоцитами, обычно незначительно. Мы вернемся к обсуждению взаимодействия между Т- и В-клетками при изложении механизмов Т-клеточной системы иммунитета.
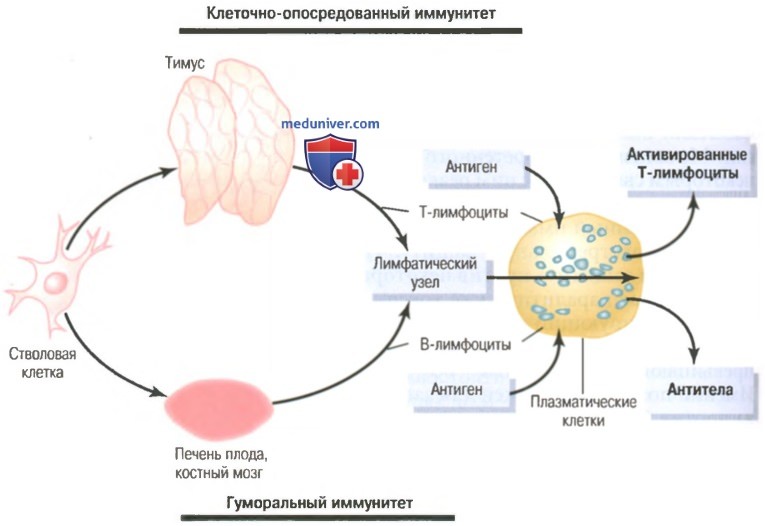
Формирование антител и активированных лимфоцитов в лимфатическом узле в ответ на действие антигенов.
Этот рисунок также демонстрирует происхождение лимфоцитов тимуса (Т-лимфоцитов) и бурсы (В-лимфоцитов), ответственных за клеточно-опосредованные и гуморальные иммунные процессы, соответственно
Специфические свойства В-лимфоцитарной системы: гуморальный иммунитет и антитела
а) Формирование антител плазматическими клетками. До воздействия специфического антигена клоны В-лимфоцитов находятся в лимфоидной ткани в состоянии покоя. При входе инородного антигена макрофаги лимфоидной ткани фагоцитируют антиген и затем представляют его прилежащим В-лимфоцитам. Кроме того, одновременно антиген представляется также Т-клеткам, и формируются активированные Т-лимфоциты. Эти Т-хелперы также вносят вклад в мощную активацию В-лимфоцитов, что мы обсудим подробно далее.
В-лимфоциты, специфичные для данного антигена, немедленно увеличиваются и принимают вид лимфобластов. Некоторые из них подвергаются дальнейшей дифференцировке, превращаясь в плазмобласты, которые являются предшественниками плазматических клеток. В плазмобластах увеличивается объем цитоплазмы, и очень сильно разрастается гранулярная эндоплазматическая сеть.
Плазмобласты затем начинают делиться со скоростью примерно один раз каждые 10 ч, производя около девяти делений, что через 4 сут приводит к появлению общей популяции примерно из 500 клеток на каждый исходный плазмобласт. Затем каждая зрелая плазматическая клетка синтезирует гамма-глобулиновые антитела с чрезвычайно высокой скоростью, примерно 2000 молекул в секунду. В свою очередь, антитела секретируются в лимфу и переносятся в циркулирующую кровь.
Этот процесс продолжается в течение нескольких дней или недель до тех пор, пока в итоге не произойдет истощение и гибель плазматических клеток.
– Также рекомендуем “Формирование клеток памяти. Антитела и их специфичность”
Оглавление темы “Механизмы Т-клеточного иммунитета. Антигены клеток крови”:
1. Механизм активации клона лимфоцитов. Формирование антител плазматическими клетками
2. Формирование клеток памяти. Антитела и их специфичность
3. Механизмы действия антител. Система комплемента при активации антител
4. Активированные Т-клетки. Антиген-представляющие клетки
5. Т-хелперы. Функции лимфокинов
6. Цитотоксические Т-клетки. Супрессорные Т-клетки
7. Причины аутоиммунных заболеваний. Иммунизация путем введения антигенов
8. Аллергические реакции замедленного типа. Анафилаксия
9. Крапивница, поллиноз. Антигены клеток крови
10. Генетическое определение агглютиногенов. Агглютинины
Источник

- Немного из истории
- Клональная селекция – что это?
- Суть клонально-селекционной теории иммунитета
- Главные принципы
- Подводим итоги
- Видео по теме
Что такое иммунитет? Это способность организма поддерживать свою целостность и активность благодаря распознаванию, а затем удалению чужеродных вредоносных веществ и клеток. Иммунитету человека посвящено много статей, научных работ, диссертаций. Множество ученых трудились над данной темой, выдвигая различные теории и проводя те или иные эксперименты. Так, большого резонанса набрала клонально-селекционная теория иммунитета, речь о которой пойдет в этой статье.
Немного из истории
Впервые о селекционной теории заговорил Пауль Эрлих. Еще в 1900 году он предположил, что в организме существуют клетки, на оболочке которых содержится большое количество различных молекул антител. Согласно его теории, данные клетки способны синтезировать любое из расположенных на поверхности антител. После связывания одного антитела с чужеродным антигеном, клетка начинает вырабатывать антитела такой же специфичности.
Позже выяснилось, что теория Пауля Эрлиха была не совсем верной. Но, начиная с 1950-х годов, ученые представляли более расширенные и приближенные к современной теории мысли. Так, весьма плодотворный вклад в эту тему сделал Нильсон Ерне в 1955 году. Благодаря его работе иммунологи в дальнейшем переместили интерес с инструктивной теории на селекционную. Отметим, что инструктивная теория основывалась на концепции, согласно которой лимфоциты под воздействием антигенов могут по несколько раз перенастраиваться, менять свои гены.
В 1957 году Дэвид Талмейдж, работая над вопросом иммунной системы человека, выразил мысль об отборе клеток. Но это была довольно краткая форма работы. И в том же году Фрэнк Макфарлейн Бернет развил эту мысль, предоставив более широкое и развернутое понятие данной теории. Причем, подтвердив ее правдивость экспериментально.

Клональная селекция – что это?
В основе данного понятия лежит идея дарвиновского отбора. То есть, если на поверхности незрелого лимфоцита рецептор вступает в связь с антигеном, поступает «отрицательный» сигнал, в результате чего клетка уничтожается. И, напротив, если рецептор, содержащийся на поверхности зрелого лимфоцита, начинает взаимодействовать с антигеном, выполняется продуцирование, секретирование и размножение антител. Данный процесс, происходящий в местах развития лимфоцитов, Бернет классифицировал как уничтожение «запрещенных» клонов.
Суть клонально-селекционной теории иммунитета
Итак, главная идея данной теории заключается в том, что в организме под воздействием тех или иных антигенов появляются так называемые клоны клеток. Далее антиген начинает контактировать с клоном, благодаря чему происходит стимуляция выработки антител. Контакт антигена с клоном клетки выполняется в избирательном порядке. Такая теория определяет функционирование всего иммунитета, который способен определять и распознавать огромнейшее число чужеродных элементов – антигенов. То есть, организм человека должен синтезировать тысячи и даже сотни тысяч различных молекул антител с соответствующими распознающими зонами.
Если говорить об этой же теории более простым языком, получается, что лимфоциты, выступающие в роли иммунных клеток организма, способны однажды изменить свой генотип, настраиваясь, отвечая и противодействуя какому-то одному чужеродному веществу, которым выступает обычно часть микроба или вируса. То есть, антиген. Происходит это только один раз, чаще всего у зародыша, и совершенно случайно, при том, до того, как клетка встретится с этим чужеродным элементом. Затем, когда контакта с антигенами уже не избежать, происходит селекция, то есть, отбор клеток, которые смогут противостоять микробам и защищать организм от вирусов. Помимо отбора таких клеток, происходит их интенсивное и масштабное размножение. Клетки, образовавшиеся в процессе размножения одного лимфоцита, называются клонами.
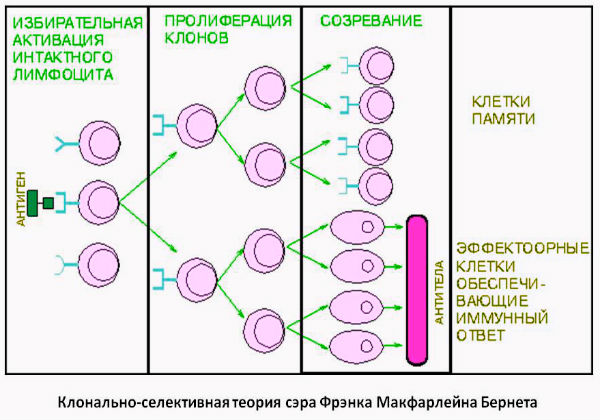
Главные принципы клонально-селекционной теории
Бернетом были приведены и доказаны следующие утверждения:
- В организме человека еще до первого контакта с антигенами уже существуют лимфоциты и антитела с нужной специфичностью;
- На поверхности лимфоцитов, принимающих участие в работе иммунной системы, расположены рецепторы антигенспецифического действия. При этом, если речь идет о B-лимфоцитах, в роли данных рецепторов выступают молекулы такой же специфичности, что и антитела, продуцируемые и секретируемые лимфоцитами;
- На поверхности лимфоцита расположены рецепторы исключительно одной специфичности;
- Лимфоциты, взаимодействующие с чужеродным элементом (антигеном), подвергаются нескольким этапам пролиферации. Также происходит масштабное клонирование плазматических клеток.

Подводим итоги
Клонально-селекционная теория иммунитета, представленная Бернетом в 1957 году, сыграла значимую роль уже в современных работах, касающихся функционирования иммунной системы человека. Некоторые ученые даже утверждают, что все учения и работы об иммунитете делятся на «до» и «после» возникновения и подтверждения клонально-селекционной теории. Позже были проведены сотни исследований на иммунологическую тему, в результате чего были выявлены различные классы клеток и их роль в противостоянии иммунитета вредоносным микробам, однако основные принципы теории Бернета до сих пор актуальны, справедливы и правдивы.
Видео по теме:
Источник
CD8+T-лимфоциты так же, как и другие клетки системы иммунитета различных популяций и субпопуляций, гетерогенны по своему составу.
Такая гетерогенность подтверждается наличием клонов цитотоксических лимфоцитов (ЦТЛ), различающихся по ряду параметров, несмотря на то что фенотипические характеристики клеток отдельных клонов ЦТЛ еще окончательно не определены.
Еще в конце 1980-х годов S. Rosenberg и сотр. показали, что в процессе индукции активности ЦТЛ появляются два типа цитотоксических лимфоцитов, каждый из которых может представлять ЦТЛ на отдельных этапах дифференцировки.
Клоны цитотоксических лимфоцитов по различным критериям
Дальнейшие исследования подтвердили возможность выделения различных клонов ЦТЛ по отдельным критериям.
Одним из таких критериев является способность к секреции цитокинов, в результате чего цитотоксические лимфоциты распределяются на две субпопуляции — Tcl и Тс2. Этот принцип распределения ЦТЛ имеет определенные ассоциации с разделением СD4+Т-лимфоцитов на Тh1 и Th2, в связи с чем некоторые авторы Тс1 определяют как Th1-подобные, а Тс2 — как Тh2-подобные.
Поэтому не случайно Tcl характеризуются отдельными исследователями как Thl/Tcl фенотип и экспансия клеток этого фенотипа, по их мнению, является оптимальной для регрессии опухоли. Клетки клона Tcl продуцируют IFNy, IL-2, а клетки Тс2 секретируют IL-4, IL-5, IL-10.
При различиях в синтезе цитокинов оба клона обладают общими функциями, включая перфорин- и Fas-зависимую цитотоксичность, а также способность к индукции гиперчувствительности замедленного типа (ГЗТ), при различиях в интенсивности инфильтрации этими клетками участка развития ГЗТ — инфильтрация Тс2 выражена в меньшей степени (данные получены при введении аллоспецифических Tcl и Тс2 мышам).
Описаны клоны ЦТЛ с различным уровнем экспрессии антигена CD8 — димерный гликопротеин (гетеродимер этого белка экспрессируется цитотоксическими лимфоцитами, а гомодимер — естественные киллеры (ЕК)). Изучение цитотоксической активности клеток этих клонов и продукции цитокинов (IFNy, IL-4) показало, что клетки клона с высоким уровнем экспрессии CD8 обладали выраженной цитотоксичностью, продуцировали IFNy и не продуцировали IL-4; клетки другого клона (низкий уровень экспрессии) продуцировали IFNy и IL-4 и их цитотоксичность была незначительной.
На основании этих данных авторы пришли к заключению, что IL-4 усиливает развитие ЦТЛ, которые характеризуются слабой цитотоксичностью. Эти данные представляют большой интерес в свете понимания неоднозначной роли интерлейкинов в функционировании СD8+Т-лимфоцитов и соответственно их роли в опухолевом процессе.
Одним из критериев распределения ЦТЛ на клоны явились и различия в распознавании отдельных опухолевых клеток. Например, было показано, что большинство Т-клеточных клонов проявляют специфический лизис в отношении аутологичных опухолевых клеток и не распознают клетки свежевыделенных опухолей, которые экспрессируют пептид MART-1 (27-35), представляемый молекулами HLA-A2. При этом оказалось, что опухолеспецифические цитотоксические лимфоциты не лизировали аутологичные клетки линий меланомы и лизировали свежевыделенные опухолевые клетки.
Сравнительным анализом клеток, инфильтрирующих опухоль и обнаруженных в циркуляции с учетом их способности к лизису различных опухолевых клеток, авторы установили, что иммунологический ответ в отношении клеток, представленных отдельными линиями, не отражает иммунологический ответ in situ.
При исследовании клеток опухоли, индуцированной ультрафиолетовым облучением, выявлено, что отдельные клоны ЦТЛ способны распознавать только один из антигенов, который экспрессирует клетка-мишень, что и привело авторов к мысли о существовании различных клонов ЦТЛ.
Отдельные клоны цитотоксических лимфоцитов выделены и по способности экспрессировать FasL в зависимости от особенностей стимулов. Такой принцип позволил выделить клон ЦТЛ — К135С20, клетки которого экспрессируют FasL в результате перераспределения TCR под влиянием анти-СD3-антител или стимуляции форболмеристат-индометацином, а также другой клон — ВМ3.3, FasL которых появлялся только после перераспределения TCR; в последнем случае отсутствие способности к экспрессии FasL коррелировало с дефектом экспрессии классической формы протеинкиназы.
Существование различных клонов ЦТЛ показано и на уровне наивных клеток. В частности, новые данные об изучении наивных клеток памяти цитотоксических лимфоцитов свидетельствуют о наличии четырех клонов, различающихся по способности пролиферировать и дифференцироваться in vivo и in vitro.
Эти клоны следующие:
1) CCR7+CD45RA+ (наивные клетки);
2) ТСМ, CCR7+CD45RA- (central памяти);
3) ТЕМ, CCR7-CD45RA-(эффекторные клетки памяти);
4) TEMRA, CCR7+CD45RA+(CCD45RA+-эффекторные клетки памяти).
В общей субпопуляции наивных клеток памяти можно выделить два фенотипа с учетом экспрессии ко-стимулирующей молекулы CD28 и CDllb: CD8+CD28+CDllb- и CD8+CD28 CDllb+. Клетки, не экспрессирующие молекулы CD28, могут продуцировать IFNy, содержать перфорин и проявлять высокую цитотоксичность, в то время как клетки, не экспрессирующие CDllb, продуцируют IL-2 и могут пролиферировать в ответ на действие митогена. Фенотипические и функциональные свойства клеток этих клонов предполагают, что они представлены промежуточными фенотипами процесса дифференцировки ЦТЛ и что экспрессия CDllb может отличаться при сравнении клеток памяти и эффекторных клеток СD8+СD28+Т-лимфоцитов человека.
Еще один вариант гетерогенности ЦТЛ проявляется в различии экспрессии ингибиторных рецепторов, которые, как известно, специфически взаимодействуют с молекулами I класса ГКГ; такая гетерогенность предполагает и различную роль этих рецепторов в биологии Т-клеток.
Наконец, получена информация, что небольшая часть активированных СD8+Т-лимфоцитов (бластные формы) может модулировать фенотип гепатоцитов.
Приведенные данные неоспоримо свидетельствуют, что цитотоксические лимфоциты является гетерогенной субпопуляцией, и есть основания полагать, что перечень критериев, по которым могут быть выделены отдельные клоны ЦТЛ, со временем увеличится.
Привлечение внимания к существованию различных клонов ЦТЛ представляется важным не только с позиций фундаментальной значимости этого факта, но и как еще одна иллюстрация чрезвычайной сложности интерпретации результатов клинического изучения СD8+Т-лимфоцитов.
Цитотоксичность CD8+T-лимфоцитов и ее механизмы
После констатации способности некоторых субпопуляций лимфоцитов повреждать клетки-мишени стал вопрос о механизмах этого повреждающего действия. Результаты первых исследований привели к выводу, что для осуществления цитотоксического действия лимфоциты используют комплемент.
Дальнейшее изучение комплементзависимых повреждений клеточной мембраны (модель антителозависимого лизиса эритроцитов) показало, что в реализации клеточной цитотоксичности принимают участие комплементподобные молекулы, известные как перфорины и имеющие значительную гомологию с литическим компонентом комплемента. Следует отметить, что в отдельных случаях перфоринзависимый лизис гомологичных клеток может происходить и с участием комплемента.
По мере изучения роли перфорина в клеточной цитотоксичности стало очевидным, что лизис клеток мишеней, в частности опухолевых, может осуществляться без дегрануляции и выделения содержимого гранул. Такой вывод был сделан еще в 1987 г. на основании изучения сериновых протеаз, которые так же, как и перфорин, находятся в гранулах. Отсутствие выделения сериновых протеаз при способности лимфоцитов проявлять цитотоксическое действие свидетельствовало об отсутствии дегрануляции.
Однако несмотря на то что лизис, обусловленный дегрануляцией, приводит к быстрому накоплению свободного Са2+ и повышению активности фосфатаз, получены доказательства возможности лизиса и без участия Са2+ — кальцийнезависимый путь.
В результате накопления соответствующих фактов было сделано заключение, что одни и те же эффекторные клетки используют различные механизмы цитолиза. В настоящее время известно несколько систем, с помощью которых осуществляется лизис клеток-мишеней.
Бережная Н.М., Чехун В.Ф.
Опубликовал Константин Моканов
Источник