Кариотипирование методом культивирования лимфоцитов
[16-001]
Исследование кариотипа (количественные и структурные аномалии хромосом) по лимфоцитам периферической крови (1 человек)
6290 руб.
Цитогенетическое исследование – кариотипирование – является основным методом диагностики хромосомных нарушений и проводится в целях выявления нарушений количества и структуры хромосом. Используется для пренатальной диагностики.
Синонимы русские
- Хромосомные риски
- Кариотипирование супругов
- Определение хромосомного набора
Синонимы английские
- Karyotyping
- Karyotyping Chromosome Analysis
Метод исследования
Световая микроскопия.
Какой биоматериал можно использовать для исследования?
Венозную кровь.
Как правильно подготовиться к исследованию?
- Исследование проводится в состоянии сытости, не рекомендуется сдавать кровь на данное исследование натощак.
- Исключить (по согласованию с врачом) прием антибактериальных и химиотерапевтических препаратов в течение 14 дней до исследования.
- Исследование рекомендуется проводить не ранее чем через 2 недели после перенесенных инфекционных/острых воспалительных заболеваний.
Общая информация об исследовании
Кариотипирование – цитогенетическое исследование, изучение хромосомного набора человека, позволяющее обнаружить отклонения в структуре и числе хромосом. Оно помогает выявить нарушения хромосом, вероятно, не влияющие на здоровье человека, но тем не менее важные для планирования будущей беременности и для здоровья будущего ребенка (патологии плода, аномалии развития).
Кариотип – это полный хромосомный набор клетки человека. В норме он состоит из 46 хромосом, из них 44 аутосомы (22 пары), имеющих одинаковое строение и в мужском, и в женском организме, и одна пара половых хромосом (XY у мужчин и XX у женщин). Каждая хромосома несет гены, ответственные за наследственность. Кариотип 46, ХХ – соответствует нормальному женскому кариотипу, а кариотип 46, XY – это нормальный мужской кариотип. Кариотип остается неизменным в течение всей жизни.
Нарушения хромосомного набора могут являться причиной наследственной патологии, бесплодия, невынашивания беременности, рождения ребенка с различными пороками развития.
Для цитогенетического исследования хромосом чаще всего используют препараты кратковременной культуры крови, реже клетки костного мозга и культуры фибробластов.
Кариотипирование культуры лимфоцитов периферической крови человека – сложное многоступенчатое цитогенетическое исследование, проводится, когда клетки входят в фазу митоза – непрямого деления с тождественным распределением генетического материала между дочерними клетками. Оно включает в себя следующие этапы:
- Постановка культуры лимфоцитов, рост клеток в течение 72 часов. (Рост клеток может быть осложнен различными факторами: наличие инфекционных, хронических, простудных заболеваний; прием лекарственных препаратов; диета; прием алкоголя и т. п. Все эти факторы необходимо исключить перед сдачей анализов).
- Обработка культур лимфоцитов: колхицинизация, гипотонизация, фиксация.
- Приготовление препаратов хромосом на стекле.
- Монохромное и дифференциальное окрашивание препарата.
- Анализ препаратов (подсчитывается общее количество хромосом, проводится оценка структуры каждой хромосомы). Анализ хромосом осуществляется на разрешении в 400-500 полос (бэндов).
Различают несколько видов нарушений структуры хромосом:
- трисомии – добавление еще одной хромосомы к паре;
- моносомии – утрата одной хромосомы из пары;
- делеции – утрата участка хромосомы;
- дупликации – повторение определенного участка хромосомы;
- инверсии – поворот участка хромосомы на 180 градусов;
- транслокации – перенос участков хромосомы в новое положение.
Хромосомные нарушенияразличаются также по принципу регулярности. Регулярные мутации присутствуют при делении каждой клетки или большинства клеток. Они проявляются в момент зачатия плода либо в первые несколько дней беременности. Нерегулярные аберрации появляются в результате негативного воздействия радиации, химических средств и т.д.
Нарушение расхождения хромосом может произойти во время клеточного деления (мейоза). Если такое нарушение происходит в процессе образования сперматозоидов или яйцеклеток, то в половой клетке появляется лишняя хромосома, которая при зачатии будет передана ребенку. В результате она будет присутствовать во всех клетках организма ребенка. Примером трисомии может служить синдром Дауна (лишняя 21-я хромосома) или синдром Патау (трисомия 13-й хромосомы). Также нарушение расхождения хромосом может произойти при первых делениях оплодотворенной яйцеклетки. Например, утрата Х-хромосомы приводит к развитию Х0-синдрома, или синдрома Шерешевского – Тернера. Аномалии, связанные с нарушением расхождения хромосом, встречаются не так часто, поэтому вероятность их повторения в одной и той же семье достаточно мала.
Структурные же нарушения хромосом передаются по наследству, при этом степень семейного риска и дальнейшая передача дефекта от поколения к поколению становится значительно высокой.
Кариотипирование также рекомендуют проводить в тех семьях, где есть высокая вероятность рождения ребенка с болезнью, сцепленной с Х-хромосомой.
Когда назначается исследование?
Показания для кариотипирования супружеских пар:
- мужское бесплодие: тяжелая олигозооспермия, необструктивная азооспермия, тератозооспермия;
- первичная аменорея;
- привычное невынашивание беременности в первом триместре (2 и более выкидышей);
- наличие выкидышей неясного генеза в анамнезе;
- случаи мертворождений в анамнезе;
- случаи ранней младенческой смертности в анамнезе;
- рождение детей с хромосомной аномалией (например, синдромом Дауна);
- рождение детей с множественными врождёнными пороками развития (МВПР);
- планирование ЭКО;
- неудачные попытки ЭКО;
- прогноз здоровья будущего ребенка.
Показания для кариотипирования детей:
- наличие врождённых пороков развития;
- умственная отсталость;
- задержка психомоторного развития;
- задержка психо-речевого развития в сочетании с микроаномалиями;
- нарушение или задержка полового развития;
- задержка роста;
- аномалии пола.
Что означают результаты?
Для мужчин нормальным считается кариотип 46,XY. Это означает, что определено 46 нормальных хромосом, в том числе X и Y хромосома.
Для женщин нормальным считается кариотип 46,XX. Это означает, что определено 46 нормальных хромосом, в том числе две X хромосомы.
В случае выявления патологического кариотипа, необходима консультация медицинского генетика по результатам исследования для правильной его интерпретации.
Литература
- Reddy UM, Page GP, Saade GR, et al. Karyotype versus microarray testing for genetic abnormalities after stillbirth. N Engl J Med 2012;367:2185-93.
- Murphy KM, Cohen JS, Goodrich A, Long PP, Griffin. CA 2007. Constitutional duplication of a region of chromosome Yp encoding AMELY, PRKY, and TBL1Y: implications for chromosome analysis. J Mol Diagn, 9: 408-413.
- ISCN (2013): An International System for Human Cytogenetic Nomenclature; Karger AG, Basel, 2013/
- ISCN (2016): An International System for Human Cytogenetic Nomenclature; S. Karger AG, Basel, 2016/
- ISCN Symbols and Abbreviated Terms//Coriell Institute for Medical Research/
Источник
Цитогенетические исследования в гематологии: окрашивание хромосом, метод FISH
Цитогенетическое исследование — это микроскопический анализ хромосом, результаты которого весьма важны для постановки диагноза, классификации, лечения и научного исследования заболеваний системы крови, прежде всего — онкогематологических. Значение цитогенетических методов для диагноза и лечения определяется доступностью опухолевых клеток для кариотипирования и их гетерогенностью, а с научной точки зрения — возможностью изучения изменений в структуре и функции генетических локусов, ассоциированных со злокачественной трансформацией.
Морфология хромосом сильно варьирует во время клеточного цикла. Для микроскопического анализа хромосомы должны быть визуализированы как дискретные структуры. Наилучшим образом это достигается на стадии прометафазы митоза, когда каждая хромосома видна как две идентичные хроматиды, и особенно на стадии метафазы, когда хромосомы максимально конденсированы и располагаются в одной плоскости в центре клетки отдельно одна от другой.
Нормальные клетки человека содержат 22 пары аутосом и одну пару половых хромосом: две Х-хромосомы у женщин и по одной копии половых хромосом (X и Y) у мужчин.
Для цитогенетического анализа лейкозов, миелодиспластических синдромов и хронических миелопролиферативных заболеваний исследуют клетки костного мозга. При невозможности их получения может быть исследована кровь (если она содержит бласты). Цитогенетический анализ лимфом выполняется в клетках ткани лимфатического узла. Культивирование клеток из опухоли повышает митотический индекс (пропорцию клеток, находящихся в фазе митоза) и способствует пролиферации злокачественных клеток.
Сравнительное кариотипирование нормальных клеток проводят в Т-лимфоцитах периферической крови, которые предварительно культивируют в среде с митогеном растительного происхождения — фитогемагглютинином.
Окрашивание хромосом в гематологии
В конце 1960-х годов была разработана методология дифференциального окрашивания метафазных хромосом, а в 1971 г. создана номенклатура хромосомных сегментов, позволяющая точно описывать хромосомные аномалии. Позднее были внедрены методики окрашивания менее конденсированных и, соответственно, более длинных профазных и прометафазных хромосом, которые обладают более высоким разрешением, так как позволяют визуализацию 500-2000 сегментов (метафазное окрашивание визуализирует только 300 сегментов).
Достаточно большое количество профазных и прометафазных клеток для анализа получают путем синхронизации клеточного цикла, культивируя клетки в среде, содержащей антиметаболит (например, метотрексат), который ингибирует синтез ДНК. Подавление синтеза ДНК останавливает клеточный цикл в интерфазе. Затем клетки переносят в среду без метотрексата, обогащенную тимидином, где они одновременно входят в фазу митоза. Обработка клеточной культуры колхицином останавливает митоз одновременно во всех клетках на стадии профазы или прометафазы.
Первая стойкая хромосомная аномалия при злокачественной опухоли человека была выявлена в 1960 г. у больных хроническим миелолейкозом и получила название филадельфийской хромосомы (Ph), по имени города, в котором было сделано это открытие. Применение технологии хромосомного окрашивания позволило выявить множество хромосомных аномалий, большая часть которых встречается при онкогематологических заболеваниях. Некоторые красители окрашивают различные участки хромосом с вариабельной интенсивностью в зависимости от структуры хроматина в этих участках, их нуклеотидного и белкового состава.
В результате такого окрашивания получают уникальный паттерн чередования светлых и темных поперечных полос, специфичный для каждой хромосомы.
В настоящее время существуют несколько видов дифференциального окрашивания хромосом. При Q-окрашивании акрихин-ипритом (quinacrine) или акрихиндигидрохлоридом выявляется особый тип флюоресценции каждой хромосомы с образованием Q-исчерченности (Q-banding) — поперечных флюоресцентных полос, называемых Q-полосами (Q.-bands). Это позволяет идентифицировать отдельные хромосомы. Анализ Q-полос выполняют с помощью флюоресцентного микроскопа.

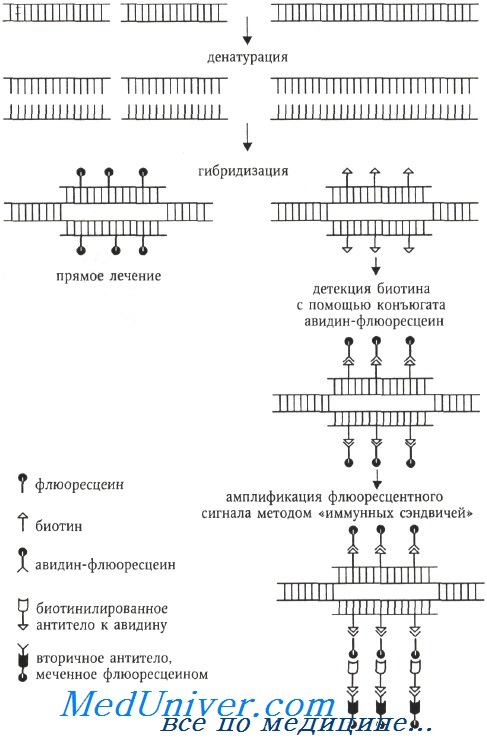
Схема анализа ДНК методом FISH
При окрашивании по Гимзе (G-banding) хромосомы приобретают вид серии темных и светлых полос или бэндов (bands). G-окрашивание применяется чаще, чем Q-окрашивание, так как анализ выполняется с помощью светового микроскопа, а G-полосы, в отличие от Q-полос, не выцветают со временем. Наиболее широко применяется методика, называемая GTG-окрашиванием (G bands by trypsin using Giemsa), с предварительной обработкой трипсином.
R-бэндинг (обработка хромосом горячим спиртовым раствором перед окрашиванием по Гимзе) выявляет полосы, которые обратны G-полосам и называются R-полосами (reverse of G bands).
Помимо Q-, G- и R-окрашивания, позволяющих выявлять полосы вдоль всей длины хромосомы, существуют методики, специализированные для исследования отдельных хромосомных структур, в том числе конститутивного гетерохроматина (С-окрашивание — от англ. constitutive), теломерного района (Т-окрашивание) и района ядрышкового организатора (NOR-окрашивание — от англ. nucleolus organizing region). Размеры и положение С-полос уникальны для каждой хромосомы, но преимущественно они включают центромерныи район и используются при исследовании хромосомных транслокаций, вовлекающих центромерные районы хромосом.
Цитогенетический анализ опухолевых клеток затруднен в связи с неясной морфологией хромосом и слабой различимостью полос. Если в исследование взяты наиболее удобные для анализа метафазные пластинки, образец может быть ошибочно охарактеризован как цитогенетически нормальный.
С развитием методов рекомбинантной ДНК стало возможным использование гибридизации in situ для определения местоположения на хромосомах или в клеточном ядре любой ДНК- и РНК-последовательности. С ее помощью можно изучать и диагностировать онкологические и наследственные генетические болезни. Молекулярная гибридизация in situ является важным инструментом цитогенетических исследований, позволяет выявлять хромосомные перестройки, идентифицировать маркерные хромосомы, проводить быстрое кариотипирование клеточных линий. Важно, что подобный анализ можно проводить не только на метафазных хромосомах, но и на интерфазных ядрах.
Разрешающая способность «интерфазной цитогенетики» на два порядка выше, чем классической цитогенетики.
Несмотря на многоцелевое использование молекулярной гибридизации ДНК-ДНК (РНК) in situ, все модификации метода выполняются в соответствии с общими принципами. Существуют несколько вариантов, которые включают в себя несколько этапов: подготовка и мечение ДНК (РНК)-зонда, приготовление препаратов хромосом, собственно гибридизация, детекция гибридных молекул.
В 1980-х годах цитогенетическая методология обогатилась молекулярно-цитогенетическим методом, называемым флюоресцентной гибридизацией in situ (fluorescence in situ hybridization, FISH), который вскоре стал наиболее популярным. Суть этого метода заключается в гибридизации ДНК-зондов к специфическим последовательностям ДНК, меченных флюорохромами, с метафазными или интерфазными хромосомами, которые визуализируются флюоресцентной микроскопией. Определение нуклеотидной последовательности методом FISH выполняется непрямым способом, путем гибридизации синтетического олигонуклеотида (зонда) с анализируемой ДНК (называемой также матричной ДНК или ДНК-мишенью).
Если зонд синтезирован с включением флюоресцентных или антигенных молекул, которые распознаются флюоресцирующими антителами, становится возможной визуализация относительного положения зонда на анализируемой ДНК.
Флюорохром может быть связан с ДНК ковалентно (прямое мечение) или посредством иммуноцитохимических реакций, когда ДНК-зонд метят гаптеном (биотин, дигоксигенин), а флюорохром связан с алкалоидом авидином (стрептавидином), обладающим сильным сродством к биотину (или с антителами против биотина или дигоксигенина). При использовании гаптенов возможна амплификация флюоресцентного сигнала с помощью биотинилированных антител к авидину и вторичных антител, специфичных предыдущему слою антител и окрашенных флюорохромом.
Для амплификации флюоресцентного сигнала применяется метод «иммунных сэндвичей». Например, на препарат, изображенный на схеме, наносят биотинилированные антитела к авидину, а затем снова комплекс авидин-флюоресцеин. При необходимости цикл может быть повторен. Антитела в свою очередь выявляются с помощью ферментативного (например, авидинпероксидазы) или флюоресцентного детектора.
Метод FISH предназначен для выявления:
1) гибридных клеток;
2) транслокаций и других, в том числе числовых, хромосомных аномалий;
3) меченых хромосом в интерфазных и метафазных клетках.
Высококонтрастная флюоресцентная гибридизация достигается благодаря использованию флюоресцентных красителей разного цвета. С помощью двуцветной FISH выявляются тонкие структурные аномалии, например хромосомные транслокации, в том числе и неразличимые при дифференциальном окрашивании.
В настоящее время возможно выполнение многоцветной гибридизации in situ для одновременного окрашивания всех хромосом в сложном кариотипе с множественными числовыми и структурными аномалиями. Комбинация разных модифицирующих агентов и флюорохромных красителей позволяет одновременно выявлять несколько последовательностей ДНК в одном ядре (флюоресцеин дает зеленую флюоресценцию, техасский красный и родамин — красную, гидроксикумарин — голубую и т. д.). Сочетание пяти флюорохромов в разных пропорциях и компьютерный анализ изображений позволяет одновременно окрасить разным цветом все хромосомы и визуализировать 27 различных ДНК-зондов, которые служат уникальной меткой для каждой хромосомы. Эта методика называется многоцветной FISH (multicolor, или multiplex, fluorescence in situ hybridization, M-FISH).
Значение цитогенетических методов неодинаково при разных онкогематологических заболеваниях. Миелоидные клетки обычно легко кариотипируются при дифференциальном окрашивании, и FISH лишь подтверждает результаты рутинной цитогенетики. Лимфоидные клетки у больных хроническим лимфолейкозом и, особенно, множественной миеломой кариотипировать значительно сложнее из-за низкого уровня пролиферации (даже при использовании В-клеточных митогенов). В этом случае FISH демонстрирует в несколько раз большую частоту анеуплоидии, чем обычные цитогенетические методики.
Клиническое значение цитогенетических исследований
Диагноз. Потомство клетки с приобретенной цитогенетической аномалией может иметь пролиферативное преимущество и давать начало клону — клеточной популяции, происходящей от одной клетки-предшественницы. Обнаружение клональных хромосомных аномалий способствует постановке диагноза клонального поражения костного мозга. Например, цитогенетический анализ позволяет установить диагноз миелодиспластического синдрома у пациентов с умеренной цитопенией или при наличии в аспирате костного мозга минимально выраженных качественных нарушений гемопоэза.
Присутствие специфических хромосомных аномалий помогает выделить подгруппы пациентов, которым требуется специфическая терапия. Например, транслокация t(15;17)(q22;qll-21) подтверждает диагноз острого промиелоцитарного лейкоза (ОМЛ — МЗ), в комплексном лечении которого используется ретиноевая кислота.
Прогноз. Результаты цитогенетического анализа имеют не только диагностическое, но и прогностическое значение. Например, обнаружение множественных хромосомных аномалий у больных острыми лейкозами до начала лечения является прогностически неблагоприятным и служит основанием для выполнения трансплантации костного мозга или стволовых клеток периферической крови в первой полной ремиссии.
Контроль результатов лечения. Цитогенетический анализ костного мозга пациентов после проведенного лечения помогает контролировать степень элиминации опухолевого клона и, следовательно, полноту ремиссии. Выявление хромосомных аномалий, характерных для опухолевых клеток данного пациента, является ранним признаком, свидетельствующим о приближающемся рецидиве.
Цитогенетический анализ имеет большое значение в диагностике и лечении гематологических заболеваний, которое все возрастает по мере совершенствования методологии и накопления знаний об этиологической и патогенетической роли хромосомных аномалий в развитии этих болезней.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
– Также рекомендуем “Кариотипирование в гематологии. Классификация хромосом”
Оглавление темы “Методы исследования в гематологии”:
- Уровень железа в крови норме. Исследование обмена железа
- Осмотическая резистентность эритроцитов в норме. Биохимические исследования в гематологии
- Миелограмма в норме – цитология исследования костного мозга
- Гистологические исследования в гематологии. Показания к трепанобиопсии
- Цитогенетические исследования в гематологии: окрашивание хромосом, метод FISH
- Кариотипирование в гематологии. Классификация хромосом
- Хромосомные аномалии в гематологии – классификация
- Молекулярно-генетические исследования в гематологии – возможности
- Полимеразная цепная реакция (ПЦР) в гематологии – возможности
- Методы детекции точечных мутаций в гематологии – возможности
Источник