Какие лимфоузлы при раке эндометрия
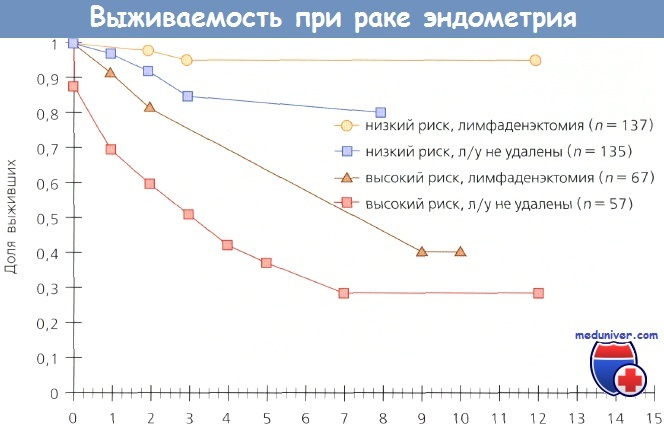
Метастазирование рака эндометрия в лимфоузлы и ее прогнозДлительное время абдоминальная гистерэктомия с придатками считалась стандартом лечения рака эндометрия (РЭ). По этой причине без внимания оставалась большая частота метастазирования в лимфоузлы. Несмотря на то что и первые, и более поздние публикации указывали на то, что у большого числа больных раком эндометрия (РЭ) даже с I стадией появятся метастазы в лимфоузлах, эти потенциальные очаги распространения опухоли в схемах лечения не учитывали. В 1973 г. Morrow и соавт. установили, что из 369 пациентокс I стадией рака эндометрия (РЭ) метастазы влимфоузлахтаза обнаружены у 39. В 1976 г. Creasman и соавт. привели примеры еще 140 больных, у 16 из которых выявлены метастазы в тазовых лимфоузлах. Эти данные уточняли по ходу появления новых случаев рака эндометрия (РЭ). В относительно большой группе пациенток с клинически установленной I стадией рака эндометрия (РЭ) почти у 10% были обнаружены метастазы в лимфоузлах таза. В исследовании Morrow и соавт. только 31 % больных с I стадией заболевания и метастазами в лимфоузлах пережили 5-летний рубеж, при том, что большинству из них была проведена послеоперационная ЛТ. Polish и соавт. опубликовали показатели выживаемости больных с микроскопическими метастазами в лимфоузлах, которым провели ЛТ как этап первичного лечения. 5-летняя выживаемость при подтвержденных хирургическим стадированием метастазах в лимфоузлах таза составила 67%, а в случаях поражения парааортальных узлов с метастазами или без таковых в лимфоузлах таза — 47 и 43% соответственно. В исследовании Creasman и соавт. у 102 больных для гистологической диагностики удаляли парааортальную жировую клетчатку, в результате чего в 10 (9,8 %) случаях выявили метастазы в этой области. Boronow и соавт. при дополнении и обновлении одного из первых в этом направлении исследований GOG обнаружили, что из 222 пациенток с I стадией рака эндометрия (РЭ) у 23 (10,4 %) выявлены метастазы в лимфоузлах таза. Из 156 больных, которым провели микроскопическую оценку парааортальных лимфоузлов, метастазы были выявлены у 16 (10,2 %).
DiSaia в ходе длительного наблюдения отметил рецидивы заболевания у 21 (10,5%) из 199 пациенток, у которых не было метастазов в лимфоузлах таза, и у 13(56 %) из 23, имевших метастатическое поражение этих узлов. При отсутствии метастазов в парааортальных узлах рецидивы наблюдались у 15 (11 %) из 140 больных, а при их поражении — у 10 (59 %) из 17. Creasman, анализируя данные GOG о 621 пациентке с I стадией РЭ, обнаружил, что в 144 (22%) случаях заболевание распространилось за пределы матки: в тазовые и парааортальные лимфоузлы, придатки матки, органы брюшной полости — и/или были обнаружены злокачественные клетки в смывах. Частота метастазирования в лимфоузлы у больных со II стадией рака эндометрия (РЭ) значительно выше, чем при 1 стадии заболевания. Morrow и соавт. привели данные о 85 пациентках: в 31 (36,5 %) случае выявлены метастазы в лимфоузлахтаза. В исследовании GOG 148 больным с клинически установленной II стадией РЭ провели хирургическое стадирование; у 66 процесс распространялся на шейку матки. Среди больных с поражением только желез эндоцервикса метастазы в тазовых лимфоузлах были обнаружены у 3 (17%) по сравнению с 35% пациенток с вовлечением стромы. Ни у одной больной с поражением только желез шейки матки метастазов в парааортальных лимфоузлах не было по сравнению с 23 % пациенток с вовлечением стромы. При наличии инвазии в строму шейки матки метастазы в тазовых и парааортальных лимфоузлах выявляли у 46 % больных. В годовом отчете FIGO приведены данные о 43, 103 и 121 пациентке с III стадией рака эндометрия (РЭ) и степенью дифференцировки G1, G2 и G3 соответственно. 5-летняя выживаемость составила 62, 61 и 47 % соответственно. Ben-Shachar и соавт. представили результаты лечения 349 больных, которых прооперировали по поводу рака эндометрия (РЭ). До операции у 52 % из них диагностированы высокодифференцированные опухоли (G1). Хирургическое стадирование ± парааортальная лимфаденэктомия были выполнены в 82 % случаев. После сравнения результатов пред- и послеоперационного гистологического исследования у 19 % пациенток оказалась более высокая степень дифференцировки (G2 или G3). Метастазы в лимфоузлах обнаружены у 3,9 % пациенток с высокодифференцированной аденокарциномой (G1), у 10,5% заболевание распространилось за пределы матки. Признаки высокого риска — инвазия, захватывающая более половины толщины миометрия, низкодифференцированные (G3) и неблагоприятные морфологические варианты опухоли, переход процесса на шейку матки — были выявлены у 26 % больных, у которых до операции диагностирован высокодифференцированный рак (G1). Результаты хирургического стадирования указали па необходимость проведения адъювантной терапии у 12 % пациенток и отказ от нее — у 17 %.
С 1988 г., когда эксперты FIGO перешли с клинического определения стадии рака эндометрия (РЭ) на хирургическое стадирование, возник вопрос о роли лимфаденэктомии при лечении стадии рака эндометрия (РЭ). Несет ли она только диагностическую функцию, что уже существенно, или служит и лечебной процедурой? В первоначальных исследованиях выполняли селективную лимфаденэктомию — удаление подозрительных на наличие метастазов лимфоузлов. Все большее количество данных свидетельствует о том, что необходимо выполнять полную лимфаденэктомию. Onda и соавт. провели тазовые и парааортальные лимфаденэктомии у 173 больных при 1—III стадии стадии рака эндометрия (РЭ), удалив в среднем 38 тазовых и 29 парааортальных узлов. Метастазы в лимфоузлах обнаружены у 30 (17%) пациенток: у 10 — только в тазовых лимфоузлах (группа Т), у 2 — только в парааортальных и у 18 — в тех и других (последние 20 больных вошли в группу А). В группе Т провели ЛТ обычными полями, в группе Л — расширенными и/или ПХТ. У 143 больпых без метастазов в лимфоузлах 5-летняя выживаемость составила 95 %, у 30 пациенток с метастазами в группе Т — 100 %, а в группе А — 75%. По мнению авторов, системная тазовая и парааортальная лимфаденэктомия, а также последующие ЛТ и XT, назначенные на основании результатов гистологического исследования лимфоузлов, позволили улучшит!) выживаемость больных. Mohan и соавт. проанализировали результаты лечения 159 больных с I стадией заболевания,которым была выполнена тазовая лимфаденэктомия е последующей брахитерапией (контактной лучевой терапией). Общая 15-летняя выживаемость составила 92%, частота рецидивирования — 4,4%; во всех случаях рецидивы представляли собой отдаленные метастазы. В публикации под редакцией Podratz и соавт. рассмотрены 4 исследования, включая и вышеназванное, в которых лимфаденэктомию выполняли самым тщательным образом больным в группах умеренного и высокого риска, а послеоперационную ЛТ не назначали. Среди 305 больных диагностировано 20 (6,6%) рецидивов заболевания; только в 5 из них рецидивы были местными/регионарными, причем 4 локализовались во влагалище. Этим 4 пациенткам не провели послеоперационную брахитерапию, но в последующем излечение было достигнуто с помощью ЛТ.
В ретроспективном исследовании, выполненном в клинике Мауо, 137 больных с высоким риском поражения лимфоузлов метастазами, которым была выполнена парааортальная лимфаденэктомия (ПЛА+), сравнили с пациентками, которым этот этап не выполняли (ПЛА—). В группе ПЛА+ 5-летняя выживаемость составляла 85 % по сравнению с 77 % в группе ПЛА—. У 51 больной с метастазами в тазовых или парааортальных лимфоузлах показатель выживаемости равнялся 77 % в группе ПЛА+ по сравнению с 42 % в группе ПЛА—. Kilgore и соавт., анализируя результаты лечения 649 пациенток, пришли к выводу о том, что выживаемость перенесших тазовую и парааортальную лимфаденэктомию значительно лучше, чем у пациенток с сохраненными лимфоузлами. Кроме того, выживаемость после лимфаденэктомии лучше, чем без нее, но с послеоперационной ЛТ. В небольшом исследовании, включавшем 41 пациентку с РЭ III стадии, Bristow и соавт. установили, что безрецидивная выживаемость больных значительно возрастает при полном удалении всех макроскопически измененных лимфоузлов по сравнению со случаями, когда во время операции не были удалены явно метастатические узлы (37,5 vs 8,8 мес; р = 0,006). В исследовании Havrilesky у 91 больной была установлена III стадия РЭ, причем у 39 обнаружены микрометастазы в нормальных по размеру лимфоузлах и у 52 — увеличенные метастатические узлы. После операции 92 % этих больных получали адъювантную терапию; ЛТ проведена 85% пациенток. У 39 пациенток с микроскопическими метастазами в лимфоузлах 5-летняя выживаемость равнялась 58 %, а у 41 больной с полным удалением макроскопически увеличенных метастатических узлов — 48% и всего 22 % у 11 женщин с неудаленными лимфоузлами. Авторы пришли к выводу, что эти данные свидетельствуют о терапевтической эффективности лимфаденэктомии. Schink и соавт. определили размер опухолей у 91 больной с I стадией РЭ. Частота метастазов в лимфоузлах при размере опухоли менее 2 см составляла всего 5,7%, более 2 см в диаметре — 21 %, а в случаях поражения всего эндометрия этот показатель возрастал до 40 %. У пациенток с опухолью менее 2 см и инвазией менее чем на 1/2 толщины миометрия метастазов в лимфоузлах не было. На основании многофакторного анализа авторы установили, что размер опухоли — независимый прогностический фактор.
– Также рекомендуем “Метастазирование рака эндометрия в придатки матки и ее прогноз” Оглавление темы “Аденокарцинома матки”:
|
Источник
Рекомендации по лимфаденэктомии при раке эндометрия
Нет сомнений в том, что хирургическое определение стадии позволяет более точно идентифицировать истинное распространение заболевания. Среди пациенток с клинической I стадией рака эндометрия (РЭ) примерно у 25% выявляют распространение заболевания за пределы органа; среди пациенток с предполагаемой II стадией не менее чем у 75 % будет установлена либо более низкая стадия, либо выход процесса за пределы матки.
Важно не только подобрать адекватное лечение (например, с учетом поражения лимфоузлов), но и предотвратить необоснованную терапию. Высказывалось мнение о возможном увеличении осложнений, связанных с более широким использованием хирургического стадирования. По данным Moore и Larson и соавт., уровень послеоперационных осложнений после хирургических вмешательств с лимфаденэктомией и без нее был одинаковым.
На примере 80 пациенток Fanning и Firestein проанализировали объем кровопотери и осложнения, обусловленные лимфаденэктомией. Среднее количество удаленных тазовых лимфоузлов равнялось 21, парааортальных — 7. Средняя продолжительность лимфаденэктомии составляла 24 мин, средний объем кровопотери — 25 мл. Процент осложнений был низким и был обусловлен абдоминальной гистерэктомией с двусторонней аднексэктомией.
Childers и соавт. рекомендовали лапароскопический метод удаления лимфоузлов в сочетании с влагалищной гистерэктомией и двусторонней аднексэктомией. В руках специалистов, владеющих данной хирургической техникой, исходы заболевания сопоставимы с результатами после стандартных абдоминальных операций.

Имеются некоторые преимущества предлагаемого метода: короткий срок госпитализации и быстрая реабилитация после операции. Приближается к завершению крупное исследование GOG, сравнивающее лапароскопические и абдоминальные операции при раке эндометрия (РЭ).
Вопрос о влиянии метода хирургического стадирования рака эндометрия (РЭ) на выживаемость постоянно в поле зрения исследователей, т. к. информация об истинной распространенности заболевания существенным образом влияет па исход отдельных случаев. Kilgore и соавт. (шт. Алабама) опубликовали данные, свидетельствующие о том, что лимфаденэктомия не только обеспечивает терапевтический эффект, но и улучшает выживаемость больных раком эндометрия (РЭ).
Они обследовали и лечили 649 больных раком эндометрия (РЭ); у 212 пациенток выполнили полную тазовую лимфаденэктомию, у 205 — селективную, у 208 — лимфоузлы не удаляли. Выживаемость больных, которым выполнили полную тазовую лимфаденэктомию, была выше, чем у пациенток, которым эта операция не проводилась (р = 0,0002). Выживаемость больных из группы низкого риска (опухоль ограничена маткой) после лимфаденэктомии была более высокой по сравнению с теми, кому лимфаденэктомия не проведена (р = 0,026).
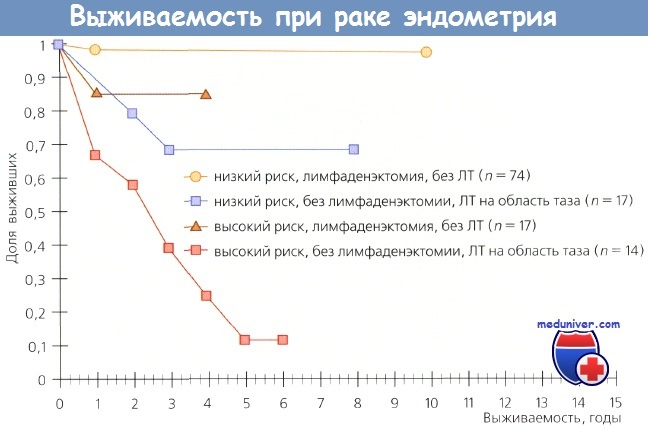
Больные раком эндометрия (РЭ) из группы высокого риска (распространение заболевания на шейку, придатки и серозную оболочку матки, положительные результаты смывов из брюшной полости), которым была выполнена лимфаденэктомия, также имели более высокий показатель выживаемости (р = 0,0006). Даже при оценке отдельных подгрупп больных терапевтическое преимущество лимфаденэктомии было очевидным.
Выживаемость больных из групп как низкого, так и высокого риска, которым была выполнена лимфаденэктомия, но они не получили послеоперационную ЛТ, была выше по сравнению с выживаемостью пациенток из тех же групп, которым лимфаденэктомию не выполнили, но провели облучение. Авторы не сомневаются в терапевтической ценности лимфаденэктомии и отмечают, что объем этого вмешательства зависит от количества пораженных метастазами лимфоузлов.
По данным Chung, при раке эндометрия (РЭ) существует взаимосвязь между ретроперитонеальным рецидивом и состоянием лимфоузлов на момент первичного хирургического вмешательства. Если они поражены метастазами, то забрюшинный рецидив не представляется необычным. И наоборот, рецидивы в забрюшинном пространстве не возникают, если и тазовые, и парааортальные лимфоузлы интактные.
По данным многофакторного анализа, только наличие метастазов в ретроперитонеальных лимфоузлах было значимым для прогноза выживаемости.
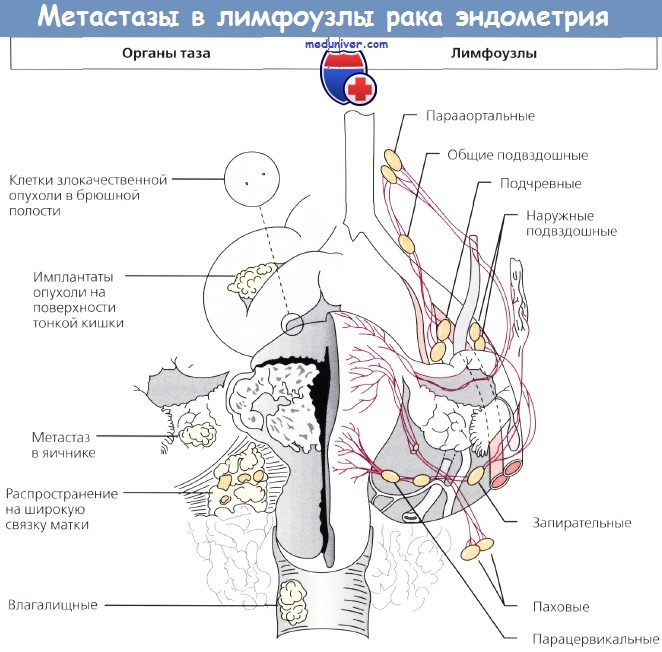
– Также рекомендуем “Прогестины в лечении рецидива рака эндометрия и их эффективность”
Оглавление темы “Рак эндометрия”:
- Рекомендации по хирургическому стадированию рака эндометрия
- Рекомендации по лучевой терапии рака эндометрия
- Рекомендации по удалению матки (гистерэктомии) при раке эндометрия
- Рекомендации по химиотерапии рака эндометрия
- Рекомендации по лимфаденэктомии при раке эндометрия
- Прогестины в лечении рецидива рака эндометрия и их эффективность
- Тамоксифен в лечении рецидива рака эндометрия и его эффективность
- Гонадотропин-рилизинг гормон (ГнРГ) в лечении рецидива рака эндометрия и его эффективность
- Химиотерапия рецидива рака эндометрия и ее эффективность
- Лечение рака эндометрия при первично-множественных опухолях
Источник
Пути метастазирования опухоли при раке шейки матки и тела матки. Лимфатическая система яичников.
Клинические наблюдения показывают, что чаше всего метастазы при раке шейки матки обнаруживаются в следующих шести группах лимфатических узлов, являющихся для шейки матки регионарными: околошеечных (парацервикальных), околоматочных (параметральных), запирательпых, внутренних подвздошных, наружных подвздошных и общих подвздошных. Значительно реже наблюдается метастазирова-ние рака шейки матки в околоаортальные и паховые лимфатические узлы. Перечисленные группы узлов, в свою очередь, могут быть подразделены на три подгруппы: первичная (околошеечные и околоматочные), промежуточная (наружные и внутренние подвздошные, запирательные) и вторичная подгруппа (общие подвздошные, околоаортальные и паховые лимфатические узлы).
Существует два основных пути лимфогенного метастазирования при раке шейки матки. Первый путь: от околошеечных и околоматочных узлов к наружным подвздошным и запирательным, а затем к околоаортальным и значительно реже — паховым лимфатическим узлам. Второй основной путь: от околошеечных и околоматочных узлов к внутренним подвздошным, а затем к общим подвздошным и околоаортальным лимфатическим узлам. Распространение раковых клеток может происходить как по одному из этих путей, так и по обоим, а также только с одной стороны или с обеих сторон одновременно (Papadia, 1958).
Общность лимфатической и венозной системы шейки матки и влагалища, а также тесный контакт между этими органами является анатомическим обоснованием нередкого распространения карциномы шейки матки на стенки влагалища.
Согласно клиническим данным, при раке шейки матки сначала поражаются внутренние подвздошные и подвздошные (общие и наружные), а затем околоаортальные лимфатические узлы; при раке тела матки в первую очередь поражаются околоаортальные и паховые лимфатические узлы; метастазирование при раке шейки матки происходит быстрее, чем при раке тела матки.
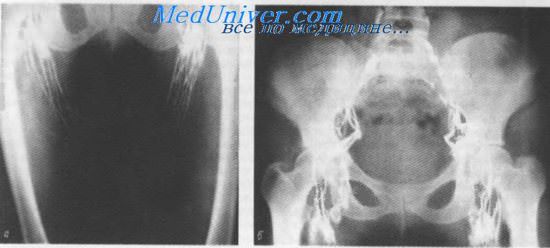
Лимфограмма. Глубокие лимфатические сосуды и узлы нижней конечности (а) и таза (б)
Лимфатическая система яичников
Лимфатические сосуды яичника на поверхности органа представлены в виде грубой сети. В воротах и в брыжейке яичника отводящие лимфатические сосуды образуют богатое подъяичниковое сплетение (plexus subovaricus); по выходящим из него 2—3 лимфатическим стволам лимфа оттекает в общие для яичника, тела матки и маточной трубы лимфатические узлы, расположенные по ходу яичниковых сосудов (nodi lymphatici ovarici) и далее — в регионарные лимфатические узлы; последние расположены преимущественно: слева— по левой полуокружности брюшной аорты, справа — по передней поверхности нижней полой вены.
Взаимоотношения лимфатических сосудов дна матки, яичников и маточной трубы также самые тесные. Отводящие лимфатические сосуды всех трех органов сливаются в упоминавшееся выше общее для них подъничниковое сплетение. Отток лимфы из матки, яичника и маточной трубы происходит в околоаортальные лимфатические узлы, в которые впадают также лимфатические сосуды и от органов брюшной полоста (Д. А. Жданов, 1952). Существует тесная связь путей оттока лимфы матки, мочевого пузыря и прямой кишки.
Хирургическая анатомия лимфатической системы матки имеет практическое значение и в связи с использованием в клинике метода предоперационного (прижизненного) окрашивания лимфатических узлов, например при операции Вертгейма (Е. В. Антипова, 1963; М. Марков, 1960).
Обнаружение метастазов в лимфатических узлах таза затруднено из-за огромного числа вариантов нормы; тем не менее, применение метода лимфографии перед операцией и во время последней имеет много преимуществ в связи с реальной возможностью более полного осуществления лимфаденэктомии. Методом лимфографии, выполнявшейся, в частности, после операции Вертгейма, было установлено, что в зоне иссечения лимфатических узлов последние контрастируются в тех случаях, когда удаление узлов было неполным, так как возможна частичная их регенерация. При тщательном же удалении лимфатических сосудов и узлов на большом протяжении последние не восстанавливаются и на лимфотраммах не обнаруживаются.
Восстановленные лимфатические узлы не достигают исходного состояния: они уменьшены в размерах, полигональны по форме и менее контрастны.
Лимфатические сосуды после операции Вертгейма теряют прямолинейность хода, образуют между собой многочисленные связи, не имеют четкообразных утолщений, становятся более извилистыми и чрезвычайно узкими. Ниже места резецированных лимфатических узлов и сосудов (паховая область, бедро) примерно в половине случаев образуется широкая сеть коллатералей, направляющихся к лимфатическим сосудам противоположной стороны. Основные лимфатические коллекторы бедра подвергаются редукции и деформации.
– Также рекомендуем “Расширенная абдоминальная экстирпация матки.”
Оглавление темы “Операции в гинекологии.”:
1. Хирургическое лечение трубного бесплодия
2. Сальпинго-сальпингоанастомоз. Техника сальпинго-сальпингоанастомоза.
3. Операция пересадки яичника в полость матки. Лимфатическая система матки.
4. Пути метастазирования опухоли при раке шейки матки и тела матки. Лимфатическая система яичников.
5. Расширенная абдоминальная экстирпация матки.
6. Основные этапы расширенной абдоминальной экстирпация матки.
7. Мочеточник. Хирургическая анатомия женского мочеточника.
8. Мочевой пузырь. Хирургическая анатомия женского мочевого пузыря.
9. Мочеиспускательный канал. Хирургическая анатомия женского мочеиспускательного канала.
10. Операции при недержании мочи. Операция прямой мышечной пластики сфинктера мочевого пузыря.
Источник
