Этапы развития т лимфоцитов в тимусе
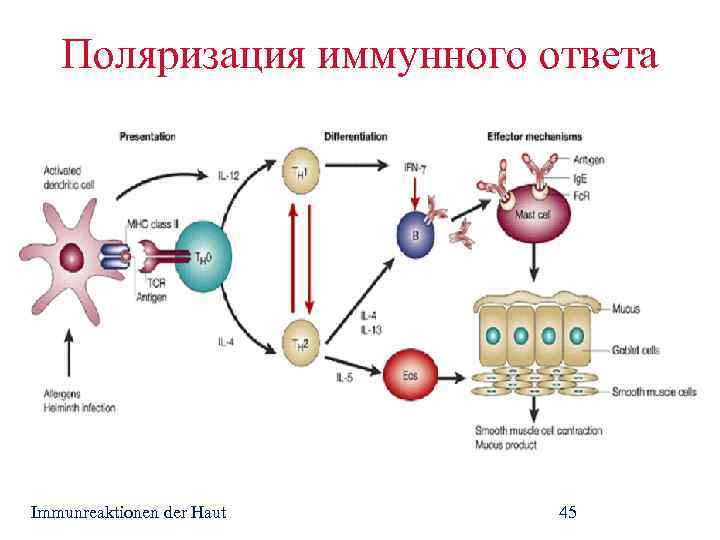
Т-лимфоциты несут на себе поражающее воображение разнообразие рецепторов, позволяющее распознавать практически любые чужеродные субстанции, с которыми может столкнуться организм. Путь от гемопоэтической стволовой клетки к 107–109 клонов Т-лимфоцитов с уникальными антиген-связывающими последовательностями — удивительное достижение эволюции. Многостадийное развития Т-лимфоцитов может выглядеть пугающим и запутывающим со страниц учебников. Однако, если вы дадите ему второй шанс, вы увидите, что это красивый и слаженный процесс.
Как и остальные клетки крови, Т-лимфоциты берут свое начало в костном мозге от гемопоэтической стволовой клетки. Такие клетки-предшественницы имеют мало общего со зрелыми функциональными Т-лимфоцитами: они не имеют антигенных рецепторов (TCR) и не умеют узнавать чужеродные антигены. Их ждет сложный путь развития, который осилят немногие, однако те, которые выживут, создадут армию, готовую к любой угрозе. Для развития Т-лимфоцитов в нашем теле формируется специальный орган — тимус. Создав достаточный репертуар рецепторов, тимус подвергается инволюции и практически не детектируется после пубертатного периода. Численность Т-лимфоцитов во взрослом организме в основном поддерживается делением зрелых клеток.
Для миграции в тимус клетки, чья судьба — стать Т-лимфоцитом, используют хемокиновый рецептор CCR9, лиганд для которого — CCL25 — секретируют клетки тимуса. Достигнув тимуса, предшественники Т-лимфоцитов становятся тимоцитами. Первым делом они получают сигнал от эпителиальных клеток тимуса через рецептор Notch-1, который окончательно определяет их судьбу в пользу Т-лимфоцита.
Следующая задача тимоцитов — активная пролиферация. Скорость деления тимоцитов крайне высока, поскольку 95 %–98 % этих клеток погибает. Дело в том, что судьба развивающегося Т-лимфоцита по умолчанию — апоптоз, спасти от которого его может только успешное прохождение нескольких раундов отбора. Сигнал для первого раунда деления — интерлейкин 7, который выделяют эпителиальные и другие клетки тимуса. Мутации в гене ИЛ-7 или его рецептора приводят к тяжелым иммунодефицитам. Пролиферация приводит к созданию большого пула клеток, которые называют дважды негативными клетками, поскольку они не несут на себе корецепторы CD4 и CD8. Большинство из них (90 %) дадут начало αβ Т-лимфоцитам, а 10 % — γδ Т-лимфоцитам.
После этого тимоциты приступают к перестройке генов антигенных рецепторов. Это тот самый момент, когда из небольшого количества генов возникает всё разнообразие антигенных рецепторов — миллионы и миллиарды. В ходе этого процесса участки генов антигенных рецепторов перестраиваются случайным образом. Ключевое слово здесь — случайный, поскольку процесс формирования рецепторов, способных эффективно распознавать чужеродные антигены, никак не зависит от этих антигенов и происходит задолго до встречи с ними!
До сих пор тимоциты содержали гены TCR в зародышевой конфигурации, т. е. не подвергшиеся перестройке. Такие гены не могут образовать TCR. Тимоциты начинают с перестройки генов одной из двух цепей TCR — β-цепи. После этого тимоциты проходят через первую контрольную точку. В случае успешной перестройки клетка экспрессирует β-цепь, которая вместе с инвариантной α-цепью формирует на поверхности клетки pre-TCR. Такой рецептор активируется без участия лиганда и передает в клетку сигналы для дальнейшего развития. Остальные клетки не проходят отбор: в случае неудачной перестройки pre-TCR не экпрессируется и клетка подвергается апоптозу в отсутствие сигналов к выживанию.
Активация pre-TCR поставляет в клетку важные сигналы для дальнейшего развития:
- Останавливается перестройка локуса β-цепи во втором аллеле. Это называется аллельное исключение — зрелые Т-лимфоциты экспрессируют β-цепь TCR только с одного аллеля.
- Начинается экспрессия двух ко-рецепторов CD4 и CD8, теперь тимоциты называются дважды позитивными.
- Начинается второй раунд пролиферации. Через pre-TCR клетки получают мощный сигнал к делению, приводящий к еще более интенсивной экспансии, чем в первом раунде.
- После этапа деления запускается перестройка α-цепи рецептора.
В отличие от цепи-партнера, α-цепь может подвергаться многократной перестройке, и большинство тимоцитов успешно с ней справятся. После перестройки α-цепи тимоциты наконец экспрессируют на своей поверхности полный αβ TCR. Однако впереди главная проверка, пройти которую суждено немногим.
Задачи последнего этапа отбора:
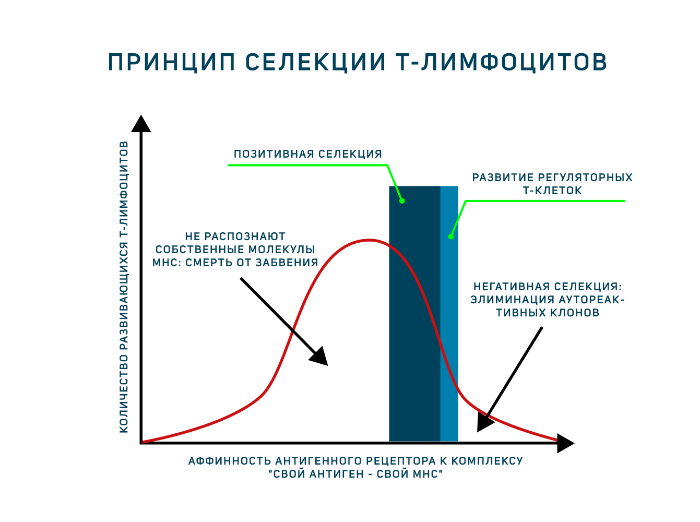
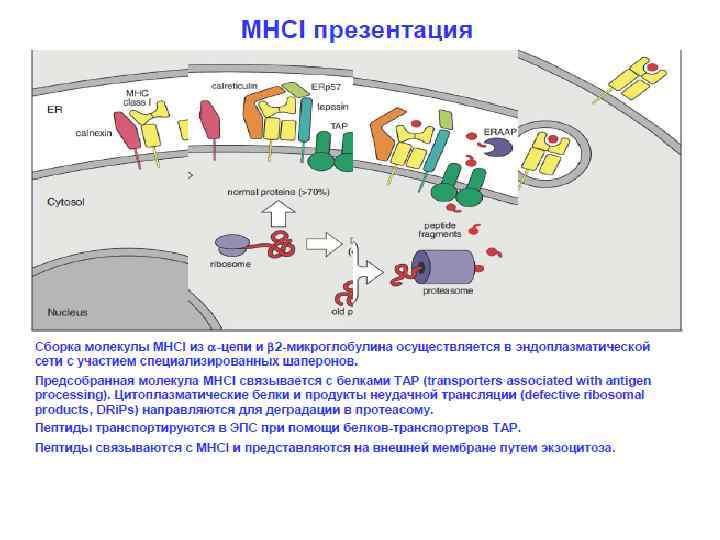
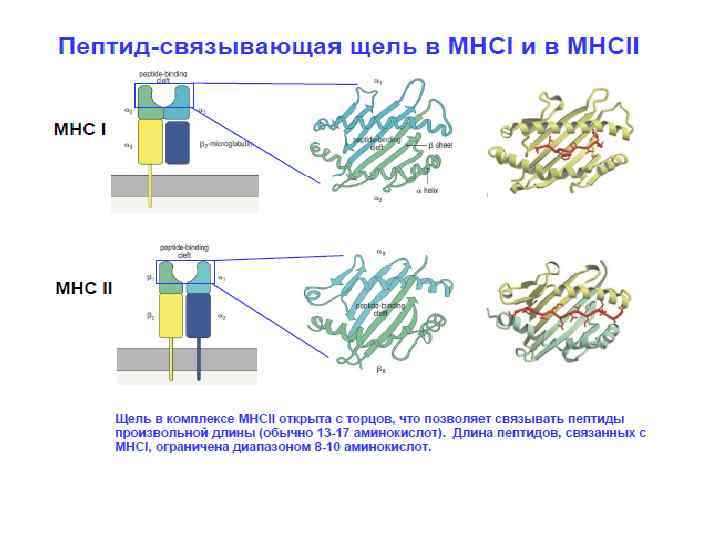
- Отобрать клетки, распознающие молекулы главного комплекса гистосовместимости (MHC) организма. Этот этап присутствует в развитии тимоцитов, поскольку зрелые Т-лимфоциты способны распознавать антигены только в составе МНС. Поэтому они должны знать МНС своего организма в лицо. Это называется позитивная селекция.
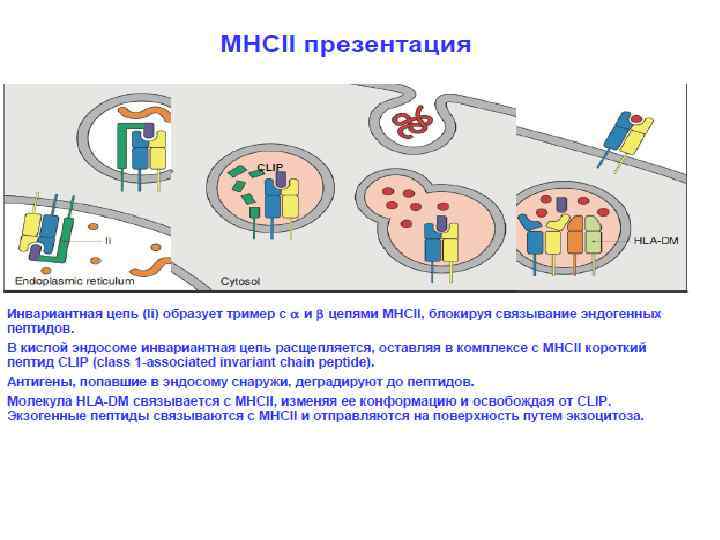
- Элиминировать клетки, распознающие собственные антигены. Это называется негативная селекция.
Однако антигенпрезентирующие клетки тимуса (эпителиальные клетки тимуса, дендритные клетки и макрофаги) располагают только комплексами «свой МНС — свой антиген». И позитивная, и негативная селекция осуществляется на основании взаимодействия TCR с такими комплексами! Для объяснения была предложена гипотеза аффинности. Тимоциты, чьи антигенные рецепторы проявят низкую аффинность к таким комплексам, продолжат развитие. Тимоциты, чьи рецепторы свяжутся с представленными антиген-МНС комплексами прочно, подвергнутся апоптозу как аутореактивные клоны (клональная делеция). Клетки, не распознающие МНС вовсе, т. е. не прошедшие позитивную селекцию, умрут особым способом, который называется смерть от забвения (death by neglect). Ещё один вариант развития — среднее связывание рецептора с антигенным комплексом, такие тимоциты могут дать начало регуляторным Т-клеткам. Таким образом, регуляторные Т-клетки — единственные лимфоциты, которые взаимодействуют со своим будущим антигеном в процессе развития! Развитию этого подтипа Т-лимфоцитов сейчас посвящено много исследований.
Особую роль в негативной селекции играет белок AIRE (аутоиммунный регулятор), который заставляет клетки тимуса экспрессировать в небольших количествах антигены, в норме присутствующие только в определенных тканях. Это позволяет сформировать толерантность к тканеспецифичным антигенам, встречающимся только за пределами тимуса. Мутация в белке AIRE приводит к развитию аутоиммунного полиэндокринного синдрома. AIRE содержится в эпителиальных клетках медуллы. При этом известно, что наиболее эффективно негативная селекция осуществляется при презентации антигена дендритными клетками и макрофагами, а не стромой тимуса. В новом исследовании был показан перенос антигенов из эпителиальных клеток тимуса в дендритные клетки, которые их и презентируют!
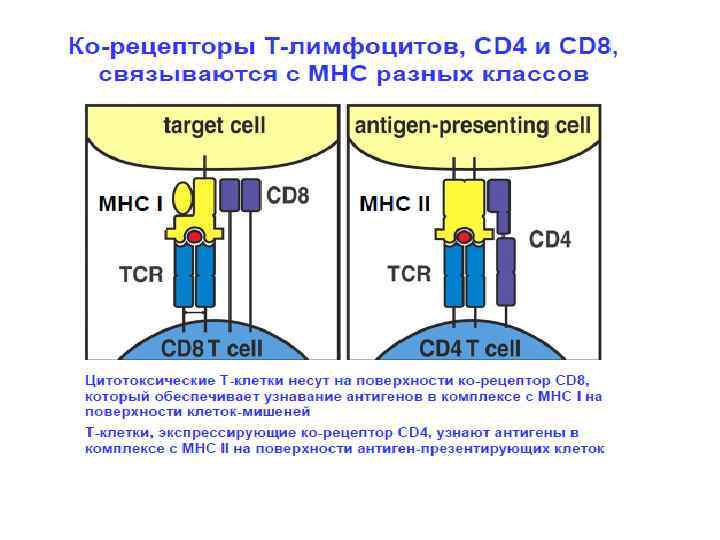
Одновременно с позитивной и негативной селекцией осуществляется проверка, соответствует ли корецептор распознаваемому классу МНС — т. е. происходит дифференцировка в функциональные подклассы. Выживают только клетки с правильной комбинацией: CD8 + MHC I — цитотоксические Т-лимфоциты и CD4 + MHC II — Т-хелперы.
Последнее, что должен сделать лимфоцит перед тем, как покинуть тимус — это изменить тип сигналинга через антигенный рецептор. Если незрелые Т-лимфоциты с высоким родством к антигену погибают, то зрелые — активируются (молекулярные основы такой принципиальной разницы не ясны). Теперь лимфоциты готовы заселить периферические лимфоидные органы и нести оборону. Зрелые Т-лимфоциты покидают тимус, используя градиент сфингозин-1-фосфата, — липида, присутствующего в высоких концентрациях в крови и лимфе, для хемотаксиса в кровяное русло. Для хоуминга во вторичные лимфоидные ткани они используют CD62L (L-селектин).
γδ Т-лимфоциты несут менее разнообразные антигенные рецепторы, по-видимому, не зависящие от МНС. Они не экспрессируют корецепторы CD4, CD8. γδ Т-лимфоциты выступают в роли первой линии обороны против часто встречающихся бактерий в эпителиальных и слизистых тканях и скорее относятся ко врожденной иммунной системе, чем к адаптивной.
Источники:
- Kenneth Murphy, Casey Weaver. Janeway’s Immunobiology 9th edition. Garland Science, 2017.
- Abul Abbas, Andrew H. Lichtman, Shiv Pillai. Cellular and Molecular Immunology 9th Edition. Elsevier, 2017.
- Perry J. S. et al. CD36 Mediates Cell-Surface Antigens to Promote Thymic Development of the Regulatory T Cell Receptor Repertoire and Allo-tolerance //Immunity. – 2018. – 923-936.
Нашли опечатку? Выделите фрагмент и нажмите Ctrl+Enter.
Источник
- Иммунология и аллергология
- Иммунология
- Иммунология: Учебник
Два наблюдения: необходимость тимуса для накопления функционально зрелых Т-клеток на периферии и высокая гибель активно пролиферирующих тимоцитов in situ, указывают на тот факт, что в тимусе происходят те основные события, которые определяют полноценность работы всей Т-системы. Подобная феноменология требовала выяснения, по крайней мере, двух вопросов: каков биологический смысл массовой гибели клеток в тимусе и как формируются субпопуляции клоноспецифических Т- клеток (Т- киллеров, Т-хелперов) в органе?

Рис. 7.1. Значение эпителиального микроокружения тимуса для дифференцирован костномозговых предшественников до зрелых Т-клеток.
Мутантные мыши scid имеют полноценный тимус, однако Т-клетки не образуются, так как имеется дефект рекомбинации генов для антиген распознающих рецепторов (1). Другая мутантная линия мышей — nude — также неспособна к формированию Т-клеток из-за отсутствия тимуса: у этой линии мышей обнаруживается только рудимент органа (2). Трансплантация клеток костного мозга мышей nude мышам scid обеспечивает развитие Т-клеток (3). Опыт демонстрирует наличие у мышей nude полноценных костномозговых предшественников Т-клеток. При трансплантации мышам nude тимуса от мышей scid восстанавливается образование Т-клеток у nude-хозяина. Эта форма трансплантации показывает роль эпителиального микроокружения тимуса для нормального развития костномозговых предшественников до зрелых Т-клеточных форм
Этапы внутритимусной дифферен цировки клеток от мигрировавшего в орган костномозгового предшественника (пре-Т-клет- ки) до зрелого Т-лимфоцита, покидающего тамус, связаны с изменением экспрессии фенотапических, Т-клеточных маркеров. Основными из них являются: CD4 — корецептор Т-хелперов, CD8 — корецептор цитотоксических Т-лимфоцитов (ЦТЛ; Т-киллеров) и сфТКР — Т-клеточный антигенраспознающий рецептор. Специфическая комбинация этих поверхностных молекул может быть использована в качестве маркеров дифферен цировки клеток в тимусе (табл. 7.1).
Первые мигранты из костного мозга — пре-Т-клетки — представляют собой лимфобласты, имеющие определенный набор
Таблица 7.1
Фенотипические маркеры дифференцирующихся тимоцитов
| Этап | Маркеры | Тип дифференцирующихся тимоцитов | |
| корсцепторы Т-клеток | Т-клеточный рецептор | ||
| I | CD4 CD8- | apTKP- | двойной негатив |
| 2 | cm* CDs* | apTKP” | |
| 3 | CD4+ CD8+ | aflTKP* | двойной позитив |
| 4 | CD4+ CD8+ | apTKP+ | двойной ПОЗИТИВ |
| 5 | CD4+ CDS’ | apTKP+ | одинарный позитив |
| CD4- CD8+ | apTKP* | одинарный позитив | |
поверхностных молекул, но лишенных основных маркеров диф- ференцировки: CD4 и CD8 (рис. 1.2). Отсюда и их название — “двойные негативы11. Они заселяют верхнюю часть коры тимуса, расположенные, непосредственно под капсулой органа — субкапсулярную область (рис. 7.3). В полностью развитом тимусе двойные негативные клетки составляют незначительный пул (всего около 5% от общего числа тимоцитот?
Взаимодействие раннего предшественника со стромой субкапсулярной области приводит к экспрессии первого специфического маркера Т-клеток: CD2 — у людей и Thy-1 — у мышей. Обе молекулы обладают адгезивными свойствами и относятся к суперсемейству иммуноглобулинов. Thy-1 является исключительным маркером Т-клеток мышей и сохраняется на всех стадиях диф- ференцировки данных клеток, хотя уровень его экспрессии у более зрелых тимоцитов и периферических Т-клеток снижен по сравнению с ранними предшественниками.
Тимоцитарные бласты субкапсулярной области, находясь в тесном контакте с эпителиальными клетками-кормилицами, ак-
Рис. 7.2. ЭпшянттшеэаикпсойдяФфереяцщхяпТ-клстмс.
На первом этапе из плюри потентной стволовой кроветворной клетки (СКК) костного мозга, обеспечивающей миело- и лимфопоэз, образуется общий для Т- н В-лимфоцитов предшественник — ПрЛЦ. Ближайший потомок ПрЛЦ — проти- моцит, или коммитированный предшественник Т-клеток (пре-Т-кл.). Характерным маркером пре-Т-клеток костного мозга является один из антигенов мозга (AM). Первые мигрирующие в субкапсулярную область тимуса пре-Т-клетки теряют AM, но приобретают типичный маркер тимоцитов и периферических Т-клеток — Thy-1. Тимоциты субкапсулярной зоны являются в основном двойными негативами и не экспрессируют Т-клеточный рецептор (ТКР). Фенотип таких клеток — CD4″CD8~a0TKP Постепенно, по мере перемещения в корковый слой тимоциты начинают экспрессию как CD4-, так и С08-корецепторов, а также сфТКР. Медуллярная зона тимуса — место локализации властных форм с фенотипом, характерным для самостоятельных субпопуляций Т-клеток (CD4+CD8’a0TKP+ — Т-хелпе- ры/индукторы; CD4’CD8+apTKP*). Формированием различных субпопуляций завершается внутритимусная дифференцировка тимоцитов. Образовавшиеся субпопуляции мигрируют в периферические лимфоидные органы (лимфатические узлы, селезенку и др.)

Рис. 7.3. Локализация дифференцирующихся тнмоцнтоь и различных областях пща.
Пре-Т- клетки, мигрирующие из костного мозга в тимус, заселяют субкапсулярную зону тимуса. Клетки этой стадии развития представляют собой незрелые формы, которые не экспрессируют ТКР и корецепторы (фенотип CD4CD8TKP). В результате их взаимодействия с эпителиальными клетками-кормилицами, представленными в субкапсуле, начинается процесс внутритимусной дифференциров- ки. В промежуточной зоне между субкапсулой и корой, а также частично в коре, появляются тимоциты с умеренной экспрессией корецепторов и (3-цепи ТКР (фенотип CD4±CD8±pTKP±). Под влиянием эпителиальных клеток коры проходит дальнейшее созревание тимоцитов, что регистрируется по усилению экспрессии корецепторов CD4 и CD8 и полноценой экспрессии ТКР (фенопип СШ’ХОв^офТКР*). Последующая дифференцмровка осуществляется в переходной зоне кортико-медуллярного соединения под влиянием дендритных клеток и макрофагов. В результате образуются сублопуляции Т-киллеров/супрессоров (фенотип CD4′ CD8+apTKP+) и Т-хелперов/индукторов (фенотип CD4+CD8’apTKP+)
тивно пролиферируют и завершают свой путь развития в данной области умеренной экспрессией CD4 и CD8. Тимоциты с фенотипом CD4*, CDS*, рТКР* перемещаются в корковый слой.
Клетки коры — это в основном малые, плотно упакованные тимоциты. Они находятся в непосредственных контактных отношениях с кортикальными эпителиальными клетками, обладающими разветвленными выростами, которые окружают тимоциты. Выраженная экспрессия на поверхности эпителиальных клеток молекул 1 и II классов МНС является определяющим фактором положительной селекции клеток тимуса (см. ниже). В результате взаимодействия эмигрантов из субкапсулярной области с эпителиальными клетками коры происходит активная, одновременная экспрессия на поверхности тимоцитов двух корецепторов — CD4 и CD8, что дало названием кортикальным клеткам “двойные позитивы”. При этом двойные позитивные тимоциты становятся обладателями полноценных арТКР. Таким образом основной фенотип кортикальных тимоцитов — CD4+, CD8+, арТКР4′.
Факт прохождения положительной селекции в коре определяет дальнейшую дифференцировку на субпопуляпии CD4+CD8′ и CD4″CD8+, которая осуществляется в основном в переходной области — кортико-медуллярном соединении под влиянием взаимодействия с дендритными клетками и макрофагами. Эти клетки получили название “одинарных позитивов”. Здесь же проходит и отрицательная селекция тимоцитов (см.ниже). В результате прошедших дифференцировочных событий в медуллярной области накапливаются клетки с фенотипом CD4+CD8’TKP+ (Т-хелгтеры) и CD4″CD8*TKP+ (Т-киллеры), часть которых мигрирует в периферические лимфоидные органы.
Источник: В.Г. Галактионов., «Иммунология: Учебник» 1998
А так же в разделе «Этапы внутритимусной дифференцирован лимфоцитов »
- Основная феноменология
- 7.1.3. Реорганизация генов Т-клеточного рецептора в процессе дифференцнровки тимоцитов
- Положительная селекция клеток в тимусе
- Отрицательная cejieKuun клеток в тимусе
- 7.1.4.4. Возможные механизмы положительной и отрицательной селекции клеток в тимусе
Источник

Лекция 4 Т-ЛИМФОЦИТЫ
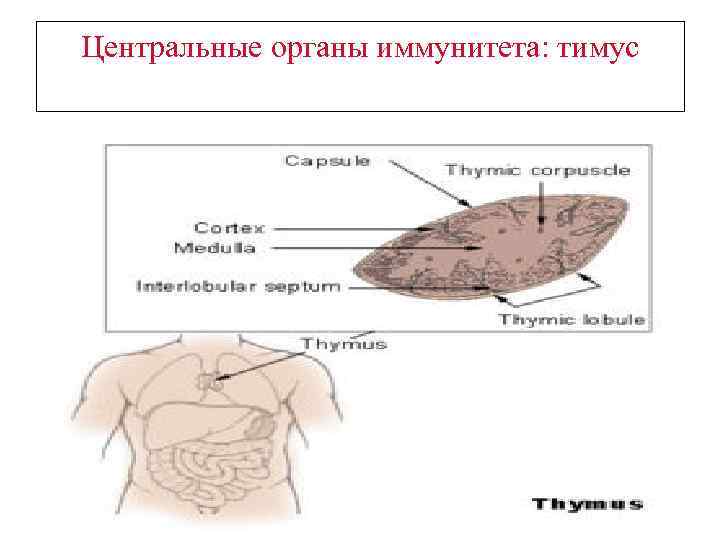
Центральные органы иммунитета: тимус
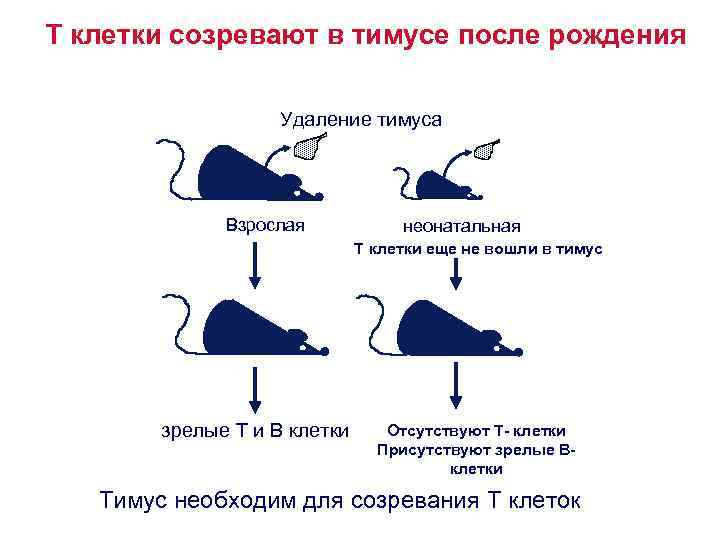
Т клетки созревают в тимусе после рождения Удаление тимуса Взрослая неонатальная T клетки еще не вошли в тимус зрелые T и B клетки Отсутствуют Т- клетки Присутствуют зрелые Вклетки Тимус необходим для созревания T клеток
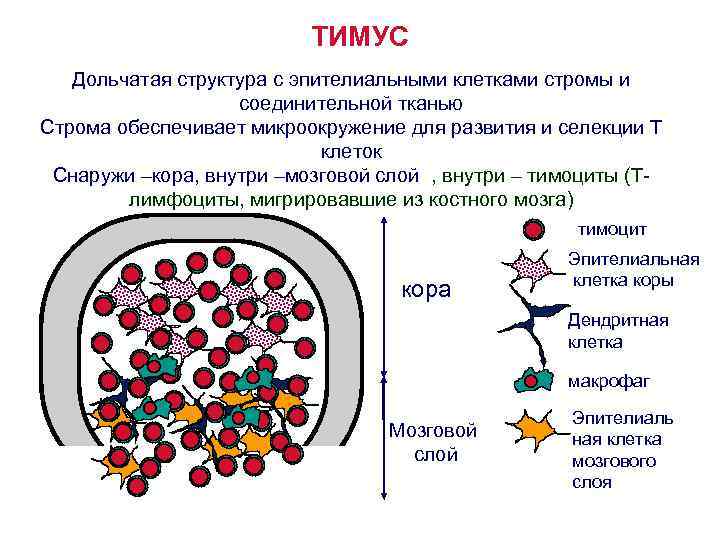
ТИМУС Дольчатая структура с эпителиальными клетками стромы и соединительной тканью Строма обеспечивает микроокружение для развития и селекции Т клеток Снаружи –кора, внутри –мозговой слой , внутри – тимоциты (Тлимфоциты, мигрировавшие из костного мозга) тимоцит кора Эпителиальная клетка коры Дендритная клетка макрофаг Мозговой слой Эпителиаль ная клетка мозгового слоя
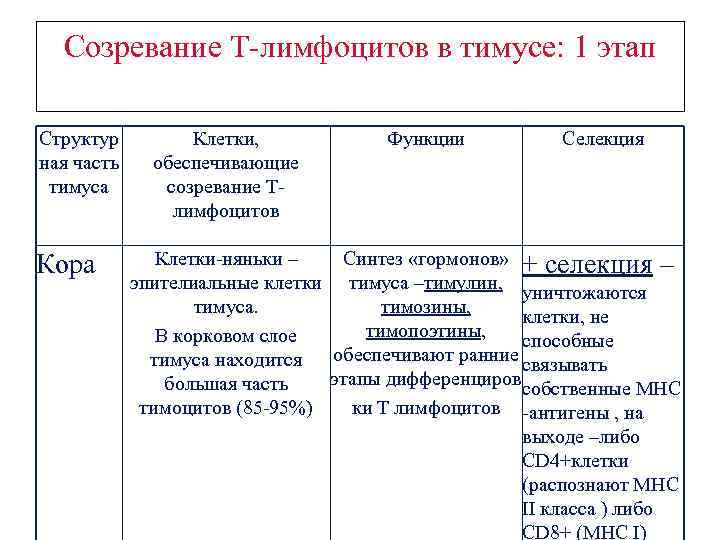
Созревание Т-лимфоцитов в тимусе: 1 этап Структур ная часть тимуса Кора Клетки, обеспечивающие созревание Тлимфоцитов Функции Селекция Клетки-няньки – Синтез «гормонов» + селекция – эпителиальные клетки тимуса –тимулин, уничтожаются тимуса. тимозины, клетки, не тимопоэтины, В корковом слое способные обеспечивают ранние связывать тимуса находится этапы дифференцировсобственные МНС большая часть тимоцитов (85 -95%) ки Т лимфоцитов -антигены , на выходе –либо CD 4+клетки (распознают МНС II класса ) либо CD 8+ (МНС I)
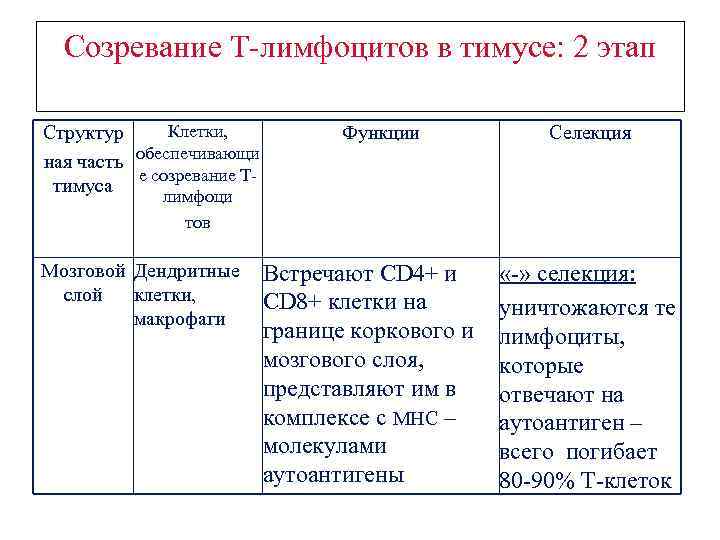
Созревание Т-лимфоцитов в тимусе: 2 этап Клетки, Структур ная часть обеспечивающи е созревание Ттимуса Функции Селекция лимфоци тов Мозговой Дендритные слой клетки, макрофаги Встречают CD 4+ и CD 8+ клетки на границе коркового и мозгового слоя, представляют им в комплексе с МНС – молекулами аутоантигены «-» селекция: уничтожаются те лимфоциты, которые отвечают на аутоантиген – всего погибает 80 -90% Т-клеток

Интенсивность отбора тимоцитов • T клетки созревают в тимусе, но гораздо больше Т- клеток погибает в тимусе. • 98% клеток погибает в тимусе без развития воспаления и изменения размеров тимуса. • Макрофаги тимуса фагоцитируют апоптозные тимоциты.
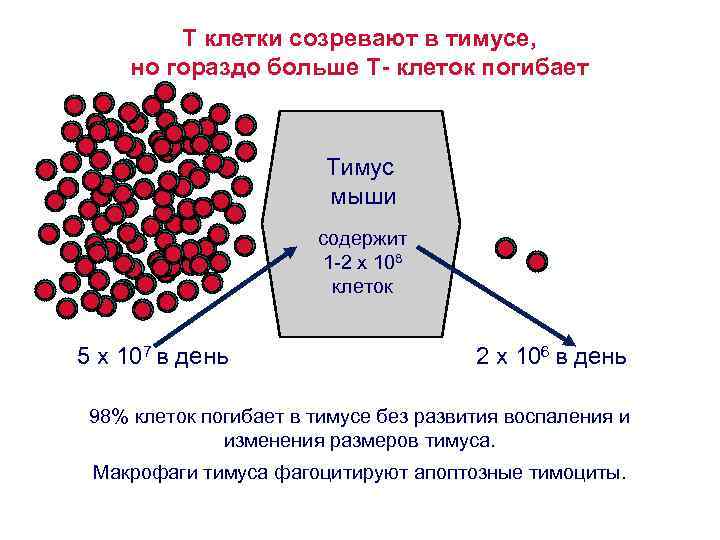
T клетки созревают в тимусе, но гораздо больше Т- клеток погибает Тимус мыши содержит 1 -2 x 108 клеток 5 x 107 в день 2 x 106 в день 98% клеток погибает в тимусе без развития воспаления и изменения размеров тимуса. Макрофаги тимуса фагоцитируют апоптозные тимоциты.

Двойное распознавание – «свое» и «чужое» • T клетки способны развиваться только в том случае, если их Tc. R распознают часть собственных молекул MHC. • Tc. R способны распознавать собственные антигены – молекулы главного комплекса гистосовместимости (МНС), ассоциированные с фрагментами чужеродных АГ. • MHC молекулы участвуют в активации Т клеток.

Процесс созревания тимоцитов: этапы формирования корецепторов • • Корецепторы: CD 4 – распознает молекулы МНС 2 класса CD 8 – распознает молекулы МНС 1 класса В коре находятся незрелые двойные негативные (CD 3/Tc. R-CD 4 – 8 -) и двойные позитивные тимоциты (CD 3/Tc. R- CD 4+ 8+), при переходе в мозговой слой клетки теряют либо CD 4, либо CD 8 молекулы и становятся однопозитивными • В мозговом слое – зрелые однопозитивные тимоциты, их 2 типа: • либо (CD 3+ Tc. R CD 4+) –Т –хелперы • либо (CD 3+ Tc. R CD 8+) –Т –цитотоксические клетки
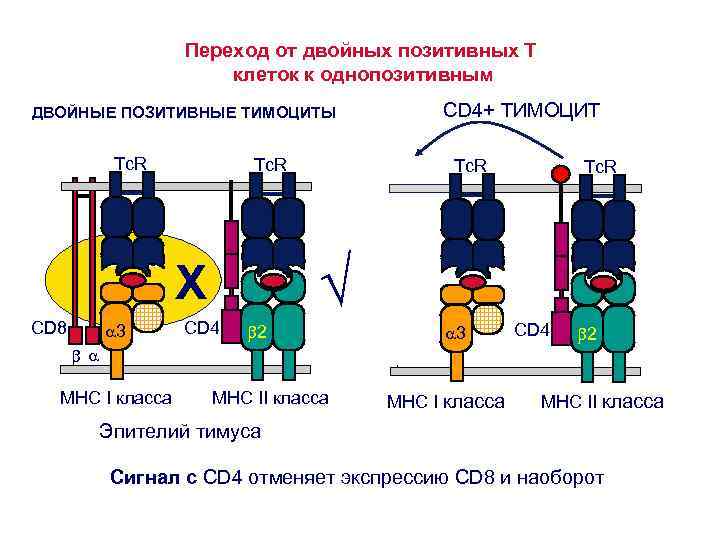
Переход от двойных позитивных Т клеток к однопозитивным CD 4+ ТИМОЦИТ ДВОЙНЫЕ ПОЗИТИВНЫЕ ТИМОЦИТЫ Tc. R 3 Tc. R √ X CD 8 Tc. R CD 4 2 CD 8 3 CD 4 2 MHC I класса MHC II класса Эпителий тимуса Сигнал с CD 4 отменяет экспрессию CD 8 и наоборот

Строение Т рецепторов • Т клеточный рецептор имеет и -цепи (есть альтернативные рецепторы, которые имеют и цепи- обеспечивают иммунитет слизистых оболочек, первичный ответ при инфекции). • Каждая и цепь в составе Т рецептора имеет: • 1 наружный вариабельный Vдомен и и 1 наружный константный Cдомен • Трансмембранный сегмент • Цитоплазматический хвостик (короткий)
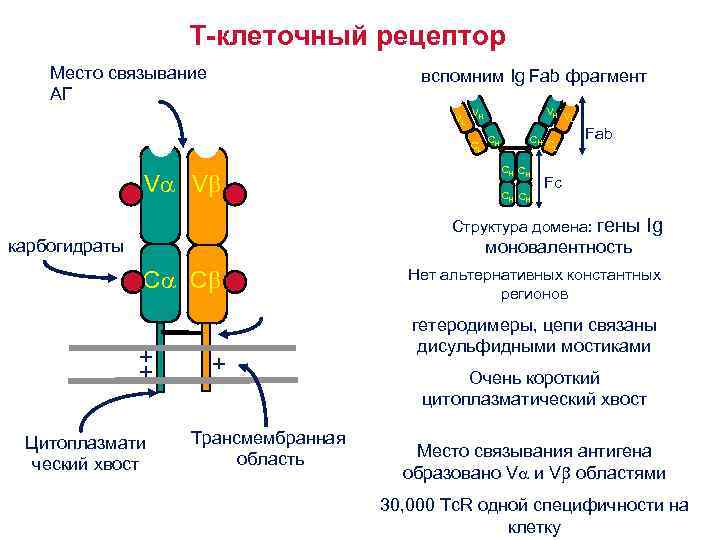
Т-клеточный рецептор Место связывание АГ вспомним Ig Fab фрагмент VL CL V V VH V L VH CH CH CH CL Fab Fc Структура домена: гены карбогидраты моновалентность C C + + Цитоплазмати ческий хвост + Трансмембранная область Ig Нет альтернативных константных регионов гетеродимеры, цепи связаны дисульфидными мостиками Очень короткий цитоплазматический хвост Место связывания антигена образовано V и V областями 30, 000 Tc. R одной специфичности на клетку

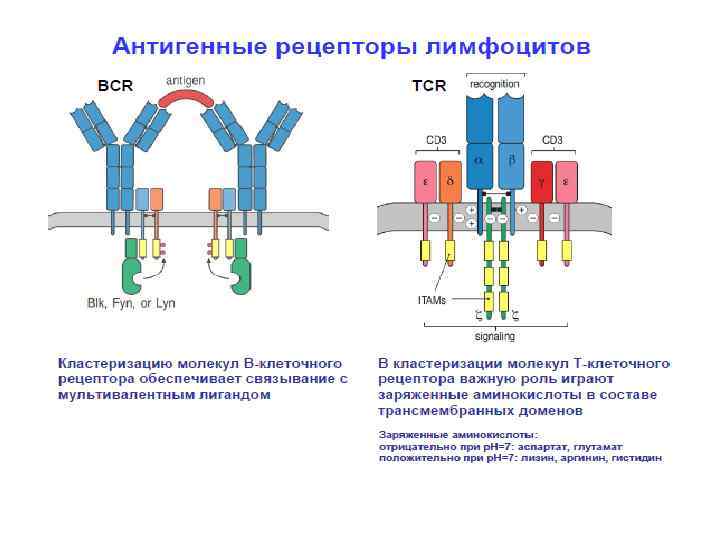
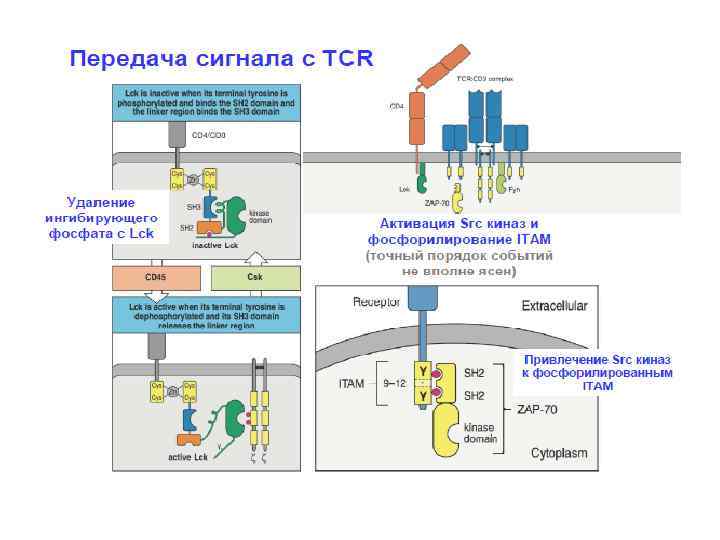
Строение Т рецепторного комплекса • На клеточной поверхности -Т клеточный рецептор (или ) расположен в непосредственной близости к комплексу, называемому CD 3. • Через комплекс CD 3 происходит передача сигнала с Т клеточного рецептора в клетку.
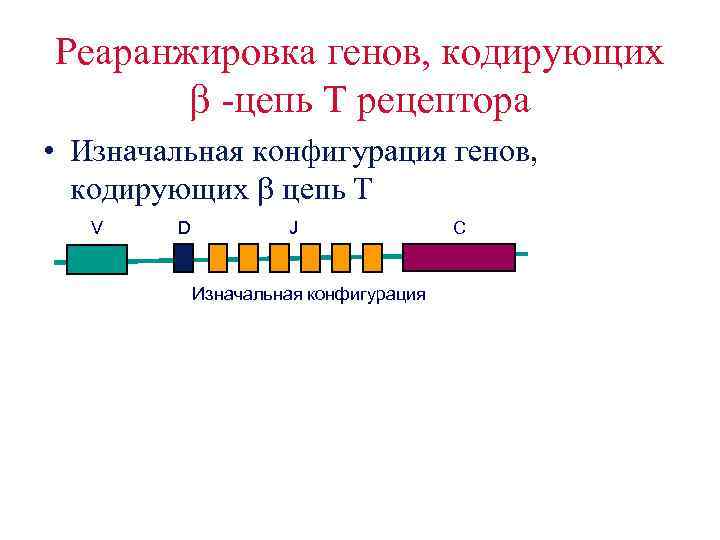
Реаранжировка генов, кодирующих -цепь Т рецептора • Изначальная конфигурация генов, кодирующих цепь Т V D J Изначальная конфигурация C

Реаранжировка генов, кодирующих Т рецептор, путем соматической рекомбинации • 1 этап – слияние генов D-J • 2 этап – слияние генов V-DJ • 3 этап – сборка цепи V D J C V DJ C V-DJ слияние D-J слияние
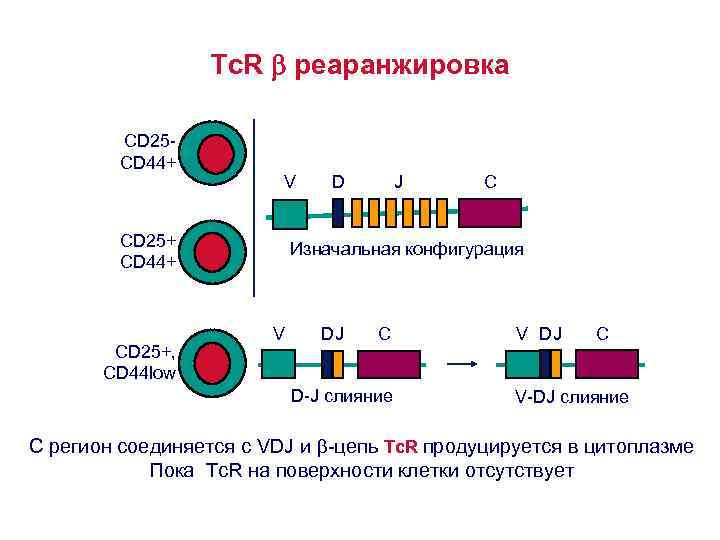
Tc. R реаранжировка CD 25 CD 44+ V CD 25+ CD 44+ CD 25+, CD 44 low D J C Изначальная конфигурация V DJ C D-J слияние V DJ C V-DJ слияние C регион соединяется с VDJ и -цепь Tc. R продуцируется в цитоплазме Пока Tc. R на поверхности клетки отсутствует

Реаранжировка генов, кодирующих -цепь Т рецептора, сборка Т рецептора • Те же этапы, что и при перестройке генов -цепи. • По окончании реаранжировки генов цепи происходит считывание м РНК , построение белков, совместная сборка и цепей, экспрессия на поверхностную мембрану Т- рецепторного комплекса. • T клетки уже могут распознать антиген и взаимодействовать с молекулами MHC I и II классов через корецепторы – CD 4 и CD 8. • После этого начинается селекция
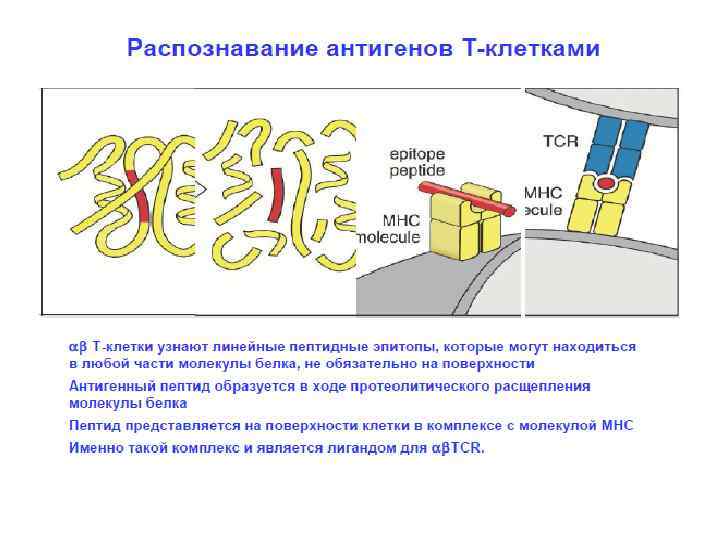


Антигены и суперантигены: различные механизмы презентации и распознавания антигены суперантигены Требуется процессинг до пептидов Не процессируются Tc. R и цепи участвуют в распознавании презентируются молекулами MHC I или. II класса Большинство белков антигены только Tc. R цепь участвует в распознавании Презентируются в основном молекулами MHC II класса Очень небольшое число антигенов суперантигены
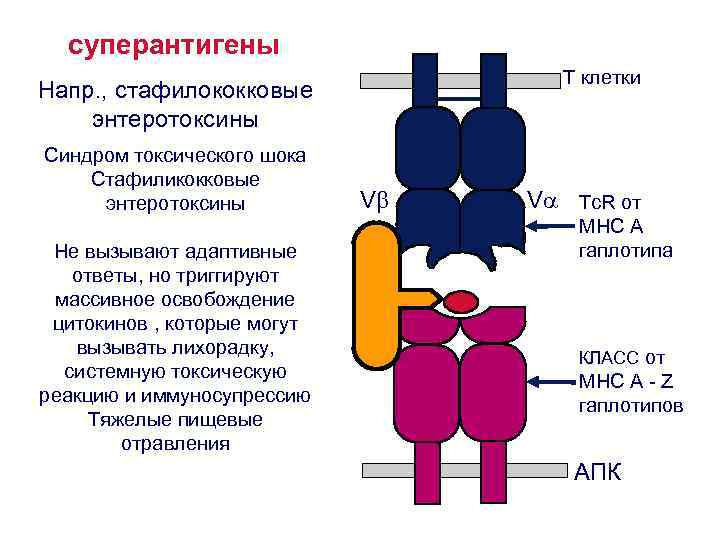
суперантигены T клетки Напр. , стафилококковые энтеротоксины Синдром токсического шока Стафиликокковые энтеротоксины Не вызывают адаптивные ответы, но триггируют массивное освобождение цитокинов , которые могут вызывать лихорадку, системную токсическую реакцию и иммуносупрессию Тяжелые пищевые отравления V V Tc. R от MHC A гаплотипа КЛАСС от MHC A – Z гаплотипов АПК


Каким образом развивается аутотолерантность к антигенам, отсутствующим в тимусе? • T клетки, несущие Tc. R , и вступающие во взаимодействие с антигенами тимуса, уничтожаются (отрицательная селекция). • Но! Некоторые аутоантигены не экспрессируются в тимусе – т. е. с ними тимоцит встретится впервые, когда он выйдет на периферию. • Вывод: клеточная толерантность должна развиваться и вне тимуса.

Механизмы формирования периферической толерантность или анергии Антигенпрезентирующие клетки не выполняют функцию костимуляции, т. е. не передают сигналы активации Т клеткам, вступившим в контакт с антигеном.

Костимуляция: АПК – Т лимфоцит 1. Костимулирующие молекулы- члены семейства B 7 (CD 80 и CD 86) экспрессируются на большинстве АПК, включая, клетки Лангерганса, моноциты/макрофаги, В клетки и др. , но не клетками, которые не обладают функциями иммунорегуляции – такими, как мышечные, нервные клетки , гепатоциты, эпителиальные клетки и др. 2. Молекулы семейства B 7 (CD 80 и CD 86) на АПК связываются с молекулой CD 28 на поверхности Т клетки.

Механизм костимуляции Т клеток • На покоящихся Т клетках экспрессируются низкоаффинные рецепторы к интерлейкину -2 (IL 2 R) – его и цепи, но не -цепь. • После стимуляции Т лимфоцита, активируются гены, кодирующие -цепь. • Экспрессия -цепи IL 2 R превращает IL 2 рецептор в высокоаффинную форму. • Костимулирующие сигналы активируют ядерные факторы транскрипции , это приводит к повышению продукции интерлейкина -2 более, чем в 100 раз. • Связывание IL 2 R с IL 2 запускает процесс пролиферации Т лимфоцитов, т. е. клональную экспансию.
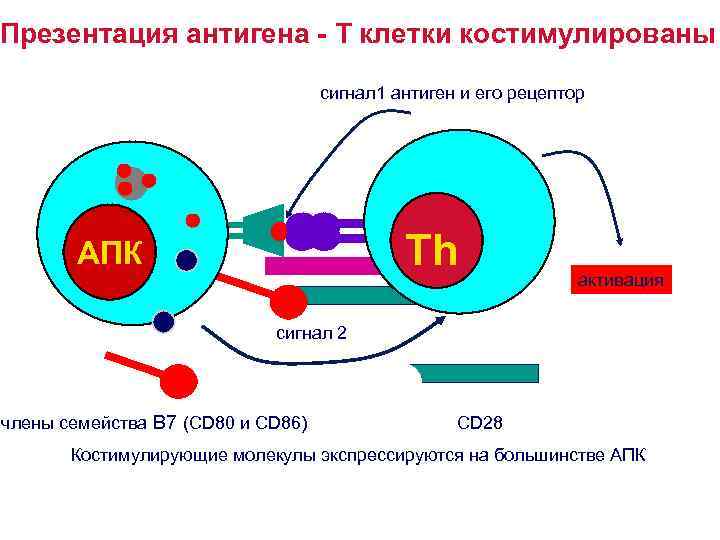
Презентация антигена – T клетки костимулированы сигнал 1 антиген и его рецептор Th АПК активация сигнал 2 члены семейства B 7 (CD 80 и CD 86) CD 28 Костимулирующие молекулы экспрессируются на большинстве АПК
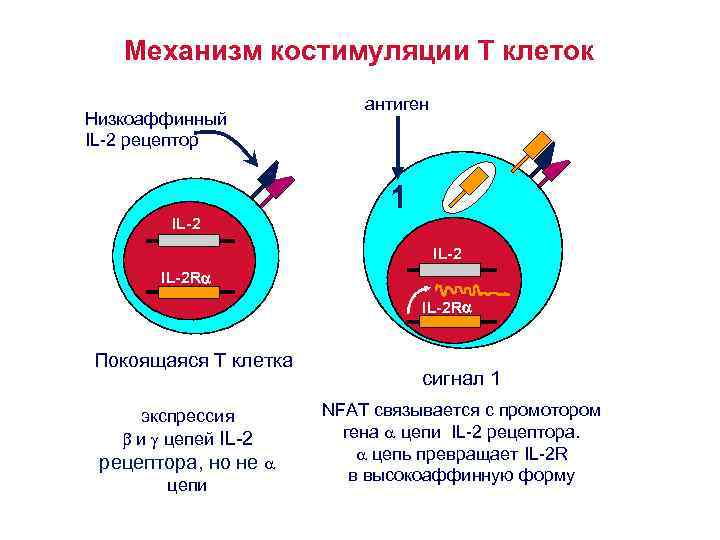
Механизм костимуляции Т клеток Низкоаффинный IL-2 рецептор антиген 1 IL-2 R Покоящаяся Т клетка экспрессия и цепей IL-2 рецептора, но не цепи сигнал 1 NFAT связывается с промотором гена цепи IL-2 рецептора. цепь превращает IL-2 R в высокоаффинную форму
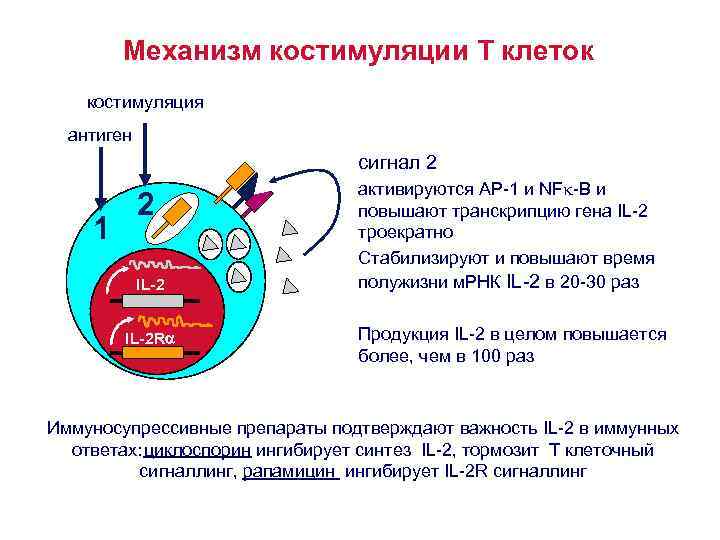
Механизм костимуляции Т клеток костимуляция антиген сигнал 2 1 2 IL-2 R активируются AP-1 и NFk-B и повышают транскрипцию гена IL-2 троекратно Стабилизируют и повышают время полужизни м. РНК IL-2 в 20 -30 раз Продукция IL-2 в целом повышается более, чем в 100 раз Иммуносупрессивные препараты подтверждают важность IL-2 в иммунных ответах: циклоспорин ингибирует синтез IL-2, тормозит Т клеточный сигналлинг, рапамицин ингибирует IL-2 R сигналлинг
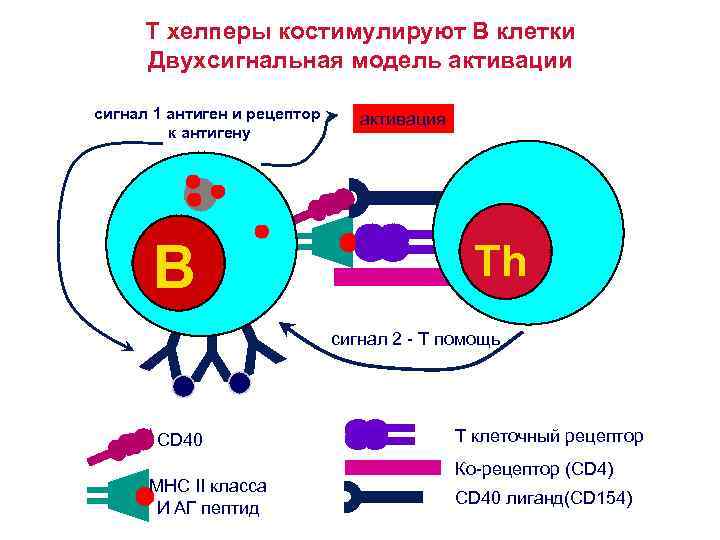
T хелперы костимулируют В клетки Двухсигнальная модель активации сигнал 1 антиген и рецептор к антигену B Y YY CD 40 MHC II класса И АГ пептид активация Th сигнал 2 – T помощь T клеточный рецептор Ко-рецептор (CD 4) CD 40 лиганд(CD 154)

Анергия (неотвечаемость) развивается при отсутствии сигналов костимуляции • Если Т клетка получает только 1 сигнал – антиген+МНС, который распознается Т клеточным рецептором, но при этом не получает костимулирующих сигналов, она не способна к активации. • В этом случае Т-клетка не способна продуцировать IL-2 и поэтому не способна пролиферировать и подвергаться клональной селекции.
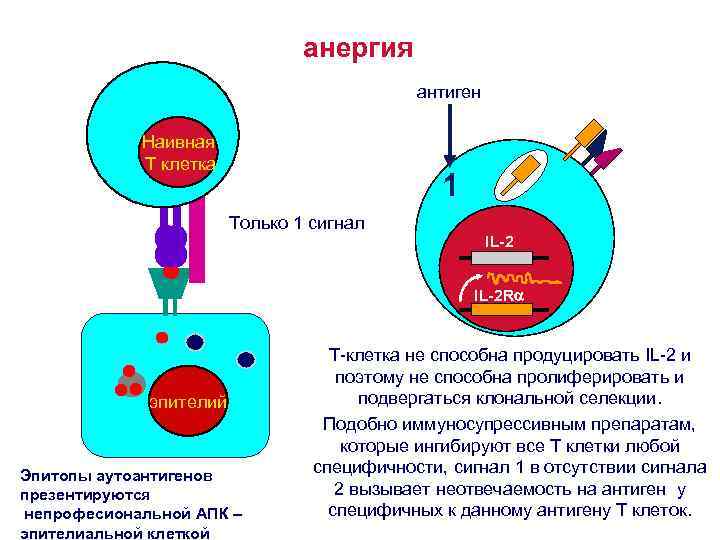
анергия антиген Наивная Т клетка 1 Только 1 сигнал IL-2 R эпителий Эпитопы аутоантигенов презентируются непрофесиональной АПК – эпителиальной клеткой Т-клетка не способна продуцировать IL-2 и поэтому не способна пролиферировать и подвергаться клональной селекции. Подобно иммуносупрессивным препаратам, которые ингибируют все Т клетки любой специфично?