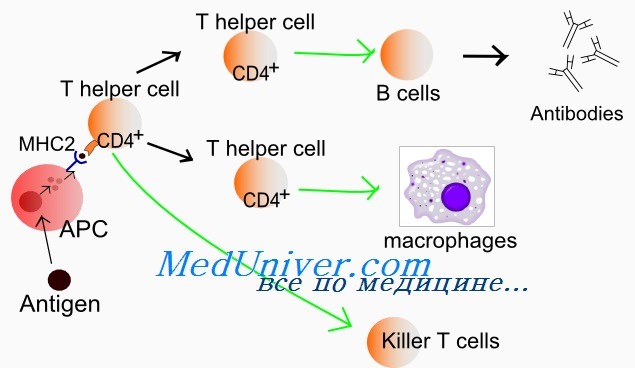
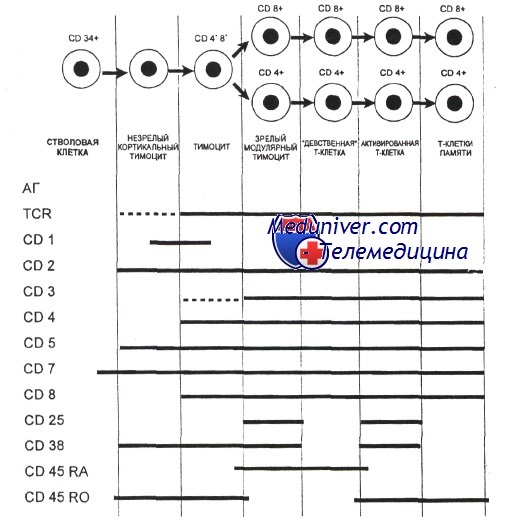
Этапы развития т лимфоцитов
Т-лимфоциты несут на себе поражающее воображение разнообразие рецепторов, позволяющее распознавать практически любые чужеродные субстанции, с которыми может столкнуться организм. Путь от гемопоэтической стволовой клетки к 107–109 клонов Т-лимфоцитов с уникальными антиген-связывающими последовательностями — удивительное достижение эволюции. Многостадийное развития Т-лимфоцитов может выглядеть пугающим и запутывающим со страниц учебников. Однако, если вы дадите ему второй шанс, вы увидите, что это красивый и слаженный процесс.
Как и остальные клетки крови, Т-лимфоциты берут свое начало в костном мозге от гемопоэтической стволовой клетки. Такие клетки-предшественницы имеют мало общего со зрелыми функциональными Т-лимфоцитами: они не имеют антигенных рецепторов (TCR) и не умеют узнавать чужеродные антигены. Их ждет сложный путь развития, который осилят немногие, однако те, которые выживут, создадут армию, готовую к любой угрозе. Для развития Т-лимфоцитов в нашем теле формируется специальный орган — тимус. Создав достаточный репертуар рецепторов, тимус подвергается инволюции и практически не детектируется после пубертатного периода. Численность Т-лимфоцитов во взрослом организме в основном поддерживается делением зрелых клеток.
Для миграции в тимус клетки, чья судьба — стать Т-лимфоцитом, используют хемокиновый рецептор CCR9, лиганд для которого — CCL25 — секретируют клетки тимуса. Достигнув тимуса, предшественники Т-лимфоцитов становятся тимоцитами. Первым делом они получают сигнал от эпителиальных клеток тимуса через рецептор Notch-1, который окончательно определяет их судьбу в пользу Т-лимфоцита.
Следующая задача тимоцитов — активная пролиферация. Скорость деления тимоцитов крайне высока, поскольку 95 %–98 % этих клеток погибает. Дело в том, что судьба развивающегося Т-лимфоцита по умолчанию — апоптоз, спасти от которого его может только успешное прохождение нескольких раундов отбора. Сигнал для первого раунда деления — интерлейкин 7, который выделяют эпителиальные и другие клетки тимуса. Мутации в гене ИЛ-7 или его рецептора приводят к тяжелым иммунодефицитам. Пролиферация приводит к созданию большого пула клеток, которые называют дважды негативными клетками, поскольку они не несут на себе корецепторы CD4 и CD8. Большинство из них (90 %) дадут начало αβ Т-лимфоцитам, а 10 % — γδ Т-лимфоцитам.
После этого тимоциты приступают к перестройке генов антигенных рецепторов. Это тот самый момент, когда из небольшого количества генов возникает всё разнообразие антигенных рецепторов — миллионы и миллиарды. В ходе этого процесса участки генов антигенных рецепторов перестраиваются случайным образом. Ключевое слово здесь — случайный, поскольку процесс формирования рецепторов, способных эффективно распознавать чужеродные антигены, никак не зависит от этих антигенов и происходит задолго до встречи с ними!
До сих пор тимоциты содержали гены TCR в зародышевой конфигурации, т. е. не подвергшиеся перестройке. Такие гены не могут образовать TCR. Тимоциты начинают с перестройки генов одной из двух цепей TCR — β-цепи. После этого тимоциты проходят через первую контрольную точку. В случае успешной перестройки клетка экспрессирует β-цепь, которая вместе с инвариантной α-цепью формирует на поверхности клетки pre-TCR. Такой рецептор активируется без участия лиганда и передает в клетку сигналы для дальнейшего развития. Остальные клетки не проходят отбор: в случае неудачной перестройки pre-TCR не экпрессируется и клетка подвергается апоптозу в отсутствие сигналов к выживанию.
Активация pre-TCR поставляет в клетку важные сигналы для дальнейшего развития:
- Останавливается перестройка локуса β-цепи во втором аллеле. Это называется аллельное исключение — зрелые Т-лимфоциты экспрессируют β-цепь TCR только с одного аллеля.
- Начинается экспрессия двух ко-рецепторов CD4 и CD8, теперь тимоциты называются дважды позитивными.
- Начинается второй раунд пролиферации. Через pre-TCR клетки получают мощный сигнал к делению, приводящий к еще более интенсивной экспансии, чем в первом раунде.
- После этапа деления запускается перестройка α-цепи рецептора.
В отличие от цепи-партнера, α-цепь может подвергаться многократной перестройке, и большинство тимоцитов успешно с ней справятся. После перестройки α-цепи тимоциты наконец экспрессируют на своей поверхности полный αβ TCR. Однако впереди главная проверка, пройти которую суждено немногим.
Задачи последнего этапа отбора:
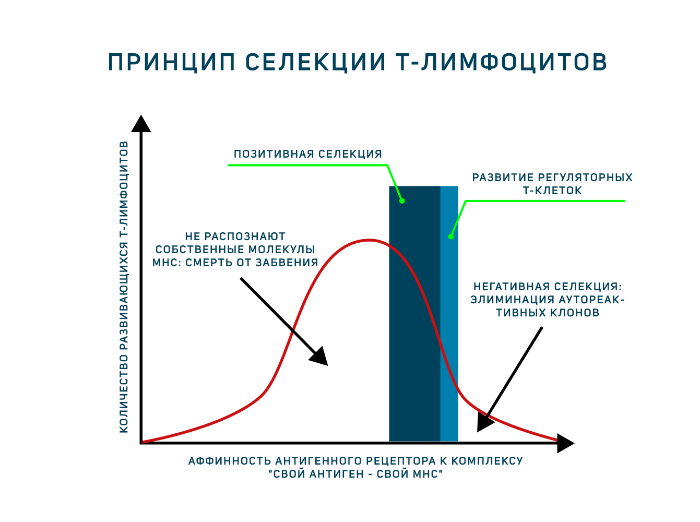
- Отобрать клетки, распознающие молекулы главного комплекса гистосовместимости (MHC) организма. Этот этап присутствует в развитии тимоцитов, поскольку зрелые Т-лимфоциты способны распознавать антигены только в составе МНС. Поэтому они должны знать МНС своего организма в лицо. Это называется позитивная селекция.
- Элиминировать клетки, распознающие собственные антигены. Это называется негативная селекция.
Однако антигенпрезентирующие клетки тимуса (эпителиальные клетки тимуса, дендритные клетки и макрофаги) располагают только комплексами «свой МНС — свой антиген». И позитивная, и негативная селекция осуществляется на основании взаимодействия TCR с такими комплексами! Для объяснения была предложена гипотеза аффинности. Тимоциты, чьи антигенные рецепторы проявят низкую аффинность к таким комплексам, продолжат развитие. Тимоциты, чьи рецепторы свяжутся с представленными антиген-МНС комплексами прочно, подвергнутся апоптозу как аутореактивные клоны (клональная делеция). Клетки, не распознающие МНС вовсе, т. е. не прошедшие позитивную селекцию, умрут особым способом, который называется смерть от забвения (death by neglect). Ещё один вариант развития — среднее связывание рецептора с антигенным комплексом, такие тимоциты могут дать начало регуляторным Т-клеткам. Таким образом, регуляторные Т-клетки — единственные лимфоциты, которые взаимодействуют со своим будущим антигеном в процессе развития! Развитию этого подтипа Т-лимфоцитов сейчас посвящено много исследований.

Особую роль в негативной селекции играет белок AIRE (аутоиммунный регулятор), который заставляет клетки тимуса экспрессировать в небольших количествах антигены, в норме присутствующие только в определенных тканях. Это позволяет сформировать толерантность к тканеспецифичным антигенам, встречающимся только за пределами тимуса. Мутация в белке AIRE приводит к развитию аутоиммунного полиэндокринного синдрома. AIRE содержится в эпителиальных клетках медуллы. При этом известно, что наиболее эффективно негативная селекция осуществляется при презентации антигена дендритными клетками и макрофагами, а не стромой тимуса. В новом исследовании был показан перенос антигенов из эпителиальных клеток тимуса в дендритные клетки, которые их и презентируют!
Одновременно с позитивной и негативной селекцией осуществляется проверка, соответствует ли корецептор распознаваемому классу МНС — т. е. происходит дифференцировка в функциональные подклассы. Выживают только клетки с правильной комбинацией: CD8 + MHC I — цитотоксические Т-лимфоциты и CD4 + MHC II — Т-хелперы.
Последнее, что должен сделать лимфоцит перед тем, как покинуть тимус — это изменить тип сигналинга через антигенный рецептор. Если незрелые Т-лимфоциты с высоким родством к антигену погибают, то зрелые — активируются (молекулярные основы такой принципиальной разницы не ясны). Теперь лимфоциты готовы заселить периферические лимфоидные органы и нести оборону. Зрелые Т-лимфоциты покидают тимус, используя градиент сфингозин-1-фосфата, — липида, присутствующего в высоких концентрациях в крови и лимфе, для хемотаксиса в кровяное русло. Для хоуминга во вторичные лимфоидные ткани они используют CD62L (L-селектин).
γδ Т-лимфоциты несут менее разнообразные антигенные рецепторы, по-видимому, не зависящие от МНС. Они не экспрессируют корецепторы CD4, CD8. γδ Т-лимфоциты выступают в роли первой линии обороны против часто встречающихся бактерий в эпителиальных и слизистых тканях и скорее относятся ко врожденной иммунной системе, чем к адаптивной.
Источники:
- Kenneth Murphy, Casey Weaver. Janeway’s Immunobiology 9th edition. Garland Science, 2017.
- Abul Abbas, Andrew H. Lichtman, Shiv Pillai. Cellular and Molecular Immunology 9th Edition. Elsevier, 2017.
- Perry J. S. et al. CD36 Mediates Cell-Surface Antigens to Promote Thymic Development of the Regulatory T Cell Receptor Repertoire and Allo-tolerance //Immunity. – 2018. – 923-936.
Источник
Гематология: Развитие Т-лимфоцитовПредшественники, прекоммитированные к развитию в Т-лимфоциты, непрерывно мигрируют от костного мозга в вилочковую железу, однако их число, по-видимому, очень мало. Незрелые предшественники Т-клеток поступают в область коры вилочковой железы, где созревают в функциональные субпопуляции Т-клеток. Особенностью развития тимоцитов является высокая скорость пролиферации. Различные стадии развития тимоцита можно определить по изменению экспрессии поверхностных и цитоплазматических молекул, рецепторов цитокинов и состояния реаранжировки генов Т-клеточного рецептора. Т-клеточный рецептор (TCR) распознает только короткие пептиды, которые заполняют полость в молекулах первого или второго класса главного комплекса гистосовместимости (МНС I и II, МНС комплекс у человека обозначается как HLA). Презентация таких пептидов Т-лимфоцитам обеспечивается антигенпредставляющими клетками. TCR — гетеродимерный комплекс, сформированный при ассоциации а-и бета- или у- и S-субъединиц. Каждая из этих субъединиц кодируется отдельным геном. Т-клетки с рецепторами типов ар и уq являются различными линиями, которые разделяются до начала реаранжировки гена TCR. Наименее зрелые клетки-предшественники в вилочковой железе экспрессируют антиген CD7. Некоторые из них экспрессируют также CD44. CD44, рецептор для гиалуроновой кислоты, — один из факторов, определяющих перемещение предшественников Т-клеток в вилочковую железу. Из этих предшественников далее образуются CD2+/CD7+ клетки, в цитоплазме которых присутствует CD3. Белковый комплекс CD3 обеспечивает передачу сигналов через TCR. Пептидные цепи CD3-комплекса начинают синтезироваться на стадии про-Т-лимфоцита, и их экспрессия предшествует появлению на мембране TCR. Т-лимфоциты уq-линии первыми начинают экспрессировать рецептор CD3, но на них нет молекул CD4 или CD8. Несколько позднее на поверхности клеток, экспрессирующих рецептор типа аb, начинают одновременно экспрессироваться антигены CD4 и CD8. К этому времени заканчивается реаранжировка генов а- и р-цепей, и на поверхности клеток экспрессируется рецепторный комплекс TCR ab/CD3. По мере того как клетки, экспрессирующие CD4+, CD8+ и TCR (так называемые дважды положительные клетки), проходят от коры к мозговому веществу вилочковой железы, они созревают в CD4+ хелперные или CD8+ цитотоксические Т-клетки. Клетки, которые созревают до стадии CD4+ или CD8+, составляют менее 5% тимоцитов. Эти лимфоциты покидают вилочковую железу и заполняют вторичные лимфоидные ткани (лимфатические узлы, селезенку, лимфоидную ткань, ассоциированную со слизистыми оболочками). Т-лимфоциты с рецептором уq и CD5+B1-клетки являются функционально аналогичными популяциями, которые развиваются параллельно. Т-клетки с рецептором типа уq найдены в различных тканях, включая селезенку, эпидермис и эпителий слизистой оболочки матки, влагалища и языка. Предполагается, что эта популяция клеток может исполнять роль иммунного надзора в перечисленных тканях.
Формирование комплекса Т-клеточного рецептора и положительная и отрицательная селекция в вилочковой железеКак и гены иммуноглобулинов, гены Т-клеточного рецептора собираются из различных сегментов, находящихся первоначально в зародышевой конфигурации. Гены Т-клеточного рецептора подвергаются процессу соматической реаранжировки, при которой кодирующие сегменты присоединяются друг к другу, а присутствующие между ними интронные последовательности удаляются. Вариабельность соединений и вставок обеспечивает возникновение различий TCR и приводит к огромному количеству различных последовательностей гипервариабельного участка TCR. Репертуар различных TCR считается даже большим, чем репертуар молекул Ig (по оценкам, репертуар ab-TCR составляет 1015, а для yq-TCR — 1018). В отличие от В-лимфоцитов, Т-лимфоциты не секретируют свои рецепторы. Дважды позитивный тимоцит проходит через многоступенчатый процесс, известный как тимическая селекция. На первой фазе, называемой положительной селекцией, TCR дважды позитивного тимоцита взаимодействуют с молекулами МНС, которые экспрессируются эпителиальными клетками в коре вилочковой железы. Тимоциты, способные распознавать комплекс антигена с молекулой HLA, ускользают от апоптоза и вступают в дальнейшую дифференцировку, в то время как тимоциты, не способные к такому взаимодействию, погибают. Поскольку рекомбинации, затрагивающие возникновение TCR, являются случайными, в вилочковой железе могут развиваться и пройти позитивную селекцию Т-клетки, экспрессирующие TCR, специфичные к чужеродным и собственным антигенам. Существует вероятность, что Т-клетки, реактивные к собственным структурам организма, будут взаимодействовать с аутоантигенами в тканях, что может привести к нежелательным аутоиммунным реакциям. Для предотвращения этого дважды положительные клетки подвергаются второй фазе отбора, которая называется негативной селекцией. В ходе этой фазы дважды положительные клетки взаимодействуют с комплексом МНС-пептид, экспрессированным на поверхности дендритной клетки. Т-клетки, TCR которых взаимодействует с комплексом МНС-пептид с высокой аффинностью, подвергаются апоптозу. В ходе негативной селекции удаляются Т-клетки, экспрессирующие TCR, обладающие реактивностью к собственным антигенам. Дважды положительные клетки, пережившие негативную селекцию, снижают экспрессию корецепторов CD4 или CD8, что приводит к развитию или CD4+CD8″ или CD4″CD8+ (моноположительных) Т-лимфоцитов. При этом Т-лимфоциты, распознающие антигены, представляемые молекулами МНС II класса, сохраняют экспрессию корецептора CD4+, a Т-лимфоциты, распознающие антигены, представляемые молекулами МНС I класса, сохраняют экспрессию корецептора CD8+. Эти клетки покидают вилочковую железу и образуют периферические зрелые CD4+ и CD8+ Т-клетки.
Клетки и цитокины, регулирующие развитие Т-клетокВилочковая железа состоит из корковой и медуллярной областей, различающихся по количеству тимоцитов и составу стромальных клеток. Стромальные клетки вилочковой железы влияют на развитие тимоцитов как посредством прямых межклеточных взаимодействий, так и секрецией растворимых медиаторов. Тимоциты и клетки тимического эпителия экспрессируют ряд поверхностных клеточных детерминант, некоторые из которых вовлечены в адгезию этих клеточных популяций друг к другу. Рецептор CD2 на тимоцитах определяет связывание с детерминантой CD58 (LFA-3) и межклеточной адгезионной молекулой-1 (ICAM-1), представленными на клетках тимического эпителия. Взаимодействия между развивающимися лимфоцитами и стромой могут активировать обе популяции. Например, связывание тимоцитов со стромой может стимулировать продукцию ИЛ-1 стромальными клетками и повышать экспрессию рецептора ИЛ-2 на тимоцитах. ИЛ-7 стимулирует полиферацию тимоцитов, и фактор стволовых клеток увеличивает этот эффект. Эпителиальные клетки вилочковой железы у человека являются источником цитокинов ИЛ- 1а и b, ИЛ-3, ИЛ-6, ИЛ-8, колониестимулирующих факторов (Г-КСФ и ГМ-КСФ), лейкозингибирующего фактора (LIF) и TGF-p, а также гормонов тимозина или тимопоэтина, оказывающих влияние на пролиферацию и дифференцировку тимоцитов. Цитокины, необходимые для развития Т-клеток, могут продуцироваться самими Т-клетками. Тимоциты производят IFN-y, ФНО-а, ИЛ-2, ИЛ-3 и ИЛ-4. Естественные киллерные клетки. Естественные киллеры (NK) обладают способностью спонтанно лизировать некоторые опухолевые клетки-мишени. Человеческие NK-клетки экспрессируют CD16 и CD56, но не имеют TCR или CD3. По морфологическим характеристикам эти клетки представляют собой большие гранулярные лимфоциты (в них присутствуют крупные цитоплазматические гранулы). NK-клетки имеют гемопоэтическое происхождение и развиваются в костном мозге, но пока мало известно об их предшественниках. – Также рекомендуем “Гематология: Развитие лимфоцитов в лимфатических узлах и селезенке” Оглавление темы “Гематология”:
|
Источник
Оглавление темы “Иммунная система. Функции клеток иммунной системы. Т-лимфоциты. В-лимфоциты. Структура и функции органов иммунной системы.”: Т-лимфоциты. Характеристика Т-лимфоцитов. Типы молекул на поверхности Т-лимфоцитов.Решающее событие в развитии Т-лимфоцитов — формирование антигенраспознающего Т-клеточного рецептора — происходит только в тимусе. Для обеспечения возможности распознавания любого антигена нужны миллионы различных по специфичности антигенраспознающих рецепторов. Формирование огромного разнообразия антигенраспознающих рецепторов возможно благодаря перестройке генов в процессе пролиферации и дифференцировки клеток-предшественниц. По мере созревания Т-лимфоцитов на их поверхности появляются ан-тигенраспознающие рецепторы и другие молекулы, опосредующие их взаимодействие с антигенпредставляющими клетками. Так, в распознавании собственных молекул главного комплекса гистосовместимости наряду с Т-клеточным рецептором участвуют молекулы CD4 или CD8. Межклеточные контакты обеспечиваются наборами поверхностных адгезионных молекул, каждой из которых соответствует молекула — лиганд на поверхности другой клетки. Как правило, взаимодействие Т-лимфоцита с антигенпредставляющей клеткой не ограничивается распознаванием антигенного комплекса Т-клеточным рецептором, а сопровождается связыванием других попарно комплементарных поверхностных «костимулирующих» молекул. Таблица 8.2. Типы молекул на поверхности Т-лимфоцитов
Сочетание поверхностных молекул лимфоцитов, которые принято обозначать порядковыми номерами «кластеров дифференцировки» (clusters of differentiation — CD), обозначается как «поверхностный фенотип клетки», а отдельные поверхностные молекулы называют «маркерами», так как они служат метками конкретных субпопуляций и стадий дифференцировки Т-лимфоцитов. Так, например, на поздних этапах дифференцировки одни Т-лимфоциты утрачивают молекулу CD8 и сохраняют только CD4, а другие утрачивают CD4, а сохраняют CD8. Поэтому среди зрелых Т-лимфоцитов различают CD4+ (Т-хелперы) и CD8+ (цитотоксические Т-лимфоциты). Среди циркулирующих в крови Т-лимфоцитов клеток с маркером CD4 примерно в два раза больше, чем клеток с маркером CD8. Зрелые Т-лимфоциты несут на поверхности рецепторы для разных цитокинов и рецепторы для иммуноглобулинов (табл. 8.2). При распознавании Т-клеточным рецептором антигена Т-лимфоциты получают сигналы активации, пролиферации и дифференцировки в направлении клеток-эффекторов, т. е. клеток, способных непосредственно участвовать в защитных или повреждающих эффектах. Для этого на их поверхности резко возрастает количество адгезионных и костимулирующих молекул, а также рецепторов для цитокинов. Активированные Т-лимфоциты начинают продуцировать и секретировать цитокины, активирующие макрофаги, другие Т-лимфоциты и В-лимфоциты. После завершения инфекции, сопряженной с усиленной продукцией, дифференцировкой и активацией Т-эффекторов соответствующего клона, в течение нескольких дней 90 % эффекторных клеток погибают, поскольку не получают дополнительных сигналов активации. В организме остаются долгоживущие клетки памяти, несущие соответствующие по специфичности рецепторы и способные ответить пролиферацией и активацией на повторную встречу с тем же антигеном. – Также рекомендуем “Популяции Т-лимфоцитов. Субпопуляции Т-лимфоцитов. СD4 Т-лимфоциты. СD8 Т-лимфоциты..” |
Источник