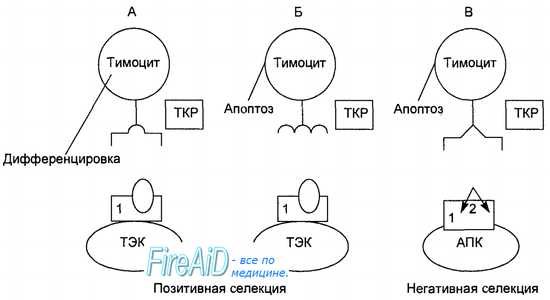
Этапы дифференцировки т лимфоцитов в тимусе
В процессе дифференцировки Т-лимфоцитов выделяют два основных этапа (как Вы помните, такие же два этапа выделяют в процессе дифференцировки В-лимфоцитов):
1. Антигеннезависимая дифференцировка – происходит постоянно в тимусе.
2. Антигензависимая дифференцировка – происходит в периферических органах иммунной системы только при контакте Т-лимфоцита с антигеном.
АНТИГЕННЕЗАВИСИМАЯ ДИФФЕРЕНЦИРОВКА Т-ЛИМФОЦИТОВ
Родоначальной клеткой Т-лимфоцитов, как и всех клеток крови, является полипотентная стволовая гемопоэтическая клетка. Её маркером является CD 34
Ранние предшественники Т-лимфоцитов мигрируют из костного мозга в тимус, где происходитантигеннезависимая дифференцировка Т-клеток под влиянием
«клеток нянек», эпителиальных клеток тимуса, а так же гормонов тимуса (α- и β-тимозины, тимулин /сывороточный фактор тимуса/, тимопоэтин, тимический гуморальный фактор).
Самыми ранними маркерами тимоцитов являются CD7, CD2. В тимусе Т-лимфоциты дифференцируются в иммунокомпетентные клетки и приобретают важную способность к распознаванию антигена. На их наружной мембране появляется (экспрессируется) особый рецептор – Т- клеточный рецептор (ТКР, англ. – TcR, T-cell receptor) для антигена. Причем для каждого антигена (эпитопа) в организме предназначен отдельный лимфоцит или его клональные дочерние лимфоциты-потомки, которые имеют специфичный антигену TcR. Тимоциты одновременно с TcR в процессе дифференцировки приобретают CD3, который тесно связан с Т-клеточным рецептором. CD3 необходим для передачи сигнала от ТКР в цитоплазму.
На поверхности тимоцитов появляются также молекулы CD8 и CD4. Это двойные позитивные клетки, т.е. их фенотип (ТКР+, CD3+, CD4+, CD8+)и они являются молодыми тимоцитами.
По своему строению молекулы TcR (ТКР) напоминают иммуноглобулины (Fab-фрагмент) и состоят из альфа- и бета- цепей (TcR αβ их подавляющее большинство) или гамма- и дельта- цепей (TcR γδ). αβ- и γδ – формы TcR весьма сходны по структуре. Каждая цепь ТКР состоит из двух областей (доменов): наружный вариабельный (V) , второй – константный (С). Отдельные гены кодирующие всю вариабельную область (V) α и β цепей TcR отсутствуют. Фрагменты вариабельных доменов кодируются тремя группами генов обозначаемых V, D, J. В клеточном геноме гены, кодирующие V-, J- и D-сегменты вариабельной области, представлены в виде многочисленных вариантов. Именно различные сочетания V-, J- и D-сегментов V области, образующиеся в процессе генной перестройки, называемой реаранжировкой, обеспечивают разнообразие молекул ТКР. Таким образом, ограниченное число генов (около 400) может кодировать рецепторы для почти бесконечного числа антигенов (многих миллионов). Причем различные комбинации генов V, D, J –сегментов – это только один из способов достижения многообразия антигенных рецепторовТ-лимфоцитов.
Основная функция зрелых Т-лимфоцитов – распознавание чужеродных антигенных пептидов в комплексе с собственными антигенами главного комплекса гистосовместимости (ГКГС) на поверхности антигенпрезентирующих клеток или на поверхности любых клеток-мишеней организма. Для выполнения этой функции Т-лимфоциты должны быть способны распознавать собственные антигены ГКГС. В то же время, Т- клетки не должны распознавать аутоантигены самого организма, связанные с собственными антигенами ГКГС. В связи с этим в тимусе молодые тимоциты проходят селекцию («отбор»), TcR которых соответствует вышеуказанным условиям.
,Позитивная селекция. Т-лимфоциты, ТКР которых обладает способностью распознавать HLA (молекулы ГКГС) стромальных клеток тимуса, выживают, а если нет – то гибнут путем апоптоза. Позитивная селекция – поддержка избирательной выживаемости. Таким образом, выживают только лимфоциты способные распознавать собственные HLA! И эта способность в последующем является важной в функционировании Т- клеток.
Кроме этого в тимусе погибают путем апоптоза аутореактивные лимфоциты (лимфоциты имеющие ТКР к антигенным детерминантам собственных тканей). Важно, что при контакте с эпителиоидными клетками тимуса Т-лимфоциты, реагирующие на «своё», разрушаются путем запуска апоптоза (запрограммированной клеточной смерти при активации через CD95 – Fas рецептор). Это отрицательная селекция. В итоге, исчезают аутореактивные клоны клеток и возникает толерантность (неотвечаемость) к «своему». В тимусе около 95 – 97% лимфоцитов погибают в результате процесса селекции.
В последующем одна из молекул CD4 или CD8 утрачивается и клетки становятся зрелыми. Клетки сохранившие CD4 являются Т-хелперами (Тh) и их ТКР распознает HLAII класса, а сохранившие CD8 – цитотоксическими Т-лимфоцитами и их ТКР обладает способностью распознавать HLAI класса. Из тимусаони мигрируют в периферические лимфоидные органы, где заселяют преимущественно Т-зависимые зоны. В частности в лимфоузлах – паракортикальную. Зрелые лимфоциты рециркулируют.
Таким образом, АНТИГЕННЕЗАВИСИМАЯ дифференцировка Т-лимфоцитов включает в себя пролиферацию, приобретение специфических маркеров Т-лимфоцитами и образование дифференцированных, зрелых субпопуляций, способных осуществлять характерные для той или иной субпопуляции функции (индукция иммунного ответа, его регуляция, цитотоксичность). В процессе антигеннезависимой дифференцировки образуются лимфоциты, которые генетически детерминированы к взаимодействию с определенным антигеном и иммунному ответу на этот антиген.
АНТИГЕНЗАВИСИМАЯ ДИФФЕРЕНЦИРОВКА Т-ЛИМФОЦИТОВ
Антигензависмая дифференцировка происходит в периферических органах иммунной системы, если Т- лимфоцит провзаимодействовал с антигеном. Начинается она с момента распознавания антигена и заканчивается образованием клона лимфоцитов, способных оказывать специфическое действие как по отношению к антигену, так и к другим иммунокомпетентным клеткам, вступившим во взаимодействие с антигеном. Причем хелперы и цитотоксические лимфоциты распознают антиген по-разному. Так, ХЕЛПЕРЫ (CD4–клетки) распознают АНТИГЕН в комплексе с HLA II КЛАССА, КИЛЛЕРЫ (CD8-клетки) – в комплексе антиген с HLA 1 КЛАССА. Распознавание антигена Т-хелпером является центральным процессом, как в гуморальном иммунном ответе, так и в усилении клеточной формы иммунного ответа.
Специфическими МАРКЕРАМИ для ВСЕЙ ПОПУЛЯЦИИ Т-ЛИМФОЦИТОВ являются имеющиеся на наружной мембране этих клеток антигены CD 3. (Раньше использовался маркер CD 2 – рецептор для эритроцитов барана, что не совсем корректно. Параметры CD антигенов смотри вприложении.)
CD8+ – на Т-цитотоксических
Маркер Т-лимфоцитов – структура, которая свойственна только Т-лимфоцитам (всем субпопуляциям Т-лимфоцитов) – CD3.
СУБПОПУЛЯЦИИ ЛИМФОЦИТОВ:
Тh лимфоциты. Примерно половина из числа циркулирующих Т-лимфоцитов несут на своей поверхности антиген CD4 . Эти Т-лимфоциты функционируют как ХЕЛПЕРЫ, то есть помощники (от англ. tohelp — помогать), «включающие» популяцию В-лимфоцитов в процесс выработки антител, а Т-эффекторы – в реализацию клеточного иммунитета. Т-хелперы опосредуют свою функцию гуморальными факторами – цитокинами, которые синтезируются этими лимфоцитами в ответ на антигенный стимул.
Недостаточность хелперной функции Т-лимфоцитов, наблюдаемая при синдроме приобретенного иммунодефицита (СПИД, одной из важнейших мишеней ВИЧ являются Т-лимфоциты хелперы), приводит к
«неотвечаемости» организма на антигенную стимуляцию, что, в конечном итоге, способствует персистенции в организме человека микроорганизмов, развитию злокачественных новообразований и является причиной летального исхода.
Т-хелперы (Th) – стимулируют пролиферацию и дифференцировку как Т-, так и В-лимфоцитов, выделяя цитокины. В зависимости от того, какие цитокины они продуцируют (в зависимости от цитокинового профиля) среди них различают:
Th1 (Т-хелперы первого типа), выделяют ИЛ-2 и γ-интерферон, и в итоге обеспечивают реакции Т- клеточного иммунитета – стимулируют иммунный ответ против внутриклеточных бактерий, противовирусный, противоопухолевый, трансплантационный иммунитет.
Th2 (Т-хелперы второго типа), секретируют ИЛ-4, ИЛ-5, ИЛ-6, ИЛ-10, ИЛ-13 и стимулируют синтез антител, способствуют развитию гуморального иммунного ответа против внеклеточных бактерий, их токсинов, а также образованиеIgE-антител.
Между Th1 и Th2 существует антагонизм: при повышении активности одних, угнетается функция других. В итоге преобладает Т-клеточный (Th1T киллеры) или В-клеточный (Th2 В-лимфоциты
антитела) иммунитет, что во многом зависит от вида антигена. Таким образом, Т-
хелперы выполняют хелперно-регуляторную функцию во взаимодействии иммунокомпетентных клеток, направленную на развитие эффекторной фазы иммунного ответа. Именно от Th зависит будет преобладать гуморальный или клеточный иммунный
ответ.
Тk. Среди субпопуляций Т-лимфоцитов различают эффекторные клетки. В связи с тем, что эти эффекторные клетки способны специфически разрушать клетки-мишени, их называют ЦИТОТОКСИЧЕСКИМИ Т-ЛИМФОЦИТАМИ, или Т-КИЛЛЕРАМИ – убийцами (от англ. tokill – убивать).
Т-киллер —одна из основных эффекторных клеток клеточноопосредованного иммунитета, которая наряду с другими клетками способна осуществлять лизис клеток мишеней. Роль Т-киллеров очень велика в реализации трансплантационного иммунитета, развитии аутоиммунных заболеваний, в противоопухолевой защите. Тk- лимфоциты (CD8+ клетки) составляют около 20 – 25% от числа циркулирующих Т-лимфоцитов (абсолютное количество – 500 – 1200 в 1 мм3 (мкл)), они несут маркерный антиген CD8 . Макромолекула CD8 служит корецептором для антигенов главного комплекса гистосовместимости I класса (ГКГС-1).
Активированные антигеном цитотоксические клетки – Т- киллеры связываются с антигенами на поверхности клеток и, выделяя белок перфорин, разрушают их. При этом Т-киллер остается жизнеспособным и может разрушать следующую клетку. Действие перфорина подобно МАК системы комплемента. Белок перфорин, полимеризуясь в мембране клетки-мишени, образует поры – каналы, тем самым, вызывая её осмотический лизис. Кроме того, цитотоксический Т-лимфоцит через пору, образованную перфорином в клетке-мишени, вбрасывает гранзимы (ферменты – сериновые протеазы), которые запускают программу апоптоза. Установлено также, что своё цитотоксическое действие Т- лимфоциты могут реализовывать путем экспрессии FasL и с его помощью индуцировать Fas-опосредованный апоптоз мишени.
«Наивные» Т-лимфоциты – это те лимфоциты, которые не встретились с антигеном и они составляют часть общего пула рециркулирующих Т-клеток.
Т-клетки иммунологической памяти – это долгоживущие лимфоциты, потомки клеток, встречавшихся с антигенами и сохраняющие к ним рецепторы.
Т-ЛИМФОЦИТЫ ИММУНОЛОГИЧЕСКОЙ ПАМЯТИ – после стимуляции антигеном способны сохранять информацию о нем до 10—15 лет и передавать ее другим клеткам. Эти клетки защищены от апоптоза. Благодаря наличию в организме Т-клеток памяти обеспечивается ускоренный иммунный ответ по вторичному типу при повторном попадании данного антигена в организм. Этим объясняется форсированная динамика вторичного иммунного ответа. Маркером Т- лимфоцитов памяти является мембранный антигенCD45RO.
Раньше ошибочно выделяли субпопуляцию Т-супрессоров, которые считались ответственными за подавление иммунного ответа. Однако в настоящее время показано, что самостоятельной субпопуляции Т- супрессоров нет. В угнетении, подавлении иммунного ответа решающее значение играет апоптоз простимулированных лимфоцитов, а также цитокин – трансформирующий фактор роста β.
Около 10 % лимфоцитов не имеют ни Т-, ни В-маркеров, они не относятся ни к Т-, ни к В-лимфоцитам и ранее получили название НУЛЕВЫЕ ЛИМФОЦИТЫ . Эта разнородная популяция лимфоцитов в зависимости от их морфофункциональных особенностей подразделяется на:
l ЕСТЕСТВЕННЫЕ (natural) КИЛЛЕРНЫЕ КЛЕТКИ (сокращенно ЕКК=ЕК=NK-клетки) и
l КИЛЛЕРНЫЕ КЛЕТКИ (К-клетки).
Общей особенностью НК- и К-клеток является способность лизировать клетки-мишени без предварительной сенсибилизации, что необходимо Т-лимфоцитам-киллерам. Морфологически это лимфоциты большого размера с зернистой цитоплазмой. Дифференцируются из общей клетки предшественника лимфоцитов (LSC).
Естественные киллеры не зависят в своем развитии от вилочковой железы. Экспрессируют на своей поверхности рецепторы к интерферону-γ и интерлейкину-2 (ИЛ 2). Функционально они являются цитотоксическими клетками киллерами, но на NK нет антигенраспознающих рецепторов, которые обязательно присутствуют на Т-киллерах. Натуральных киллеров на клетку мишень наводят антитела IgG специфичные к мембранным антигенам клетки-мишени. Первоначально антитела связываются с антигеном на клетке, а затем с помощью Fc рецептора к IgG (FcγRIII) NK присоединяется к этому комплексу АТ – АГ-клетки-мишени. Функция НК-клеток в организме заключается в защите от развития опухолей, вирусов и др.
Основными их маркерами являютсяCD16 и CD56. (FcγRIII по CD- номенклатуре это CD16).
Разрушение клетки-мишени ЕК осуществляет с помощью перфорина. Содержание ЕК (CD16+ клеток) у здоровых людей – 8 – 22%.
К-клетки неоднородная группа клеток, несущая на своей поверхности рецепторы к Fc- фрагменту Ig G и способны к антителозависимой клеточной цитотоксичности. К ним относятся моноциты, нейтрофилы, макрофаги, эозинофилы, конечно НК и некоторые лимфоциты.
Антителозависимая клеточноопосредованная цитотоксичность (АЗКЦ) является своеобразным отражением связи между гуморальным и клеточным звеньями иммунной системы. Антитела выступают в роли«наводчиков» клеток-эффекторов на клетки-мишени, несущие чужеродные антигены.
Все лимфоциты (Т-, В-, НК- и К-клетки) обладают способностью к миграции и рециркуляции (см. методическую, что обеспечивает повсеместный контроль за размножением клеток собственного организма, а при проникновении чужеродного антигена —генерализированный иммунный ответ и сохранение иммунологической памяти обантигене.
Источник
Стволовая гемопоэтическая клетка, мигрирующая в тимус,
превращается (дифференцируется) под влиянием тимического микроокружения в
Т-лимфоцит. Цель дифференцировки:
- обучить распознаванию чужеродного
материала, попавшего в организм, и его разрушению (т. е. осуществлению
киллинг-эффекта); - создать толерантность по отношению к собственным (self)
антигенам. тимус играет главную роль в этих процессах, поскольку является тем
органом, где про¬исходит антигеннезависимая дифференцировка Т-клеток и создание
(генерирование) чрезвычайно разнообразного набора (репертуара)
антигенраспознающих Т-клеточных рецепторов.
Вначале стволовая гемопоэтическая клетка попадает в корковую
зону тимуса и превращается в ранний предшественник Т-лимфоцита. Фенотип этой
клетки следующий: ТАГРР-альфа, бета +, CD3+ CD4-, CD8-, т. е. характеризуется
наличием Т-клеточного распознающего рецептора, в составе которого имеются
альфа- и бета-цепи, CD3 структура, но отсутствуют молекулы CD4 и CD8.
Далее, здесь же в корковой зоне тимуса, под влиянием тимического
микроокружения, гормонов тимуса и, особенно, ИЛ-7 ранний предшественник
Т-лимфоцита превращается в незрелый Т-лимфоцит, фенотип которого следующий:
ТАГРР-альфа, бета +, CD3+, CD4+, CD8+. Набор таких мембранных структур говорит
о том, что данная клетка способна: 1) распознать любой антиген с помощью
ТАГРР-альфа, бета; 2) после распознавания передать сигнал внутрь клетки для ее
активации с помощью CD3 структуры: 3) превратиться как в CD4+ (хелпер), так и в
CD8+ (киллер) клетки при развитии эффекторного звена иммунного ответа.
На следующем этапе
дифференцировки незрелый предшественник Т-лимфоцита переходит в мозговое
вещество тимуса, где завершается тимический этап созревания. При этом
происходят два важнейших события: 1) индуцируется толерантность к аутоантигенам;
таким образом, минимизируется возможность развития аутоиммунного заболевания;
2) происходит разделение Т-лимфоцитов на две субпопуляции: CD4+CD8- (хелперы) и
CD4-CD8+ (киллеры) (не нужно за-бывать, что на их мембране сохраняются молекулы
ТАГРР-альфа, бета и CD3). Этот этап также реализуется при важном участии ИЛ-7.
Покидая тимус, зрелые покоящиеся Т-лимфоциты, которые
находятся в G(O) стадии клеточного цикла, расселяются в Т-зоны периферических
лимфоидных органов. Такие Т-лимфоциты характеризуется следующими свойствами:
- способностью распознавать чужеродные антигены, которые презентируются ему в
виде пептида с помощью молекул ГКГ класса I и класса II, и развивать
эфферентную часть иммунного ответа; - неспособностью распознавать большинство
аутологичных антигенов, как в растворимой форме, так и в виде молекул на
мембране клеток. Это главное препятствие на пути к развитию аутоиммунного
ответа.
Часть Т-лимфоцитов, покидающих тимус, все же способна распознавать
аутоантигены, однако такие Т-лимфоциты (и В-лимфоциты) либо подвергаются делении
(разрушению) в периферических органах, либо находятся в состоянии анергии
(неспособности к активации и реализации эфферентной части иммунного ответа).
Т-лимфоциты-хелперы (CD4+ клетки) представлены тремя
субпопуляциями: т. н. нулевыми Т-хелперами (Тх0), которые дифференцируются в
Т-хелперы 1-го типа (Tx1) и 2-го типа (Тх2). В этой дифференцировке основную
роль играют ИЛ-12, ИЛ-2, гамма-интерферон, ИЛ-10, ИЛ-4, ИЛ-5.
Т-лимфоциты-хелперы (CD4+ клетки) участвует в распознавании
атигенногопептида , который презентируется с помощью молекул ГКГ класса П. В
этом случае для активации Т-лимфоцита необходим дополнительный,
костимуляционный, сигнал.
Источник
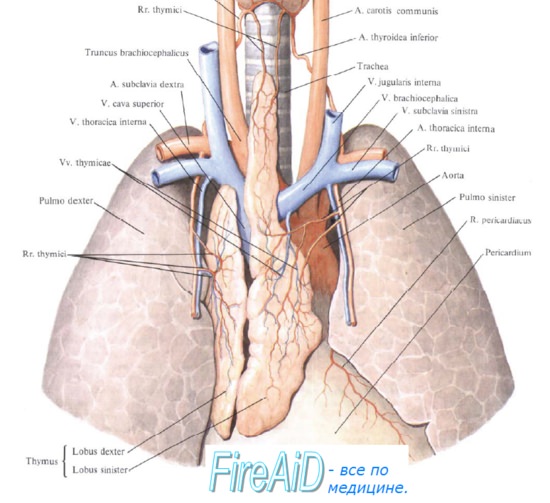
Оглавление темы “Иммунная система. Функции клеток иммунной системы. Т-лимфоциты. В-лимфоциты. Структура и функции органов иммунной системы.”: Тимус (вилочковая железа). Тимоциты. Функции тимуса ( вилочковой железы ). Этапы отбора тимоцитов.Тимус в качестве одного из центральных органов иммунной системы является местом созревания Т-лимфоцитов из клеток-предшественниц и формирования огромного разнообразия зрелых Т-лимфоциов, способных распознать своими рецепторами любой антиген. Лимфоциты, находящиеся в тимусе, называют тимоцитами. В тимусе идут параллельно несколько процессов: Ранние клетки-предшественницы Т-лимфоцитов из костного мозга поступают в корковый слой тимуса. Постепенно они мигрируют из коркового слоя тимуса в мозговой, контактируя с тимическими эпителиальными клетками, макрофагами и дендритными клетками. На тимоциты влияют продуцируемые тимическими эпителиальными клетками гормоны: тимулин, al- и (34-тимозины, тимопоэтин, контролирующие их дифференцировку. В процессе продвижения в мозговой слой тимоциты созревают (дифференцируются), поэтапно приобретая характерные для зрелых Т-лимфоцитов поверхностные рецепторы и антигены.
От стромальных клеток тимуса и продуцируемых ими молекул каждый тимоцит получает сигналы: усиления пролиферации, изменений поверхностного фенотипа (сочетания молекул, присутствующих на поверхности клеток), перестройки («реаранжировки») генов, ответственных за широкое разнообразие специфических антигенраспознающих рецепторов. Основная функция зрелых Т-лимфоцитов — это распознавание чужеродных антигенных пептидов в комплексе с собственными молекулами главного комплекса гистосовместимости на поверхности антигенпредстав-ляющих клеток. Для выполнения этой функции Т-лимфоциты располагают специфическими антигенраспознающими рецепторами. Отбор тимоцитов идет в два этапа (рис. 8.4). После того как на тимоците формируется Т-клеточный рецептор определенной специфичности, в следующие этапы развития вступают только те тимоциты, которые проявили способность распознавать собственные молекулы главного комплекса гистосовместимости, присутствующие на эпителиальных клетках коры тимуса данного организма. В отличие от зрелого Т-лимфоцита, который при встрече с антигенным пептидом, специфичным для его Т-клеточного рецептора, получает сигнал активации, незрелые тимоциты в тимусе при распознавании специфичных для их Т-клеточных рецепторов аутоантигенных пептидов получают сигнал генетически программированной гибели — апоптоза. Таким образом, идет «выбраковка» аутореактивных Т-лимфоци-тов, 95—98 % тимоцитов ежедневно погибают в тимусе этим путем. Только 2—5 % тимоцитов (1 • 10б) в виде зрелых Т-лимфоцитов ежедневно покидают тимус, поступая в кровь и расселяясь в лимфоидных органах.
A. Тимоцит, способный распознать своим рецептором (ТКР) собственные антигены главного комплекса гистосовместимости (1) на поверхности тимических эпителиальных клеток (ТЭК), вступает в дальнейшую дифференцировку. Б. Тимоцит, не способный распознать своим ТКР собственные антигены главного комплекса гистосовместимости (1) на поверхности ТЭК, получает сигнал апоптоза. B. Тимоцит, способный распознать своим ТКР пептидный фрагмент аутоантигена (2) на поверхности антигенпредставляющеи клетки в комплексе с собственными молекулами главного комплекса гистосовместимости (1), получает сигнал апоптоза. В результате в кровоток и в лимфоидные органы поступают только те Т-лимфоциты, которые несут рецепторы, распознающие чужеродные пептиды в сочетании с собственными молекулами главного комплекса гисто-совместимости. Тимус представляет собой единственный орган иммунной системы, подвергающийся быстрой возрастной инволюции, которая у людей начинается после первого года жизни. Человек ежегодно теряет до 3 % истинно тимической ткани, которая постепенно замещается жировой и соединительной тканью. Соответственно снижается и продукция Т-лимфоцитов. Высокая продукция Т-лимфоцитов сохраняется до двух лет, а затем быстро снижается. Однако количество Т-лимфоцитов в организме сохраняется на достигнутом уровне благодаря тому, что значительную часть популяции Т-лимфоцитов составляют долгоживущие клетки, которые не нуждаются в постоянном обновлении. Более того, зрелые Т-лимфоциты, распознавшие «свой» антиген в периферических органах иммунной системы, получают сигналы активации и избирательной пролиферации, за счет чего их численность возрастает. Перенесенная взрослым человеком тимэктомия не приводит к катастрофическому снижению количества циркулирующих Т-лимфоцитов. В качестве одного из центральных органов иммунной системы тимус выполняет следующие функции: а) контролирует пролиферацию, диффе-ренцировку, отбор и окончательное созревание Т-лимфоцитов, б) продуцирует тимические гормоны, влияющие на функции Т-лимфоцитов. – Вернуться в оглавление раздела “Физиология человека.” |
Источник