Эритроциты вырабатываются в лимфатических узлах
Образование эритроцитов. Формирование красных клеток кровиа) Области тела, где формируются эритроциты. В первые недели эмбриональной жизни примитивные ядерные эритроциты формируются в желточном мешке. Примерно с конца второго месяца беременности (середина триместра) главным органом формирования красных клеток крови становится печень, но умеренное количество образуется в селезенке и лимфатических узлах. Затем во время примерно последнего месяца беременности и после рождения красные клетки крови формируются исключительно в костном мозге.
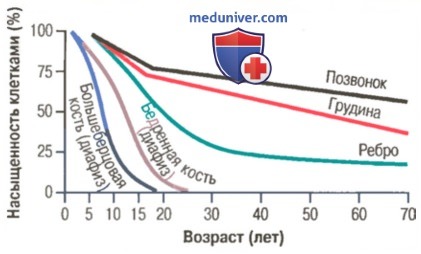
Как показано на рисунке выше, вплоть до 5-летнего возраста эритроциты формируются костным мозгом практически всех костей человека. Постепенно костный мозг всех длинных костей, за исключением проксимальных частей плечевых и большеберцовых, замещается жировой тканью и примерно после 20 лет больше не формирует красных клеток крови. При этом большинство эритроцитов продолжают формироваться в костном мозге мембранозных (плоских) костей, таких как позвоночник, грудина, ребра и подвздошная кость. Но продуктивность костного мозга даже в этих костях с возрастом снижается. Происхождение клеток крови
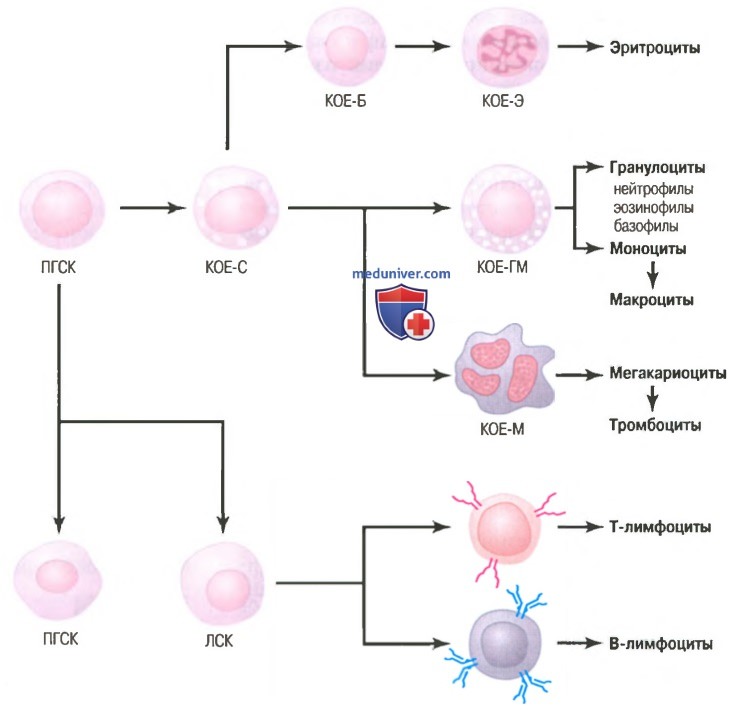
а) Полипотентные гемопоэтические стволовые клетки, индукторы роста и дифференцировки. Все клетки циркулирующей крови начинают свою жизнь в костном мозге от единой так называемой полипотентной гемопоэтической стволовой клетки. На рисунке выше показано последовательное деление полипотентных клеток, в результате которого формируются различные клетки циркулирующей крови. По мере размножения этих клеток небольшая их часть остается в виде оригинальных полипотентных клеток, которые сохраняются в костном мозге, поддерживая их поставку, хотя количество таких клеток с возрастом снижается. Большинство воспроизводимых клеток дифференцируются, формируя другие типы клеток, показанные справа на рисунке выше. Клетки промежуточных стадий очень похожи на полипотентные стволовые клетки, хотя они уже превратились в особую линию клеток и называются унипотентными (коммитированными) стволовыми клетками. Когда дифференцированные унипотентные клетки-предшественники растут в культуре, из них формируются колонии клеток крови специфического типа. Унипотентную стволовую клетку, из которой образуются эритроциты, называют эритроцитарной колониеобразующей единицей, и для обозначения этого типа стволовой клетки используют аббревиатуру КОЕ-Э. Аналогично, колониеобразующие единицы, формирующие гранулоциты и моноциты, обозначают КОЕ-ГМ и т.д. Рост и воспроизведение различных стволовых клеток регулируются множеством белков, называемых индукторами роста. Известны четыре главных индуктора роста, каждый из которых имеет особые характеристики. Один из них — интерлейкин-3 — способствует росту и размножению практически всех типов коммитированных клеток, тогда как другие стимулируют рост только специфических типов клеток. Индукторы роста способствуют росту, но не дифференцировке клеток. Дифференцировка является функцией другого набора белков, называемых индукторами дифференцировки. Каждый из них заставляет коммитированную стволовую клетку специфического типа пройти один или более этапов дифференцировки по направлению к конечной зрелой клетке крови. Формирование самих индукторов роста и дифференцировки регулируется факторами, внешними по отношению к костному мозгу. Например, как обсуждается далее в наших статьях на сайте, длительное снижение кислорода в крови способствует стимуляции роста, дифференцировки и продукции значительного количества эритроцитов. Инфекционные болезни вызывают рост, дифференцировку и конечное формирование специфических типов белых клеток крови, необходимых для борьбы с каждой инфекцией. – Также рекомендуем “Стадии дифференцировки эритроцитов. Влияние эритропоэтина на эритропоэз” Оглавление темы “Заболевания почек. Эритроциты”: |
Источник
Общая гистология – кроветворение
Кроветворением, или гемопоэзом, называют развитие крови. Различают эмбриональный гемопоэз, который происходит в эмбриональный период и приводит к развитию крови как ткани, и постэмбриональный гемопоэз, который представляет собой процесс физиологической регенерации крови.
Развитие эритроцитов называют эритропоэзом, развитие гранулоцитов — гранулоцитопоэзом, тромбоцитов — тромбоцитопоэзом, моноцитов — моноцитопоэзом, развитие лимфоцитов и иммуноцитов — лимфоцито- и иммуноцитопоэзом.
Эмбриональный гемопоэз
В развитии крови как ткани в эмбриональный период можно выделить 3 основных этапа, последовательно сменяющих друг друга – мезобластический, гепатолиенальный и медуллярный.
Первый, мезобластический этап – это появление клеток крови во внезародышевых органах, а именно в мезенхиме стенки желточного мешка, мезенхиме хориона истебля. При этом появляется первая генерация стволовых клеток крови (СКК). Мезобластический этап протекает с 3-й по 9-ю неделю развития зародыша человека.
Второй, гепатолиенальный этап начинается с 5—6-й недели развития плода, когдапечень становится основным органом гемопоэза, в ней образуется вторая генерация стволовых клеток крови. Кроветворение в печени достигает максимума через 5 мес и завершается перед рождением. СКК печени заселяют тимус, селезенку и лимфатические узлы.
Третий, медуллярный (костномозговой) этап — это появление третьей генерации стволовых клеток крови в красном костном мозге, где гемопоэз начинается с 10-й недели и постепенно нарастает к рождению. После рождения костный мозг становится центральным органом гемопоэза.
Рассмотрим подробнее особенности гемопоэза в стенке желточного мешка, в печени, в тимусе, селезенке, лимфатических узлах и в костном мозге.
Кроветворение в стенке желточного мешка
В мезенхиме стенки желточного мешка обособляются зачатки сосудистой крови, иликровяные островки. В них мезенхимные клетки округляются, теряют отростки и преобразуются в стволовые клетки крови. Клетки, ограничивающие кровяные островки, уплощаются, соединяются между собой и образуют эндотелиальную выстилку будущего сосуда. Часть стволовых клеток дифференцируется в первичные клетки крови (бласты). Большинство первичных кровяных клеток митотически делится и превращается в первичные эритробласты, характеризующиеся крупным размером – мегалобласты. Это превращение совершается в связи с накоплением эмбрионального гемоглобина (HbF) в цитоплазме бластов. В некоторых первичных эритробластах ядро подвергается кариорексису и удаляется из клеток, в других ядро сохраняется. В результате образуются безъядерные и ядросодержащие первичные эритроциты, отличающиеся большим размером по сравнению с нормоцитами и поэтому получившие название мегалоцитов. Такой тип кроветворения называется мегалобластическим. Он характерен для эмбрионального периода, но может появляться в постнатальном периоде при некоторых заболеваниях.
Наряду с мегалобластическим в стенке желточного мешка начинается нормобластическое кроветворение, при котором из бластов образуются вторичные эритробласты, из которых образуются вторичные эритроциты (нормоциты).
Развитие эритроцитов в стенке желточного мешка происходит внутри первичных кровеносных сосудов, т.е. интраваскулярно. Одновременно экстраваскулярно из бластов, расположенных вокруг сосудистых стенок, дифференцируется небольшое количество гранулоцитов — нейтрофилов и эозинофилов.
Часть СКК остается в недифференцированном состоянии и разносится током крови по различным органам зародыша, где происходит их дальнейшая дифференцировка в клеткикрови или соединительной ткани. После редукции желточного мешка основным кроветворным органом временно становится печень.
Кроветворение в печени
Печень закладывается примерно на 3—4-й неделе эмбриональной жизни, а с 5-й недели она становится центром кроветворения. Кроветворение в печени происходитэкстраваскулярно, – по ходу капилляров, врастающих вместе с мезенхимой внутрь печеночных долек. Источником кроветворения в печени являются стволовые клетки крови, из которых образуются бласты, дифференцирующиеся во вторичные эритроциты.
Одновременно с развитием эритроцитов в печени образуются зернистые лейкоциты, главным образом нейтрофильные и эозинофильные.
Кроме гранулоцитов, в печени формируются гигантские клетки — мегакариоциты, – предшественники тромбоцитов. К концу внутриутробного периода кроветворение в печени прекращается.
Кроветворение в тимусе
Тимус закладывается в конце 1-го месяца внутриутробного развития, и на 7—8-й неделе его эпителий начинает заселяться стволовыми клетками крови, которые дифференцируются влимфоциты тимуса. Увеличивающееся число лимфоцитов тимуса дает начало T-лимфоцитам, заселяющим T-зоны периферических органов иммунопоэза.
Кроветворение в селезенке
Закладка селезенки также происходит в конце 1-го месяца эмбриогенеза. Из вселяющихся сюда стволовых клеток происходит экстраваскулярное образование всех видов форменных элементов крови, т.е. селезенка в эмбриональном периоде представляет собой универсальный кроветворный орган. Образование эритроцитов и гранулоцитов в селезенке достигает максимума на 5-м месяце эмбриогенеза. После этого в ней начинает преобладать лимфоцитопоэз.
Кроветворение в лимфатических узлах
Первые закладки лимфоузлов человека появляются на 7—8-й неделе эмбрионального развития. Большинство лимфатических узлов развивается на 9—10-й неделе. В этот же период начинается проникновение в лимфатические узлы стволовых клеток крови, из которых на ранних стадиях дифференцируются эритроциты, гранулоциты и мегакариоциты. Однако формирование этих элементов быстро подавляется образованием лимфоцитов, составляющих основную часть лимфатических узлов.
Появление единичных лимфоцитов происходит уже в течение 8—15-й недели развития, однако массовое «заселение» лимфатических узлов предшественниками T- и B-лимфоцитов начинается с 16-й недели, когда формируются посткапиллярные венулы, через стенку которых осуществляется процесс миграции клеток. Из клеток-предшественников дифференцируются сначала лимфобласты (или большие лимфоциты), а далее средние и малые лимфоциты. Дифференцировка T- и B-лимфоцитов происходит, соответственно, в T- и B-зависимых зонах лимфатических узлов.
Источник
Общеизвестно, что основными клетками крови являются эритроциты, лейкоциты и тромбоциты. Приглядимся к ним поближе.
Эритроциты — строение и функции
Эритроциты — это основная часть состава клеток крови. Количество их у здоровых людей колеблется от 4,5 до 5,5 миллиона в 1 куб.мм. Если расположить их все в одну линию, то она протянется на 187000 км, более чем в 4,5 раза больше земного экватора. Ежесекундный распад 10 миллионов эритроцитов возмещается поступлением в кровь такого же их количества из кроветворных органов.
Эритроциты человека — безъядерные тельца, похожие на двояковогнутые диски, с диаметром, равным в среднем 7 микронам (0,007 мм).
По современным представлениям эритроцит имеет губчатую структуру, пропитанную гемоглобином — носителем кислорода. В составе эритроцитов его более 90%.
Из гемоглобина и кислорода (Нв) образуется непрочный оксигемоглобин. Именно из-за него кровь такого цвета. Основная часть его состава белковая — глобин и небелковая — гем. Успехи современной биохимии позволили изучить этапы его образования, очень сложного и многоступенчатого. Гем способствует гемоглобину “рыхло” соединяться с кислородом, этим он обязан железу, которое присутствует в нем.
Связи кислорода и гемоглобина целиком зависит от содержания (концентрации, или «напряжения») этого газа в окружающей среде. Если раствор гемоглобина окружен воздухом, содержащим 20% кислорода, то гемоглобин почти полностью насытится кислородом, т. е. превратится в оксигемоглобин.
Но если его поместить в безвоздушное пространство или атмосферу азота, то кислород полностью отщепится и гемоглобин окажется восстановленным.
Как эритроциты переносят гемоглобин в организме
Проходя через капилляры легких, где имеется наибольшее напряжение кислорода, гемоглобин крови целиком насыщается кислородом. Этот процесс совершается по законам диффузии газов.
Затем оксигемоглобин переносится в капилляры других тканей организма, где напряжение кислорода очень низкое благодаря чему он легко отделяется от гемоглобина. Освободившийся кислород используется клетками для поддержания их энергетического обмена.
Отечественный ученый П. А. Коржуев на примерах особей животного мира различного уровня развития показал, что расстановка разных видов животных в эволюционном ряду зависит от обеспеченности их гемоглобином (следовательно, и кислородом).
- Так, например, у рыб на килограмм веса тела гемоглобина сравнительно немного;
- У земноводных (следующая ступень развития) немного больше;
- Еще больше его у птиц и т. д.
- Самое большое его количество содержит кровь млекопитающих.
Что происходит с погибшими эритроцитами
Основная задача эритроцитов — переноска кислорода. Они обладают минимальным обменом веществ. В среднем они живут 100—120 дней. Старея, эритроциты подвергаются распаду: в конце своей жизни в селезенке, и печени приклеиваются к особым клеткам на стенках сосудов.
Такие клетки обладают способностью захватывать различные высокомолекулярные и чужие частицы, попадающие в кровь. Этот процесс поглощения (фагоцитоз) распространяется также и на состарившиеся эритроциты, которые для организма стали уже чужеродными.
Непосредственное отношение к процессу кроворазрушения имеет селезенка. Этот орган — «губчатый мешок» из очень рыхлой ткани, переполненной кровью, способен разрушать красные кровяные тельца, что дало повод уже давно называть ее «кладбищем» этих клеток. (По некоторым данным, свыше 70% всех эритроцитов, закончивших свой жизненный цикл, оказываются именно в ней).
Следует отметить, что у здорового человека селезенка разрушает лишь старые или случайно поврежденные красные тельца. Каков же механизм освобождения крови от тех из них, что уже отжили или повреждены? Это удалось открыть с помощью интересных опытов на животных с использованием современной электронной микроскопии.
Крысам вводили токсические для эритроцитов вещества и наблюдали прохождение их через стенку сосудов селезенки. Нормальные клетки легко фильтруются через сосудистые поры: при прохождении через них «гибкие» эритроциты меняют свою форму и проскальзывают в общем токе крови.
Но, старея или повреждаясь, становясь менее эластичными они больше неспособны проникать через капилляры, фильтруются в селезенке и поглощаются (фагоцитоз) ретикуло-эндотелиальными клетками. При распаде в печени эритроцитов образуется пигмент билирубин, который в кишечнике, под влиянием микробов подвергается дальнейшему химическому превращению.
При этом образуется пигмент стеркобилин, который окрашивает кал таким коричневым цветом. Количество этого пигмента в кале говорит об объемах распадающихся эритроцитов.
Нормы эритроцитов по полу и возрасту
| Пол, возраст | Норма, клеток/л |
| У взрослых мужчин | 3.9•10 12 –5,5•10 12 |
| У взрослых женщин | 3,9•10 12 –4,7•10 12 |
| В пуповинной крови плода | 3,9•10 12 –5,5•10 12 |
| 1-3 дня от рождения | 4,0•10 12 –6,6•10 12 ретикулоциты — 3–51% |
| 7 дней | 3,9•10 12 –6,3•10 12 |
| 14 дней | 3,6•10 12 –6,2•10 12 |
| 30 дней | 3,0•10 12 –5,4•10 12 |
| 60 дней | 2,7•10 12 –4,9•10 12 |
| 6 месяцев | 3,1•10 12 –4,5•10 12 ретикулоциты — 3–15% |
| до 12 лет | 3,5•10 12 –5,0•10 12 ретикулоциты — 3–12% |
| Девочки-подростки 13–19 лет | 3,5•10 12 –5,0•10 12 ретикулоциты 2-11% |
| Мальчики-подростки 13–16 лет | 4,1•10 12 –5,5•10 12 ретикулоциты 2-11% |
| 16 — 19 лет | 3,9•10 12 –5,6•10 12 |
| Пожилые люди | 4,0•10 12 |
| Беременные | 3,5•10 12 –5,6∙10 12 ретикулоциты — примерно 1% |
Что происходит с железом, накопившемся в эритроцитах
Сейчас сложилось твердое убеждение, что железо, освободившееся при гибели эритроцитов, полностью используется для построения его новых молекул, предварительно отложившись в печени и селезенке в резерве. Из резерва оно в костном мозге принимает участие в гемоглобинообразовании.
Помимо использования резервного железа, открыт механизм непосредственной утилизации гемоглобинового железа кроветворными клетками.
Здоровый человек ежесуточно при распаде эритроцитов теряет 20—30 мг железа, что равно суточной потребности. 90% этого железа вновь идет на построение нового гемоглобина в процессе созревания новых эритроцитов. Потери железа организмом ничтожны.
Лейкоциты — строение и функции
Лейкоциты — вторая основная составляющая крови, имеют ядро, протоплазму, или цитоплазму (от «цито» — клетка). Отдельные из них способны активно двигаться, наподобие простейших организмов, например, амеб.
В крови человека содержится в 1000 раз меньше лейкоцитов, чем эритроцитов.
Виды лейкоцитов
Лейкоциты бывают зернистыми и незернистыми. Зернистые лейкоциты или гранулоциты имеют протоплазму нагруженную зернами. Незернистые лейкоциты или агранулоциты зерен не содержат или содержат очень мало.
Незернистые и зернистые лейкоциты отличаются друг от друга несколькими признаками:
- способностью восприятия клетками кислых и щелочных красок;
- отсутствием или наличием зерен в цитоплазме;
- отличием в строении ядра;
- формой.
Так, например, цитоплазма эозинофила в окрашенном мазке содержит крупную зернистость, напоминающую кетовую икру, а базофильные лейкоциты имеют зерна, окрашивающиеся в фиолетово-синий цвет.
Ядра различных клеток имеют своеобразную форму, позволяющую отличать одни от других. Ядро зрелого нейтрофила, например, состоит из сегментов, соединенных между собой мостиками, а у лимфоцита ядро круглое и занимает большую часть клетки.
Защитная функция лейкоцитов
Некоторые формы лейкоцитов (прежде всего нейтрофилы и моноциты) поразительно способны к фагоцитозу, т. е. к поглощению и перевариванию различных микробов; простейших организмов, отживших клеток и всяких чужеродных веществ, попадающих в организм.
Присущая лейкоцитам защитная функция проявляется лишь после выхода из кровеносных сосудов. При кровотоке лейкоциты обволакивают внутренние стены капилляров и во множестве уходят из сосудов, протискиваясь между эндотелиальными клетками. При своем следовании они обнаруживают и переваривают в себе микробы и различные инородные тела.
Процесс движения лейкоцитов из сосудов в ткани совершается при посредстве вытягивания протоплазмы и образования ее выростов — так называемых ложноножек (псевдоподий). Лейкоциты активно проходят через неповрежденные стенки сосудов, легко проникают через оболочки (мембраны), двигаются в соединительной ткани.
Роль эозинофилов и базофилов остается еще недостаточно изученной. Больше сведений мы имеем в отношении лимфоцитов. Они образуются в лимфатических узлах, разбросанных по всему организму и в селезенке. (Количество лимфоидной ткани составляет около 1% веса тела!) Изучение продолжительности жизни лимфоцитов с использованием радиоактивной метки доказало, что они циркулируют в крови 100—200 дней, и лишь небольшая их часть исчезает из кровяного русла через 3—4 дня.
Есть основания считать, что лимфоциты участвуют в формировании иммунной системы организма и, таким образом, очень важны в процессах борьбы с микробами и действием их токсинов.
Нормы лейкоцитов по полу и возрасту
| Пол, возраст | Норма, единиц на литр (Ед/л) |
| Малыши до 3-х дней | 7 – 32 × 109 |
| До 1 года | 6 – 17,5 × 109 |
| 1-2 года | 6 – 17 × 109 |
| 2-6 лет | 5 – 15,5 × 109 |
| 6-16 лет | 4,5 – 13,5 × 109 |
| 16-21 год | 4,5 – 11 × 109 |
| Взрослые мужчины | 4,2 – 9 × 109 |
| Взрослые женщины | 3,98 – 10,4 × 109 |
| Пожилые мужчины | 3,9 – 8,5 × 109 |
| Пожилые женщины | 3,7 – 9 × 109 |
Тромбоциты — строение и функции
В крови есть еще третий форменный элемент—тромбоциты (кровяные пластинки).
Тромбоциты, как бы осколки протоплазмы производящих их гигантских клеток костного мозга — мегакариоцитов. Оказывается, что из одного мегакариоцита может образоваться до 400 пластинок. В 1 мм3 крови их насчитывается 250—400 тыс.
Размер кровяных пластинок очень мал — от 2 до 5 микрон. Они формой круглые или овальные, не имеют ядра. Сроки пребывания их в крови от 3 до 5 дней.
Клетки эти играют огромную роль в процессах свертывания крови и занимают ключевую позицию в процессе остановки кровотечения.
Основное, значимое свойство тромбоцитов — прилипать и покрывать чужеродную поверхность. Они при этом становятся больше размером и растягиваются принимая звездчатую форму. При повреждении мелких кровеносных сосудов тромбоциты устремляются к месту повреждения, прилипают кучкой и образуют собой тромб закрывающий место дефекта сосуда.
Вокруг него оседают нити фибрина и эритроциты, цвет тромба меняется на красный. Благодаря выпадению фибрина головка тромба плотно фиксируется к поврежденному сосуду и задерживает переход крови из сосуда наружу.
Таким образом, тромбоциты успешно организуют первичный, «пусковой» этап остановки кровотечения при повреждении сосуда. Поэтому при заболеваниях, которым свойственно отсутствие, малое количество или неполноценность тромбоцитов, наблюдаются самопроизвольные кровотечения и кровоизлияния.
Нормы тромбоцитов по полу и возрасту
| Пол, возраст | Норма тромбоцитов, тысяч Ед/мкл |
| У мужчин | 200-400 |
| У женщин | 180-320 |
| У женщин в критические дни | 75-220 |
| У беременных | 100-310 |
| У новорожденных | 100-420 |
| 2 недели -1 год | 150-350 |
| 1 – 5 лет | 180-380 |
| 5 – 7 лет | 180-450 |
Поделиться ссылкой:
Источник