Хромосомные аберрации в лимфоцитах
Код 20.120.
Венозная кровь
Биоматериал для этого исследования принимается по сокращённому графику. Это связано с тем, что пробы должны попасть в лабораторию в очень короткий срок. Проверьте сокращённый график в вашем отделении.
- Приём, исследование биоматериала
- Показания к назначению
- Описание
Приём и исследование биоматериала
Приём материала
- Можно сдать в отделении Гемотест — 154 отделения
- Можно сдать анализ дома
Когда нужно сдавать анализ Экспертный анализ кариотипа лимфоцитов периферической крови с выявлением хромосомных аберраций (с фотографией)?
1. Наличие в анамнезе 2 и более самопроизвольных выкидышей.
2. Бесплодие.
3. Олигозооспермия.
4. Необструктивная форма азооспермии.
5. Первичная (или вторичная) аменорея.
6. Замершая беременность.
7. Случаи детской смертности на первом году жизни или рождения в семье мертвого ребенка.
8. Рождение ребенка с врожденными сочетанными пороками.
9. Задержка развития малыша (как физического, так и умственного.
10. Генетические заболевания у родителей и близких родственников.
11. Подозрение на генетическую патологию по имеющимся внешним признакам (например: специфическая форма черепа, пальцев рук, аномалии наружных половых органов, глаз, носа и т.д.).
12. Обследование доноров генетического материала.
Подробное описание исследования
Кариотипирование (цитогенетическое обследование) – это анализ на выявление нарушений хромосомного набора человека. При кариотипировании выявляется количество и строение хромосом, что позволяет выявить хромосомные аномалии, которые могут стать причиной бесплодия, невынашивания беременности, другой наследственной болезни и рождения больного ребенка.
Каждый организм характеризуется определенным набором хромосом, который называется кариотипом. Кариотип человека состоит из 46 хромосом – 22 пары аутосом и две половые хромосомы. У женщины – это две X хромосомы (кариотип: 46, ХХ), а у мужчин одна Х хромосома, а другая – Y (кариотип: 46, ХY). В каждой хромосоме находятся гены, ответственные за наследственность. Исследование кариотипа проводится с помощью цитогенетических и молекулярно-цитогенетических методов.
Вне процесса деления клетки хромосомы в её ядре расположены в виде «распакованной» молекулы ДНК, и они трудно доступны для осмотра в световом микроскопе. Для того, чтобы хромосомы и их структура стали хорошо видны используют специальные красители, позволяющие выявлять гетерогенные (неоднородные) участки хромосом и проводить их анализ – определять кариотип. Хромосомы в световом микроскопе на стадии метафазы представляют собой молекулы ДНК, упакованные в плотные палочковидные структуры. Таким образом, большое число хромосом упаковывается в маленький объём и помещается в относительно небольшом объёме ядра клетки. Расположение хромосом, видимое в микроскопе, фотографируют и из нескольких фотографий собирают систематизированный кариотип – нумерованный набор хромосомных пар гомологичных хромосом. Изображения хромосом при этом ориентируют вертикально, короткими плечами вверх, а их нумерацию производят в порядке убывания размеров. Пару половых хромосом помещают в самом конце изображения набора хромосом.
Современные методы кариотипирования обеспечивают детальное обнаружение хромосомных аберраций (внутрихромосомных и межхромосомных перестроек), нарушения порядка расположения фрагментов хромосом – делеции, дупликации, инверсии, транслокации. Такое исследование кариотипа позволяет диагностировать ряд хромосомных заболеваний, вызванных как грубыми нарушениями кариотипов (нарушение числа хромосом), так и нарушением хромосомной структуры или множественностью клеточных кариотипов в организме. Нарушения нормального кариотипа у человека возникают на ранних стадиях развития организма. Если это происходит в половых клеток будущих родителей, то кариотип зиготы образовавшейся при слиянии родительских клеток, также оказывается нарушенным. При дальнейшем делении такой зиготы все клетки эмбриона и развившегося из него организма окажутся с одинаково аномальным кариотипом. Однако, нарушения кариотипа могут возникнуть и на ранних стадиях дробления зиготы. Развившийся из такой зиготы организм содержит несколько линий клеток (клеточных клонов) с разными кариотипами. Такое многообразие кариотипов во всём организме или только в некоторых его органах называют мозаицизмом.
Как правило, нарушения кариотипа у человека сопровождаются различными, в том числе комплексными, пороками развития, и большинство таких аномалий несовместимо с жизнью. Это приводит к самопроизвольным абортам на ранних стадиях беременности. Однако достаточно большое число плодов (~2,5%) с аномальными кариотипами донашивают до окончания беременности. Хромосомные аномалии у новорожденных являются причиной 45-50% множественных врожденных пороков развития, около 35% случаев умственной отсталости и 50% отсутствия менструации у женщин. У взрослых хромосомные аномалии клинически могут не проявляться и вовсе, или иметь место в стертых формах. Часто человек считает себя абсолютно здоровым и не подозревает о каких-либо генетических нарушениях. Но он не может иметь детей. Поэтому исследование кариотипа лимфоцитов крови рекомендуется обязательно делать всем бесплодным парам.
Другие названия этого исследования
Названия на английском языке
Cariotip,Cariotyping,Chromosome Analysis,Karyotype analysis
Названия на русском языке
Кариотип,Кариотипирование,Определение хромосомного набора,Синдром Дауна, Патау, Клайнфельтера, Шерешевского-Тёрнера,Хромосомные аномалии,Хромосомные риски,Хромосомы
- Подготовка к исследованию
- Противопоказания и ограничения
Подготовка к исследованию
1. Cпециальной подготовки не требуется.
2. Исследование проводится на сытый желудок (1,5-2 часа после еды).
3. Биоматериал должен быть доставлен в лабораторию в день взятия. Хранение не допускается.
Противопоказания и ограничения
Факторы, влияющие на результаты исследований
1. Перед диагностикой не рекомендуется подвергать себя стрессовым ситуациям, принимать спиртные напитки и курить.
2. Рацион и прием лекарственных препаратов не влияет на результат исследования.
Интерпретация результата
У мужчин – 46XY.
У женщин – 46ХХ.
47,XXY; 48,XXXY – синдром Клайнфельтера.
45X0; 45X0/46XX; 45,X/46,XY; 46,X iso (Xq) – синдром Шерешевского-Тернера.
47,ХХX; 48,ХХХХ; 49,ХХХХХ – трисомия и полисомия по X-хромосоме.
47,ХХ,+21; 47,ХY,+21 – синдром Дауна.
47,ХХ,+18; 47,ХY,+18 – синдром Эдвардса.
47,ХХ,+13; 47,ХY,+13 – синдром Патау.
46,XX,5р – синдром “кошачьего крика”.
Источник
[16-001]
Исследование кариотипа (количественные и структурные аномалии хромосом) по лимфоцитам периферической крови (1 человек)
6290 руб.
Цитогенетическое исследование – кариотипирование – является основным методом диагностики хромосомных нарушений и проводится в целях выявления нарушений количества и структуры хромосом. Используется для пренатальной диагностики.
Синонимы русские
- Хромосомные риски
- Кариотипирование супругов
- Определение хромосомного набора
Синонимы английские
- Karyotyping
- Karyotyping Chromosome Analysis
Метод исследования
Световая микроскопия.
Какой биоматериал можно использовать для исследования?
Венозную кровь.
Как правильно подготовиться к исследованию?
- Исследование проводится в состоянии сытости, не рекомендуется сдавать кровь на данное исследование натощак.
- Исключить (по согласованию с врачом) прием антибактериальных и химиотерапевтических препаратов в течение 14 дней до исследования.
- Исследование рекомендуется проводить не ранее чем через 2 недели после перенесенных инфекционных/острых воспалительных заболеваний.
Общая информация об исследовании
Кариотипирование – цитогенетическое исследование, изучение хромосомного набора человека, позволяющее обнаружить отклонения в структуре и числе хромосом. Оно помогает выявить нарушения хромосом, вероятно, не влияющие на здоровье человека, но тем не менее важные для планирования будущей беременности и для здоровья будущего ребенка (патологии плода, аномалии развития).
Кариотип – это полный хромосомный набор клетки человека. В норме он состоит из 46 хромосом, из них 44 аутосомы (22 пары), имеющих одинаковое строение и в мужском, и в женском организме, и одна пара половых хромосом (XY у мужчин и XX у женщин). Каждая хромосома несет гены, ответственные за наследственность. Кариотип 46, ХХ – соответствует нормальному женскому кариотипу, а кариотип 46, XY – это нормальный мужской кариотип. Кариотип остается неизменным в течение всей жизни.
Нарушения хромосомного набора могут являться причиной наследственной патологии, бесплодия, невынашивания беременности, рождения ребенка с различными пороками развития.
Для цитогенетического исследования хромосом чаще всего используют препараты кратковременной культуры крови, реже клетки костного мозга и культуры фибробластов.
Кариотипирование культуры лимфоцитов периферической крови человека – сложное многоступенчатое цитогенетическое исследование, проводится, когда клетки входят в фазу митоза – непрямого деления с тождественным распределением генетического материала между дочерними клетками. Оно включает в себя следующие этапы:
- Постановка культуры лимфоцитов, рост клеток в течение 72 часов. (Рост клеток может быть осложнен различными факторами: наличие инфекционных, хронических, простудных заболеваний; прием лекарственных препаратов; диета; прием алкоголя и т. п. Все эти факторы необходимо исключить перед сдачей анализов).
- Обработка культур лимфоцитов: колхицинизация, гипотонизация, фиксация.
- Приготовление препаратов хромосом на стекле.
- Монохромное и дифференциальное окрашивание препарата.
- Анализ препаратов (подсчитывается общее количество хромосом, проводится оценка структуры каждой хромосомы). Анализ хромосом осуществляется на разрешении в 400-500 полос (бэндов).
Различают несколько видов нарушений структуры хромосом:
- трисомии – добавление еще одной хромосомы к паре;
- моносомии – утрата одной хромосомы из пары;
- делеции – утрата участка хромосомы;
- дупликации – повторение определенного участка хромосомы;
- инверсии – поворот участка хромосомы на 180 градусов;
- транслокации – перенос участков хромосомы в новое положение.
Хромосомные нарушенияразличаются также по принципу регулярности. Регулярные мутации присутствуют при делении каждой клетки или большинства клеток. Они проявляются в момент зачатия плода либо в первые несколько дней беременности. Нерегулярные аберрации появляются в результате негативного воздействия радиации, химических средств и т.д.
Нарушение расхождения хромосом может произойти во время клеточного деления (мейоза). Если такое нарушение происходит в процессе образования сперматозоидов или яйцеклеток, то в половой клетке появляется лишняя хромосома, которая при зачатии будет передана ребенку. В результате она будет присутствовать во всех клетках организма ребенка. Примером трисомии может служить синдром Дауна (лишняя 21-я хромосома) или синдром Патау (трисомия 13-й хромосомы). Также нарушение расхождения хромосом может произойти при первых делениях оплодотворенной яйцеклетки. Например, утрата Х-хромосомы приводит к развитию Х0-синдрома, или синдрома Шерешевского – Тернера. Аномалии, связанные с нарушением расхождения хромосом, встречаются не так часто, поэтому вероятность их повторения в одной и той же семье достаточно мала.
Структурные же нарушения хромосом передаются по наследству, при этом степень семейного риска и дальнейшая передача дефекта от поколения к поколению становится значительно высокой.
Кариотипирование также рекомендуют проводить в тех семьях, где есть высокая вероятность рождения ребенка с болезнью, сцепленной с Х-хромосомой.
Когда назначается исследование?
Показания для кариотипирования супружеских пар:
- мужское бесплодие: тяжелая олигозооспермия, необструктивная азооспермия, тератозооспермия;
- первичная аменорея;
- привычное невынашивание беременности в первом триместре (2 и более выкидышей);
- наличие выкидышей неясного генеза в анамнезе;
- случаи мертворождений в анамнезе;
- случаи ранней младенческой смертности в анамнезе;
- рождение детей с хромосомной аномалией (например, синдромом Дауна);
- рождение детей с множественными врождёнными пороками развития (МВПР);
- планирование ЭКО;
- неудачные попытки ЭКО;
- прогноз здоровья будущего ребенка.
Показания для кариотипирования детей:
- наличие врождённых пороков развития;
- умственная отсталость;
- задержка психомоторного развития;
- задержка психо-речевого развития в сочетании с микроаномалиями;
- нарушение или задержка полового развития;
- задержка роста;
- аномалии пола.
Что означают результаты?
Для мужчин нормальным считается кариотип 46,XY. Это означает, что определено 46 нормальных хромосом, в том числе X и Y хромосома.
Для женщин нормальным считается кариотип 46,XX. Это означает, что определено 46 нормальных хромосом, в том числе две X хромосомы.
В случае выявления патологического кариотипа, необходима консультация медицинского генетика по результатам исследования для правильной его интерпретации.
Литература
- Reddy UM, Page GP, Saade GR, et al. Karyotype versus microarray testing for genetic abnormalities after stillbirth. N Engl J Med 2012;367:2185-93.
- Murphy KM, Cohen JS, Goodrich A, Long PP, Griffin. CA 2007. Constitutional duplication of a region of chromosome Yp encoding AMELY, PRKY, and TBL1Y: implications for chromosome analysis. J Mol Diagn, 9: 408-413.
- ISCN (2013): An International System for Human Cytogenetic Nomenclature; Karger AG, Basel, 2013/
- ISCN (2016): An International System for Human Cytogenetic Nomenclature; S. Karger AG, Basel, 2016/
- ISCN Symbols and Abbreviated Terms//Coriell Institute for Medical Research/
Источник
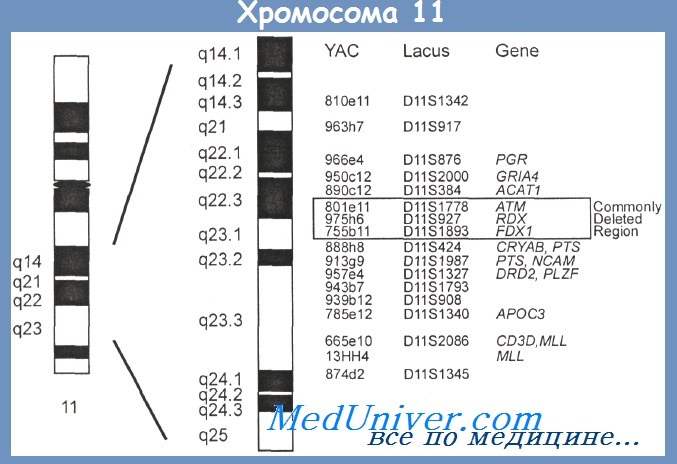
Хромосомные аномалии при хроническом лимфолейкозе – прогнозПо классификации ВОЗ, хронический лимфолейкоз (ХЛЛ) относится к опухолям из зрелых В-клеток. Клиническое течение и длительность болезни сильно варьируют: на одном полюсе находятся формы болезни с длительным, относительно спокойным течением, не требующим лечения в течение многих лет, на другом — агрессивные варианты лейкоза, нуждающиеся в интенсивном лечении сразу после постановки диагноза. Нередко встречаются «промежуточные» формы. Прогнозирование течения хронического лимфолейкоза в момент его выявления может вызывать определенные затруднения. Существует две основные клинические системы определения стадии болезни и прогнозирования ее течения, однако ни одна из этих систем не позволяет определить прогноз в каждом конкретном случае. Постоянно ведется поиск новых, более надежных прогностических показателей, которые оказались бы полезными в решении практических вопросов. В частности, важно решить, нужна ли интенсивная терапия больным с малой массой опухоли, но с лабораторными признаками плохого прогноза? Какой конкретный протокол лечения предпочтителен конкретному больному при прогрессии болезни? Известно, что хронический лимфолейкоз неоднороден не только в клиническом отношении; имеются существенные биологические и молекулярно-генетические отличия между популяциями лейкозных клеток у разных больных. В результате клинико-лабораторных сопоставлений удалось провести определенные параллели между длительностью течения болезни (прогнозом) и отдельными особенностями лейкозных клеток. Полученные данные уже используются в клинической практике, в частности с прогностическими целями. Как и при других гемобластозах, при хроническом лимфолейкозе важное клиническое значение приобрели особенности кариотипа лейкозных клеток. Еще несколько лет назад считали, что неоплазированные клетки при этом заболевании имеют нормальный кариотип. Позже удалось выяснить, что без специальных методических приемов хромосомному анализу подвергались не лейкозные, а нормальные лимфоциты больных. Изучение особенностей кариотипа хронического лимфолейкоза стало возможным только после введения веществ, стимулирующих митотическую активность В-клеток. Обычно в каждом случае применяется несколько стимуляторов, т. е. производится посадка нескольких культур из клеток крови или других пораженных органов с использованием различных стимуляторов. В отдельных культурах удается выявить клоны аномальных клеток. Иногда в разных клеточных культурах, полученных от одного больного и подвергнутых действию разных стимуляторов, обнаруживают клоны клеток с разными нарушениями кариотипа. Наиболее характерны следующие нарушения: дополнительная хромосома 12, делеции длинного плеча хромосом 6 и 13, различные перестройки длинного плеча хромосомы 11. В ряде случаев наблюдаются характерные для В-клеточных новообразований транслокации с участием района 14q32 (область локализации IgH), среди которых преобладают t(11;14)(q13;q32), t(2;14)(p13;q32) и t(14;19)(q32;p13). На протяжении нескольких лет для изучения хромосомных изменений при хроническом лимфолейкозе с успехом применяется FISH, нередко — интерфазный анализ, который позволяет выявлять нарушения кариотипа клеток вне митоза, на стадии интерфазы. При характерном для хронического лимфолейкоза низком митотическом индексе лейкозных клеток использование интерфазной FISH резко расширяет возможности анализа. С помощью этого подхода нарушения кариотипа обнаруживают у 80 % больных, тогда как обычное цитогенетическое исследование выявляет их только у 40—50 % больных. Некоторые авторы приводят другие цифры. Так, в работе D. G. Oscier и соавт. обычный хромосомный анализ позволил обнаружить клоны аномальных клеток у 141(69 %) из 206 больных хроническим лимфолейкозом при изучении краткосрочных клеточных культур, стимулированных ТПА. Использование FISH практически мало изменило эти результаты, но было одно исключение — нарушения хромосомы 13. При стандартном цитогенетическом исследовании эти нарушения удалось выявить у 17 %, а с помощью FISH — у 45% больных. Частота этой аномалии (13q-), по данным других авторов, еще выше. Так, G. W. Dewald и соавт., обследовав 113 больных хроническим лимфолейкозом, обнаружили делецию одной хромосомы из 13-й пары у 64 % больных, а делецию обоих гомологов — у 28 % обследованных.
Американские авторы представили частоту отдельных хромосомных перестроек по результатам интерфазной FISH. Так, делеция 13ql4, по их данным, составила 64%, делеция 11q—15%, трисомия 12 – 25 %, делеция 17р — 8 %. Частоты, приводимые в других публикациях, сходны, но не точно такие же. Это может быть обусловлено возрастными и географическими различиями в частоте неслучайных хромосомных аномалий, стадией болезни, на которой производили исследование, а также особенностями В-клеточных стимуляторов и других методических приемов, применявшихся конкретными авторами. Интересно, что с помощью FISH клоны клеток с делециями хромосомы 13 были выявлены у 50 % обследованных без гематологической патологии, но с так называемым синдромом CLUS (MBCL). CLUS (моноклональный ХЛЛ-фенотип в небольшом количестве клеток крови) наблюдается среди людей старше 40 лет с частотой примерно 3,5 %. Обычно это люди из семей, где есть больные хроническим лимфолейкозом. Таким образом, невозможно без применения FISH сделать заключение о наличии или отсутствии прогностически значимых изменений кариотипа при хроническом лимфолейкозе. Характерные изменения кариотипа отличаются друг от друга в прогностическом отношении. Так, делеции 17р и 11q, наличие дополнительной хромосомы 12 прогностически неблагоприятны, а присутствие делетированной хромосомы 13 как единственной аномалии считают прогностически благоприятным. По данным D. G. Oscier и соавт., продолжительность жизни (медиана) при хроническом лимфолейкозе с моносомией или делецией длинного плеча хромосомы 13 составила 292 мес, при обнаружении трисо-мии 12 — 122 мес, делеций 11q23 — 117 мес, изменений короткого плеча хромосомы 17 или мутаций гена р53 — всего 47 мес. В литературе приводятся сведения о клинико-морфологических особенностях хронического лимфолейкоза, ассоциированного с определенными аномалиями кариотипа. В частности, существует точка зрения, что хронический лимфолейкоз с трисомией 12 представляет собою отдельный вариант болезни, при котором часто наблюдаются атипичная морфология лимфоцитов и атипичный иммунофенотип, отсутствие мутации в вариабельном районе гена Н-цепей иммуноглобулина и неблагоприятное течение. Крайне неблагоприятны в прогностическом отношении делеции длинного плеча хромосомы 11 района 11q22.3-q23.1. Это сравнительно частая аномалия — до 20 % хронического лимфолейкоза. По вопросу о том, является ли трисомия 12 неблагопрятным прогностическим признаком, существуют разногласия, но все исследователи единодушны, считая делении 11q прогностически неблагоприятными. Больные с этими нарушениями сравнительно молоды, у них отмечается выраженный опухолевый рост периферических, абдоминальных и медиастинальных лимфатических узлов. Медиана выживаемости составляет 64 мес против 209 мес в группе хронического лимфолейкоза без делеций 11q. Интересные данные сообщили немецкие авторы на международном рабочем совещании по хроническому лимфолейкозу. Они изучали особенности кариотипа клеток крови больных хроническим лимфолейкозом (84 пациента) с помощью FISH. Предварительно проводили совместное культивирование клеток от больных с клетками стабильных линий, экспрессирующих специальные стимуляторы. После культивирования в большинстве проб (87 %) были обнаружены аномальные клоны с нарушениями кариотипа, характерными для хронического лимфолейкоза. У большинства больных еще до лечения хромосомные нарушения были множественными, т. е. клетки лейкозного клона содержали по 3—4 и более изменений. Частота клонов со сложными перестройками не зависела от стадии болезни. Анализ материала позволил авторам сделать вывод, что клоны клеток, содержащих более 3 аномалий, характерны для быстро прогрессирующего хронического лимфолейкоза. Большинство больных со сложными перестройками были сравнительно молоды. Авторы высказали предположение, что для прогноза хронического лимфолейкоза важно не количество, а качество хромосомных аномалий. Например, перестройки короткого плеча хромосомы 17 однозначно ассоциированы с плохим прогнозом. Другие авторы сравнили особенности кариотипа в двух группах хронического лимфолейкоза: со стабильным течением (без прогрессии по меньшей мере в течение полугода) и с более агрессивным течением. У больных обеих групп обнаружены как прогностически благоприятные, так и прогностически неблагоприятные аномалии кариотипа, но отмечена следующая тенденция: при более агрессивной форме доля клеток с аномалиями была выше и чаще наблюдались случаи со сложными перестройками. В последние годы при прогнозировании хронического лимфолейкоза большое значение придается гиперэкспрессии маркера CD38 на поверхности лимфоцитов крови. Получены убедительные данные, что у больных с гиперэкспрессией CD38 гораздо худший прогноз, чем у больных без этого признака. Однако существует и противоположное мнение. Есть также противоречия по вопросу о том, какой процент клеток с гиперэкспрессией CD38 является прогностически неблагоприятным показателем. Большинство исследователей называют 30 %, а некоторые 7 %. Тем не менее подавляющее большинство специалистов считают, что гиперэкспрессия CD38 — четкий маркер плохого прогноза, обычно сочетающийся с другими плохими прогностическими признаками, в частности, цитоге-нетическими. Кроме того, гиперэкспрессия CD38 нередко коррелирует с так называемым VH-статусом. Нередко повышенная экспрессия CD38 наблюдается на лимфоцитах, которые не претерпели мутации вариабельного участка гена Н-цепей иммуноглобулинов (отрицательный, или «немутированный», VH-статус). По VH-статусу вся группа хронического лимфолейкоза делится примерно пополам. Различия в продолжительности жизни больных с «немутированным» и «мутированным» VH-статусом очень значительны: медианы составляют 6—8 лет и 24—25 лет. Показано, что «немутированный» VH-статус нередко ассоциирован с такими прогностически неблагоприятными генетическими маркерами, как делеции 11q и 17р, трисомия хромосомы 12 и нарушения р53. Эти нарушения позволяют прогнозировать невысокую эффективность терапии. Сочетание «немутированного» VH-статуса с неблагоприятными изменениями кариотипа (делеции 11q и 17р) ухудшает прогноз: общая выживаемость составляет соответственно 98 и 58 мес. Обнаружен новый важный прогностический маркер при хроническом лимфолейкозе — белок ZAP70 (zeta-chain associated protein 70). Его выявляют у больных с «немутированным» Vн-статусом. Этот белок — тоже четкий маркер «плохого» прогноза. Вероятно, определение ZAP70 войдет в широкую клиническую практику, поскольку методика его выявления более проста, чем идентификация VH-статуса. Обследование больших групп больных хроническим лимфолейкозом с одновременным изучением разных прогностических маркеров (хромосомный анализ, FISH, VH-статус, CD38, мутации гена ТР53) позволило увидеть, что данные этих тестов нередко совпадают. Высказано предположение, что за этим совпадением стоят общий биологический смысл, общее происхождение группы хронического лимфолейкоза, при котором наблюдается сочетание отрицательного VH-статуса с одной (или двумя) из таких прогностически неблагоприятных аномалий кариотипа, как 17р- и 11q-. Даже на ранних клинико-гематологических стадиях болезни сочетание этих признаков предсказывает сравнительно невысокую эффективность терапии. Обобщая данные об особенностях хронического лимфолейкоза в зависимости от отсутствия или наличия мутаций VH, Т. Hamblin приводит следующие данные: в группе с «мутированным» VH-статусом 90 % больных имеют стабильную форму болезни, а в группе с отсутствием мутации доля таких больных всего 15 %. При цитогенетическом исследовании в первой из этих групп у большинства больных обнаружен нормальный кариотип или 13q-; мутации гена ТР53 и аномалии 11q23 практически всегда совпадают с «немутированным» статусом, как и трисомия хромосомы 12; продолжительность жизни при диагнозе на стадии В или С по Binet в 2 раза выше в группе с мутациями. Т. Hamblin высказывает предположение, что это две болезни, а не две формы одного заболевания. – Читать далее “Хромосомные аномалии при злокачественных лимфомах – прогноз” Оглавление темы “Гематология”:
|
Источник