Гипоэхогенные лимфоузлы на шее что это
Шейные лимфатические узлы являются частым местом метастазирования злокачественных опухолей, первичный очаг которых располагается в области головы и шеи. К ним, например, относятся плоскоклеточный рак верхних отделов дыхательных путей, а также метастазы рака слюнных желез и щитовидной железы.
Наиболее распространенным клиническим признаком является увеличивающееся образование шеи, которое обычно обнаруживается пациентом или его врачом. При подозрении на метастатическое поражения лимфатических узлов шеи для диагностики и определения наилучшей тактики лечения потребуется осмотр врачом-онкологом, инструментальные методы и биопсия.
Иногда новообразования вне области головы и шеи могут неожиданно метастазировать в шейные лимфатические узлы, что требует особенно тщательной диагностики для выявления первичного очага.
Лечение будет зависеть от типа и локализации первичной опухоли, которая распространилась в лимфатические узлы шеи, и, скорее всего, будет включать в себя комбинацию хирургического вмешательства, лучевой терапии и/или химиотерапии.
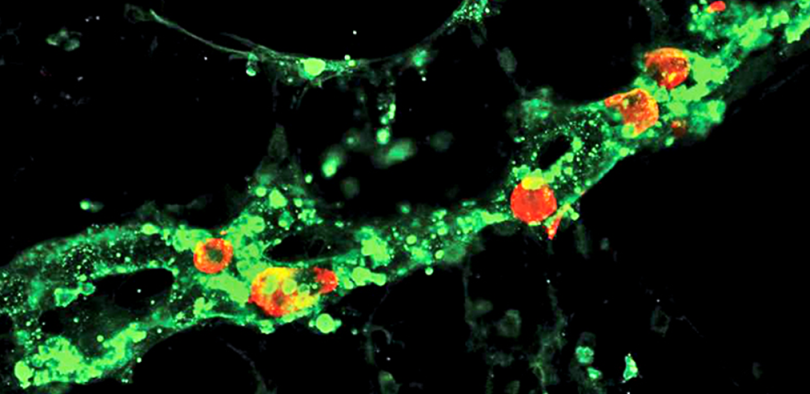
Иммунофлюоресцентная визуализация метастатических клеток меланомы (красные) внутри лимфатических сосудов (зеленые). Масштабная линейка: 100 мкм
(Science Advances/Michael Detmar Group ©)
Из чего состоит лимфатическая система шеи
Лимфатическая система шеи включает в себя сосуды и узлы.
Сосуды:
Лимфатические капилляры — это тонкостенные структуры, состоящие из одного слоя эндотелиальных клеток. Они находятся во всех тканях организма и, объединяясь друг с другом, способствуют оттоку лимфатической жидкости в более крупные лимфатические сосуды.
Стенка лимфатических сосудов состоит из трех слоев: внутреннего слоя эндотелиальных клеток, среднего мышечного слоя и внешнего слоя соединительной ткани. В лимфатических сосудах гораздо больше клапанов, чем в венозных, при этом циркуляция лимфы полностью зависит от сжатия сосудов окружающими мышцами. Лимфатические сосуды дренируют лимфу в лимфатические узлы.
Узлы:
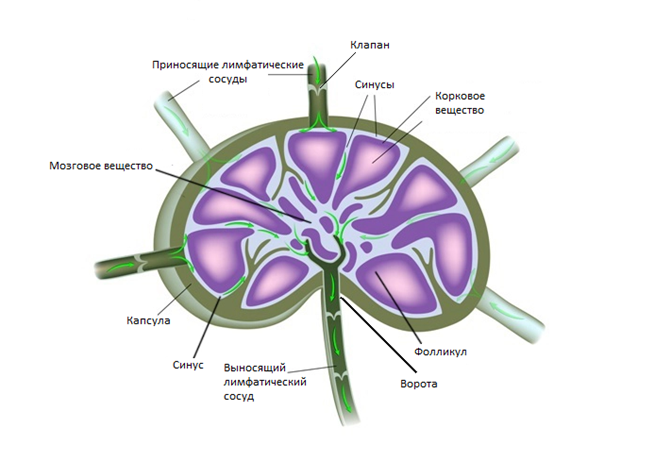
В среднем на каждой стороне шеи расположено до 75 лимфатических узлов. Снаружи узел покрывает капсула, под которой располагается субкапсулярные синусы – место куда попадает лимфатическая жидкость из приносящих лимфатических сосудов. Жидкость проходит сквозь ткань лимфатического узла, которая состоит из коркового и мозгового вещества, а затем выходит через ворота лимфатического узла и попадает в отводящие лимфатические сосуды. В итоге лимфа попадает в венозную систему в месте соустья внутренней яремной и подключичной вены.

Анатомическая структура лимфатического узла (Alila Medical Media/ Shutterstock ©)
Классификация лимфатических узлов шеи
На данный момент во всем мире рекомендована к использованию классификация Американского объединенного комитета по раку (American Joint Committee on Cancer (AJCC)) 8 издания от 2018 года:
- Уровень I (IA и IB): подбородочные и поднижнечелюстные лимфатические узлы;
- Уровень II (IIA и IIB): верхняя яремная группа (делится на 2 подуровня, границей между которыми является добавочный нерв);
- Уровень III: средняя яремная группа;
- Уровень IV: нижняя яремная группа;
- Уровень V (VА и VB): лимфатические узлы заднего треугольника шеи;
- Уровень VI: передние шейные лимфатические узлы;
- Уровень VII: верхние медиастинальные лимфатические узлы.

Уровни лимфатических узлов шеи (Tenese Winslow LLC ©)
Диагностика
Осмотр
При пальпации шеи врач обращает внимание на расположение, размер, плотность и подвижность каждого узла. Особое внимание уделяется узлам, которые кажутся фиксированными к подлежащим сосудисто-нервным структурам и внутренним органам. Описание каждого узла становится важной частью медицинской документации, которая в дальнейшем может использоваться для оценки эффекта лечения.
Лучевые методы
- Ультразвуковое исследование
Преимуществами УЗИ перед другими методами визуализации являются цена, скорость исследования и низкая лучевая нагрузка на пациента.
Ультразвуковыми признаками метастатического поражения лимфатических узлов может быть образование сферической формы, нарушение структуры, нечеткие границы, наличие центрального некроза и др.
Поскольку не всегда по УЗИ можно с уверенностью сказать является лимфатический узел пораженным или нет, иногда одновременно выполняют тонкоигольную аспирационную биопсию под ультразвуковым контролем с последующим цитологическим исследованием материала из этого узла. Результат цитологического исследования зависит от навыков врача УЗИ и качества образца (т.е. наличия достаточного количества репрезентативных клеток).
- Компьютерная томография
С появлением систем высокого разрешения и специальных контрастных веществ КТ позволяет обнаруживать лимфатические узлы, которые могли быть пропущены при иных методах диагностики.
- Магнитно-резонансная томография
Ценность МРТ – превосходная детализация мягких тканей. МРТ превосходит КТ в качестве предпочтительного исследования при оценке ряда новообразований головы и шеи, таких как основание языка и слюнные железы. Размер, наличие нескольких увеличенных узлов и центральный некроз – критерии, общие для протоколов исследования КТ и МРТ.
- Позитронно-эмиссионная томография
Этот новый метод визуализации все чаще используется для определения стадии опухолей головы и шеи. Метод основан на поглощении 2-фтор-2-дезокси-D-глюкозы (ФДГ) метаболически активными тканями. Исследование также может быть объединено с КТ, чтобы улучшить разрешение получаемого изображения и более точно определить расположение образования.
Биопсия
Биопсия — это удаление небольшого кусочка ткани для исследования под микроскопом или для тестирования в лаборатории на предмет наличия признаков злокачественности. В подавляющем большинстве случаев проводится тонкоигольная аспирационная биопсия. Врач, выполняющий биопсию, может использовать УЗИ или КТ для выполнения процедуры. Иногда тонкоигольная аспирационная биопсия не позволяет поставить окончательный диагноз, и требуются другие виды биопсии, такие как трепан-биопсия или эксцизионная биопсия.
План лечения
После определения диагноза и проведения всех диагностических исследований врач порекомендует оптимальный для пациента курс лечения. В конечном итоге лечение метастатического поражения лимфатических узлов зависит от типа и локализации первичной опухоли.
Существует три различных варианта лечения, которые могут быть использованы отдельно или в комбинации:
- хирургическое вмешательство,
- лучевая терапия,
- химиотерапия.
Хирургическое лечение
Хирургическое лечение обычно включает удаление лимфатических узлов шеи (лимфодиссекция) и последующее гистологическое исследование для точного определения стадии, так как это может существенно повлиять на дальнейшую тактику лечения. Хоть и не всегда, но чаще всего лимфодиссекция выполняется одновременно с удалением первичной опухоли.
Существуют различные виды лимфодиссекций:
- радикальная лимфодиссекция: удаление всех лимфоузлов, удаление внутренней яремной вены, удаление мышц и нервов;
- модифицированная радикальная лимфодиссекция: удаление всех лимфоузлов с сохранением мышц. Нервы и/или внутренняя яремная вена могут быть удалены;
- селективная лимфодиссекция: удаление только определенных групп лимфоузлов.
Лучевая терапия
Лучевая терапия может быть назначена в качестве самостоятельного метода лечения в послеоперационном периоде, чтобы снизить вероятность рецидива либо в комбинации с химиотерапией в качестве самостоятельного или адъювантного лечения. Обычно адъювантная лучевая терапия необходима, если по результатам гистологического исследования обнаруживается несколько пораженных лимфатических узлов.
Химиотерапия
Химиотерапия обычно добавляется к лучевой терапии в качестве самостоятельного или адъювантного (послеоперационного) лечения. В некоторых случаях может использоваться индукционная химиотерапия с целью уменьшения объема образования и последующего хирургического вмешательства.
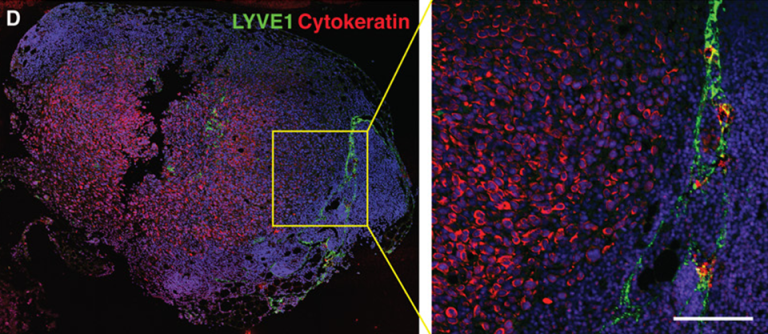
Иммунофлюоресцентная визуализация метастатически пораженного лимфатического узла с окраской на Цитокератин (красный) – маркер характерный для опухолевых клеток эпителиального происхождения. Масштабная линейка: 50 мкм
(Science Advances/Michael Detmar Group ©)
Прогноз
Метастазы в лимфатические узлы шеи могут возникать при онкологических заболеваниях различных локализаций, поэтому давать прогностические оценки для этой группы пациентов следует только после выявления первичной опухоли.
Факторы, влияющие на прогноз:
- стадия заболевания,
- локализация первичной опухоли,
- гистологический подтип и степень дифференцировки,
- количество и размер пораженных лимфатических узлов,
- характеристика края резекции опухоли.
Наблюдение после лечения
Пациенты должны регулярно посещать своего специалиста по опухолям головы и шеи для оценки состояния на предмет любых признаков рецидива заболевания.
Стандартный график наблюдения
В первые 1–2 года осмотр и сбор жалоб рекомендуется проводить каждые 3–6 месяца, на сроке 3–5 лет – один раз в 6–12 месяцев. После 5 лет с момента операции посещать врача необходимо один раз в год или при появлении жалоб. У пациентов с высоким риском рецидива перерыв между обследованиями может быть сокращен.
Список литературы:
- RUSSCO Практические рекомендации по лечению злокачественных опухолей головы и шеи. 2020г
- NCCN Clinical Practice Guidelines in Oncology Head and Neck Cancers Version 1.2021 — November 9, 2020
- DeVita, Hellman, and Rosenberg’s Cancer: Principles & Practice of Oncology (Cancer Principles and Practice of Oncology) 11th Edition 2019
- AJCC (American Joint Committee on Cancer). Cancer Staging Manual – 8th Edition. New York, NY: Springer; 2018
- Pisani, Paolo et al. “Metastatic disease in head & neck oncology.” Acta otorhinolaryngologica Italica 2020
- Van den Brekel MW. Lymph node metastases: CT and MRI. Eur J Radiol. 2000
- Chen ZW, Zhu LJ, Hou QY, Wang QP, Jiang S, Feng H. Clinical application of positron-emission tomography for the identification of cervical nodal metastases of head and neck cancer compared with CT or MRI and clinical palpation. Chinese journal of stomatology. 2008
- Qiaoli Ma et al. Unexpected contribution of lymphatic vessels to promotion of distant metastatic tumor spread. Science Advances 08 Aug 2018
- Sun, J et al. Computed tomography versus magnetic resonance imaging for diagnosing cervical lymph node metastasis of head and neck cancer: a systematic review and meta-analysis. OncoTargets and therapy. 2015
- Robbins KT, Shaha AR, Medina JE, et al. Consensus statement on the classification and terminology of neck dissection. Arch Otolaryngol Head Neck Surg. 2008
- López, Fernando et al. Cervical lymph node metastases from remote primary tumor sites. Head & neck 2016
Источник
Медицинский эксперт статьи
х
Весь контент iLive проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.
Инструментальная диагностика методом ультразвукового сканирования (УЗИ), которое также называется ультрасонографией, может выявлять во внутренних органах и полостях участки с различной акустической плотностью – гиперэхогенное или гипоэхогенное образование.
Что означает гипоэхогенное образование?
Локальное гипоэхогенное образование в том или ином органе, в отличие от гиперэхогенного, является результатом более низкой эхогенности тканей – в сравнении с параметрами акустической плотности здоровых тканей органа. То есть данный участок слабо отражает направленный на него ультразвуковой сигнал (в частотных диапазонах 2-5, 5-10 или 10-15 МГц). И это свидетельство того, что данное образование – с точки зрения его структуры – либо содержит жидкость, либо имеет полость.
Гипоэхогенное образование на экране визуализируются в виде серых, темно-серых и практически черных зон (при гиперэхогенности зоны светлые, часто – белые). Для расшифровки ультразвукового изображения существует шкала шести категорий серого Gray Scale Imaging, где каждый пиксель полученного на мониторе изображения гипоэхогенного образования – в зависимости от силы ультразвукового сигнала, возвращающегося на датчики – представляет собой конкретный оттенок серого.
Расшифрованные узи-диагностами (сонографами) результаты ультразвукового обследования изучаются врачами конкретного профиля (эндокринологом, гастроэнтерологом, урологом, нефрологом, онкологом и др.), сопоставляются с показателями сданных пациентами анализов и результатами прочих исследований.
Во многих случаях требуется дифференциальная диагностика, для чего, кроме УЗИ, используются другие аппаратные методы визуализации патологии (ангиография, цветная допплерография, КТ, МРТ и т.д.), а также проводится гистологическое исследование биоптатов.
Причины гипоэхогенного образования
Как показатель ультрасонографии, гипоэхогенное образование может иметь любую локализацию. Причины гипоэхогенного образования также разные и полностью зависят от этиологии и патогенеза тех заболеваний, которые развиваются у пациентов.
Например, гипоэхогенное образование в поджелудочной железе считается диагностическим критерием выявления таких патологий, как кисты, геморрагический панкреатит, муцинозная цистоаденома (которая склонна к малигнизации), аденокарцинома головки поджелудочной железы, метастазы при злокачественных опухолях других органов.
Гипоэхогенное образование в печени и желчном пузыре
Здоровые печеночные ткани умеренно гиперэхогенны, и гипоэхогенное образование в печени может быть при циррозных очагах; очаговом стеатозе; кистах (в том числе при Echinococcus multilocularis); билиарном абсцессе; гепатоцеллюлярной аденоме; очаговой паренхиматозной гиперплазии; гепатоме и холангиоцеллюлярной аденокарциноме небольших размеров.
Гипоэхогенные образования визуализируются также в случаях распространения в печень диффузных метастазов рака поджелудочной железы, яичников, молочных желез, яичка, желудочно-кишечного тракта.
В УЗИ-диагностике патологий желчного пузыря особое значение имеет строение его стенок, так как при отсутствии повреждений органа они визуализируется в виде трех слоев: внешнего и внутреннего гиперэхогенных и среднего гипоэхогенного.
Среди причин, вызывающих гипоэхогенное образование в желчном пузыре, следует назвать полипы, аденокарциному (с интактным внешним слоем пузыря), лимфомы (опухоли лимфоузов), ангиосаркому.
Гипоэхогенные образования селезенки
В норме эхогенность селезенки однородна, хотя чуть выше, чем печени. Но из-за высокой васкуляризации УЗИ селезенки проводится с контрастным веществом, которое накапливается в паренхиме и дает возможность (в конце паренхиматозной фазы) визуализировать очаговые поражения и гипоэхогенные образования селезенки.
К числу таких образований относят:
- острую интрапаренхимальную гематому при разрыве селезенки (вследствие травмы живота);
- гемангиомы (доброкачественные сосудистые образования) при спленомегалии;
- инфаркты селезенки (инфильтративные или гематологические);
- лимфому селезенки;
- метастазы различного происхождения (чаще всего саркомы мягких тканей, остеосаркомы, рака почки, молочной железы или яичников).
Как отмечают специалисты, эхинококковые, солитерные и дермоидные кистозные образования селезенки могут иметь эхоструктуру смешанного характера.
Гипоэхогенное образование в почке, надпочечниках и мочевом пузыре
Гипоэхогенное образование в почке может быть выявлено при включениях в паренхиму кистозных образований (в том числе недоброкачественных), гематомах (на начальных стадиях), пиогенных паранефральных абсцессах (на стадии некроза) или кавернозном туберкулезе почки.
По словам эндокринологов, обнаружить гипоэхогенное образование надпочечника – задача непростая, и УЗИ, к сожалению, справляется с ней не всегда. Например, верификация диагноза аденомы при первичном альдостеронизме, а также патологической пролиферации клеток коры надпочечников при гиперкортицизме (болезни Иценко-Кушинга) базируется на симптомах. УЗИ безошибочно обнаруживает достаточно крупную феохромоцитому, а также лимфому, карциному и метастазы. Так что, обследовать надпочечники целесообразнее всего с помощью КТ и МРТ.
При развитии доброкачественной лейомиомы, переходно-клеточного рака мочевого пузыря или феохромоцитомы (параганглиомы) мочевого пузыря, которая сопровождается артериальной гипертензией и гематурией, при обследовании на УЗИ визуализируется гипоэхогенное образование в мочевом пузыре.
Гипоэхогенное образование в брюшной полости и малом тазу
Патологии, локализованные в брюшной полости, в частности, в кишечном отделе ЖКТ, беспрепятственно исследуются ультразвуком: больной пустой кишечник имеет утолщенные гипоэхогенные стенки, контрастирующие с окружающей гиперэхогенной жировой тканью.
В далеко не полном списке причин, вызывающих визуализируемое при УЗИ гипоэхогенное образование в брюшной полости, значатся:
- грыжа, выпирающая в паховый канал;
- интраабдоминальные гематомы (травматические или связанные с коагулопатиями);
- серозная и гнойная флегмона брюшины или забрюшинного пространства;
- абсцесс терминального отдела подвздошной кишки при трансмуральном илеите (болезни Крона);
- воспаление мезентериальных лимфоузлов (лимфатических узлов брыжейки);
- B-клеточная неходжкинская лимфома или лимфома Беркитта;
- метастазирование в висцеральные лимфатические узлы брюшной полости;
- карцинома слепой кишки и др.
При УЗИ органов малого таза и матки образования с низкой акустической плотностью выявляются у женщин – при наличии миомы, аденомы, кисты или эндометриоза матки; функциональной или дермоидной кист придатков. А гипоэхогенное образование в яичнике бывает при геморрагической кисте, а также тубоовариальном абсцессе (гнойном воспалении в фаллопиевых трубах и яичниках), фолликулярной лимфоме и карциноме.
У мужчин патологиями с таким диагностическим показателем являются рак яичка, лимфоцеле яичка, варикоцеле канатика, а в ходе проведения УЗИ простаты у пациентов с доброкачественной аденомой или раком данной железы визуализируется гипоэхогенное образование предстательной железы.
Гипоэхогенное образование в подключичной области
Выявленное во время УЗИ гипоэхогенное образование в подключичной области может быть признаком:
- доброкачественных новообразований и злокачественных лимфом переднего средостения;
- хронического лимфолейкоза;
- поражений периферических лимфатических узлов метастазами рака щитовидной железы, гортани, пищевода, молочных желе, легких;
- остеосарком торакальной локализации;
- кисты и эхинококкоза легких;
- тимомы или карциномы тимуса (вилочковой железы).
Гипоэхогенность структур в данной области отмечается клиницистами у пациентов с гиперплазией или кистой паращитовидных желез, гиперпаратиреозом или узелковым аденоматозом.
Виды гипоэхогенных образований
Кроме анатомо-топографической характеристики возникшего образования, ультрасонография выявляет его форму (округлую, овальную, неправильную), размер по ширине (кранио-каудальный) и глубину относительно наружной стенки органа или полости.
По этому параметру основные виды гипоэхогенного образования включают:
- округлое гипоэхогенное образование или гипоэхогенное овальное образование (это различные кисты, варикоцеле, аденомы, опухоли надпочечников метастатической этиологии);
- гипоэхогенное узловое образование (свойственное гемангиомам, узловой билиарной гипертрофии, миомам матки, узелковому аденоматозу и др.);
- гипоэхогенное очаговое образование (характерное для цирроза и очаговой жировой инфильтрации печени, гематом и инфаркта селезенки и т.д.).
В заключении проведенного УЗИ отмечаются особенности контуров изображения:
- гипоэхогенное образование с ровными контурами (кисты, узловая гипертрофия печени, опухоли молочной железы);
- гипоэхогенное образование с неровными контурами (многие опухоли, большинство метастазов);
- гипоэхогенное образование с четким контуром (кисты, аденомы, абсцессы, имеющие на ультразвуковом изображении гиперэхогенный ободок);
- гипоэхогенное образование с нечеткими контурами (кавернозные гемангионы печени, рак щитовидной железы, метастазы в ткани органов любой локализации).
Далее оценивается гомогенность/гетерогенность образования, то есть его внутренняя структура:
- гипоэхогенное однородное образование (карциномы);
- гипоэхогенное неоднородное образование (крупные аденомы, рак печени, диффузные формы карцином и др.);
- гипоэхогенное образование с гиперэхогенными включениями (почечно-клеточный рак, аденома яичника, рак предстательной железы).
В обязательном порядке дается описание состояния окружающих тканей, дистальных акустических эффектов (усиление, ослабление, акустическая тень) и особенность латеральных теней (симметричность, асимметричность, отсутствие).
Кроме того, отмечается наличие/отсутствие васкуляризации (то есть кровеносных сосудов) в образованиях узлового характера с определением таких видов, как: гипоэхогенное образование без кровотока (аваскулярное) и гипоэхогенное образование с кровотоком.
Образования, имеющие кровеносные сосуды, разделяю на:
- гипоэхогенное образование с перинодулярным кровотоком (подтип с перинодулярной, т.е. окружающей узел васкуляризацией);
- гипоэхогенное образование с сочетанным кровотоком (сосуды имеются возле образования и внутри него);
- гипоэхогенное образование с интранодулярным кровотоком (наличие васкуляризации зафиксировано только внутри образования).
Как показывает клиническая практика, гипоэхогенное образование с интранодулярным кровотоком может указывать на его злокачественный характер.
И, наконец, принимается во внимание наличие в структуре образования соединений кальция. И гипоэхогенное образование с кальцинатами (кальцинозом) характерно для инкапсулированного хронического абсцесса печени при амебиазе, рака печени, новообразований в щитовидной и предстательной железе, злокачественных опухолей молочной железы и др.
Лечение
Пациенты могут спросить врача, какое лечение гипоэхогенного образования необходимо, и какие лекарства для этого назначаются… Но лечат не обнаруженные с помощью ультразвука аномальные участки, а заболевания, повлекшие патологическое изменение плотности ткани, слабо отражающей ультразвуковые волны.
Источник