Цитокины вырабатываемые т лимфоцитами хелперами 1 типа
CD4+ Лимфоциты выполняют главным образом хелперную функцию,
однако следует отметить, что при некоторых обстоятельствах CD4+ клетки могут
выполнять и киллерную функцию. Выполняя свою основную хелперную функцию, они
помогают, во-первых, В-клеткам превращаться в антителопродуцирующую
плазматическую клетку; во-вторых, CD8+ лимфоцитам – в зрелую цитотоксическую
Т-клетку; в-третьих, макрофагам осуществлять эффекты гиперчувствительности
замедленного типа. Указанные функции Т-лимфоцитов-хелперов реализуются за счет
того, что они в свою очередь разделяются на две субпопуляции – 1-го и 2-го типа,
выполняющие разные хелперные функции за счет продукции разных цитокинов –
интерлейкинов.
Т-лимфоциты-хелперы 1-го типа (Tx1) продуцируют
гамма-интерферон (ИНФ), ИЛ-2 и альфа-опухольнекротизирующий фактор (ОНФ).
Указанные цитокины активируют макрофаги, ЕК-к летки, созревание цитотоксических
Т-лимфоцитов-киллеров, обеспечива я преимуществен-ное развитие клеточного
иммунного ответа, в том числе, при внутриклеточной инфекции.
Напротив, Т-лимфоциты-хелперы 2-го типа (Тх2) продуцируют
ИЛ-4, ИЛ-5, ИЛ-10 и ИЛ-13, которые отвечают за развитие гуморального ответа, в
том числе, за продукцию IgE. Кроме того, ИЛ-10 обладает ингибирующим эффектом
по отношению к Tx1.
Tx1 и Тх2 различаются не только по способности продуцировать
различные цитокины, но и по наличию на своей поверхности различных
активационных маркеров. Так, после активации на мембране Тх2 экспрессируется
CD30 (молекула, относящаяся к семейству рецепторов для опухольнекротизирующего
фактора), а на поверхности активированных Tx1 появляется LAG-3 (молекула,
относящаяся к суперсемейству иммуноглобулинов).
Одним из важнейших регуляторных цитокинов, поддерживающих
баланс между Т-хелперами 1-го и 2-го типа, является ИЛ-12, который
продуцируется макрофагами. ИЛ-12 увеличивает количество Т-хелперов 1-го типа,
помогая таким образом хозяину защититься против микроорганизмов, которые
контролируются клеточным иммунным ответом. Другой важный регуляторный компонент
– это гамма-интерферон, который подавляет функционирование Т-хелперов 2-го типа.Со
своей стороны, Т-хелперы 2-го типа мог ут п роду цировать ИЛ-10, который явл
яется су п рес-сивным интерлейкином и подавляет функцию Т-лимфоцитов-хелперов
1-го типа. В настоящее время принято считать, что цитокины, которые
продуцируются Tx1 и Тх2, используются как аутокринные факторы, и как факторы,
способные вызывать реципрокную супрессию (взаимное подавление функции).
Как видно из схемы, на ранних этапах иммунного ответа под
влиянием ИЛ-12, который продуцируется антигенпредставляющей клеткой (АПК),
дифференцировка Тх0 идет преиму-щественно в сторону созревания Tx1, которые
начинают продуцировать ИЛ-2, гамма-ИНФ и альфа-ОНФ. В случае воздействия на Тх0
ИЛ-4, который продуцируется тканевыми базофила-ми (тучными клетками) и
базофильными гранулоцитами крови, Тх0 начинают дифференциро¬ваться в Тх2 и
продуцировать свой цитокиновый профиль: ИЛ-4, ИЛ-5, ИЛ-10, ИЛ-13. Гамма-ИНФ и
ИЛ-10 способны рецикпрокно подавлять функционирование Tx1 и Тх2.
ИЛ-12 обладает способностью не только влиять на созревание
Tx1, но и стимулировать их пролиферацию как паракринный фактор. Точно так же
действует и ИЛ-4 на Тх2: он сначала индуцирует дифференцировку Тх2, а затем уже
как аутокринный фактор способствует их пролиферации.
Обнаружено, что Txl и Тх2 ответственны за развитие различных
иммунопатологических реакций у человека. Так, например, функция Txl преобладает
при развитии множественного (рассеянного) склероза, инсулинозависимого
сахарного диабета, аутоиммунного тиреоидита, бо-лезни Крона, острого отторжения
аллотрансплантата. привычного невынашивания плода и др. В свою очередь, функция
Тх2 преобладает при нормально протекающей беременности, трансплантационной
толерантности, идиопатическом легочном фиброзе, прогрессирующем системном
склерозе, у ВИЧ-инфицированных больных с быстрым прогрессированием заболевания,
а также при аллергической патологии.
Таким образом, Т-лимфоциты-хелперы 1-го и 2-го типа представляют
собой важнейшие субпопуляции Т-лимфоцитов, от функционального баланса которых
зависит направленность иммунного ответа в норме и особенности клинических проявлений
при развитии иммунопатологии. На этом основании Т-хелперы получили название
“дирижеры иммунного ответа”. Другая субпопуляция Т-лимфоцитов, меньшая по
количеству, несет на своей поверхности от-личительный признак в виде молекулы
CD8 и относится, как уже упоминалось, к Т-лимфоцитам-киллерам/супрессорам.
Такое двойное название означает, что эта субпопуляция Т-лимфоцитов может
дифференцироваться либо в Т-киллер (цитотоксический Т-лимфоцит), либо в
Т-супрессор и выполнять различные функции в зависимости от потребностей
организма.
Источник
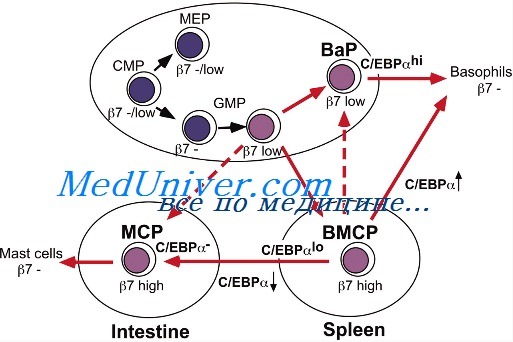
Дифференцировка Т- и В-клеток. Цитокины индуцирующие дифференцировку клеток Тh1-типа – тип I интерферонов (IFN-а)Цитокины регулируют взаимодействия между клетками врожденного и адаптивного иммунного ответа. Функциональная активность цитокинов определяет направление дифференцировки Т-клеток в Th1/ Тс1 или Тh2/Тс2 тип, а также определяет класс иммуноглобулинов, на продукцию которого переключаются В-кпетки. Тип I интерферонов (IFN-а) был идентифицирован одним из первых среди цитокинов, обладающих антивирусной активностью и оказывающих влияние на клетки врожденного иммунитета. Как недавно выявлено, INF играют важную роль в интеграции врожденного и адаптивного иммунитета путем действия на ДК и Т-клетки. Ряд IFN-a/b определяет большую группу скрыто родственных цитокинов, которые активируются при связывании с общим INF-ab рецептором. Эти цитокины включают: IFN-a. IFN-a образуют моноциты, макрофаги, нейтрофилы, NK и В-лимфоциты, а IFN-b — фибробласты, эпителиальные клетки, макрофаги. Плазмацитоидные предшественники ДК рассматриваются как важнейший тип клеток, продуцирующих тип IIFN (IFN-a/p). Они были названы как натуральные интерферон-продуцирующие клетки — NIPCs. Эти цитокины не только непосредственно ингибируют вирусную репликацию, но также активируют иммунные эффекторы, такие как NK, CTL и макрофаги для элиминации инфицированных клеток. IFN-a/b способствуют ускорению дифференцировки GM-CSF-обработанных человеческих моноцитов в ДК, стимулирующие активность Т-клеток. Анализ экспрессии маркеров ДК и их миграционного ответа на хемокины показал, что обработка ДК IFN-a/b индуцирует функциональное созревание этих клеток. Противовирусное действие интерферонов связывают с их способностью подавлять процессы транскрипции вирусного генома, а противоопухолевое действие — с подавлением пролиферации клеток вследствие активации аденилатциклазы и повышения уровня цАМФ внутри клетки.
При этом активируется протеинкиназа А, фосфорилирующая белки, подавляется пролиферация и включаются процессы дифференцировки иммунокомпетентных клеток, активируются NK, CTL, макрофаги. IFN-a/B повышают экспрессию молекул МНС на клетках различного типа. Тип II интерферонов (INF-y), является мощным активатором антимикробных функций фагоцитов и играет ключевую роль в резистентности ко многим патогенным бактериям, грибкам и внутриклеточным паразитам. Он продуцируется в ответ на действие IFN-a/b, вырабатываемых клетками врожденного иммунитета. Источником INF-y являются в основном Th1 клетки и NK, но и другие эффекторы при соответствующей стимуляции также способны секретировать INF-y: Т-клетки (NKT, CD8-T-клетки, и убТ-клетки), макрофаги, ДК, и В-клетки. Высвобождение INF-y активирует NK и нейтрофилы, стимулирует микробицидную активность макрофагов и индуцирует формирование гранулем, которые играют барьерную функцию для сдерживания внутриклеточных патогенов. Оба типа 1 и 2 интерферонов активируют NK клетки для уничтожения инфицированных вирусом клеток и высвобождения цитокинов. При проникновении в организм патогенов происходит активация макрофагов и ДК, которые начинают секретировать IL-12, TNF-a, IL-18, IL-1. IL-12 и IL-18 стимулируют выработку INF-y NK клетками и Т-лимфоцитами. INF-y с IL-12 индуцируют дифференцировку CD4 клеток в Th1, характеризующиеся способностью к продукции INF-y, IL-2 и лимфотоксина-a. Кроме того, INF-y способен ингибировать дифференцировку CD4′ клеток в Тп2 тип, синтезирующий IL-4, 5, 10, которые являются мощными ингибиторами цитокинов ТЫ типа. INF-y также активирует макрофагальную микробицидную активность через индукцию TNF-a, реактивного кислорода и NO-интермедиатов и повышает экспрессию молекул МНС и рецепторов TNF-a. При различных инфекциях (Brucella abortus, Micobacterium fortuitum, C. albicans, Klebsiella pneumoniae) немаловажную защитную роль играют также нейтрофилы, активность которых усиливается под воздействием INF-y. – Также рекомендуем “Интерлейкин-2 (IL-2). Интерлейкин-6, 12 (IL-6, 12)” Оглавление темы “Организация иммунного ответа”:
|
Источник
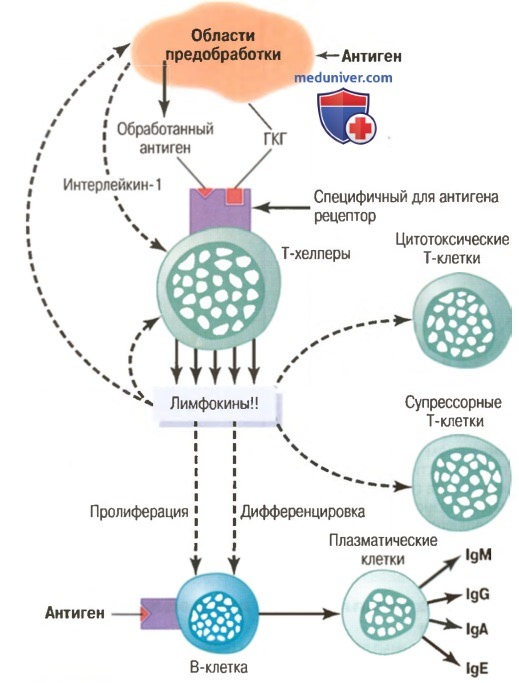
Т-хелперы. Функции лимфокиновСейчас ясно, что существуют много типов Т-клеток. Их подразделяют на три основных группы: (1) Т-хелперы; (2) цитотоксические Т-клетки (3); супрессорные Т-клетки. Функции каждой группы клеток различны. а) Т-хелперы. Их роль в общей регуляции иммунитета. Общепризнано, что Т-хелперы — наиболее многочисленные Т-лимфоциты, они обычно составляют более 75% всех Т-клеток. Согласно названию, эти клетки помогают функциям иммунной системы. Фактически они являются главным регулятором почти всех иммунных функций, как показано на рисунке ниже. Такое действие Т-хелперов связано с формированием ими ряда белковых медиаторов, называемых лимфокинами, которые действуют на другие клетки иммунной системы, а также на клетки костного мозга. Далее перечислены важные лимфокины, секретируемые Т-хелперами: • интерлейкин-2; • интерлейкин-3; • интерлейкин-4; • интерлейкин-5; • интерлейкин-6; • гранулоцитарно-моноцитарный колоние-стимулирующий фактор; • интерферон-у.
б) Специфические регуляторные функции лимфокинов. При отсутствии лимфокинов, выделяемых Т-хелперами, остальная иммунная система почти парализована. Действительно, именно Т-хелперы инактивируются или разрушаются вирусом синдрома приобретенного иммунодефицита, который оставляет организм почти полностью незащищенным против инфекционных заболеваний, что является причиной хорошо известных в настоящее время ослабляющих здоровье и губительных для организма эффектов СПИД. Некоторые из специфических регуляторных функций изложены далее. в) Стимуляция роста и размножения цитотоксических и супрессорных Т-клеток. При отсутствии Т-хелперов клоны, формирующие цитотоксические и супрессорные Т-клетки, большинством антигенов активируются лишь незначительно. Лимфокин интерлейкин-2 обладает особо сильным стимулирующим влиянием на рост и размножение цитотоксических и супрессорных Т-клеток. Некоторые другие лимфокины также имеют влияние, но менее мощное. г) Стимуляция роста и дифференцировки В-клеток до стадии формирования плазматических клеток и антител. Непосредственное действие антигена, вызывающее рост и размножение В-клеток, формирование плазматических клеток и секрецию антител, также незначительно без «помощи» Т-хелперов. Почти все интерлейкины участвуют в реакции В-клеток, но особенно интерлейкин-4, -5 и -6. Эти три интерлейкина имеют такой мощный эффект на В-клетки, что их назвали факторами, стимулирующими В-клетки, или факторами роста В-клеток. д) Активация макрофагальной системы. Лимфокины влияют также на макрофаги. Во-первых, они замедляют или прекращают миграцию макрофагов после их хемотаксического притяжения в область воспаленной ткани, в результате здесь происходит значительное скопление макрофагов. Во-вторых, лимфокины активируют макрофаги, резко увеличивая эффективность фагоцитоза, что позволяет макрофагам атаковать и разрушать большее количество внедрившихся бактерий или других агентов, повреждающих ткани. е) Стимулирующее влияние на Т-хелперы по принципу обратной связи. Некоторые из лимфокинов, особенно интерлейкин-2, оказывают прямое влияние, стимулирующее активацию самих Т-хелперов по принципу положительной обратной связи. Это значит, что лимфокин действует как усилитель, дополнительно увеличивая реакцию Т-хелперов, а также весь иммунный ответ на внедрившийся агент. – Также рекомендуем “Цитотоксические Т-клетки. Супрессорные Т-клетки” Оглавление темы “Механизмы Т-клеточного иммунитета. Антигены клеток крови”: |
Источник
Т-клетки это фактически приобретенный иммунитет, способный защитить от цитотоксического повреждающего воздействия на организм. Чужеродные клетки-агрессоры, попадая в организм вносят “хаос”, который внешне проявляется в симптомах заболеваний.
Клетки-агрессоры повреждают по ходу своей деятельности в организме все, что могут, действуя в своих интересах. А задача иммунной системы найти и уничтожить все чуждые элементы.
Специфическая защита организма от биологической агрессии (чужеродных молекул, клеток, токсинов, бактерий, вирусов, грибов и т.д.) осуществляется при помощи двух механизмов:
- продуцирования специфических антител в ответ на чужеродные антигены (потенциально опасных для организма веществ);
- выработки клеточных факторов приобретённого иммунитета (Т-клетки).
Как осуществляются иммунные реакции
При попадании в организм человека «клетки-агрессора», иммунная система распознаёт чужеродные и собственные измененные макромолекулы (антигены) и удаляет их из организма. Также при первичном контакте с новыми антигенами происходит их запоминание, что способствует их более быстрому удалению, в случае вторичного попадания в организм.
Процесс запоминания (презентация) происходит благодаря антиген-распознающим рецепторам клеток и работе антиген представляющих молекул (МНС молекул- комплексов гистосовместимости).
Что такое Т-клетки иммунной системы, и какие функции они выполняют
Функционирование иммунной системы обуславливается работой лимфоцитов. Это клетки иммунной системы, являющиеся
разновидностью лейкоцитов и способствующие формированию приобретённого иммунитета. Среди них выделяют:
- В-клетки (распознающие «агрессора» и вырабатывающие к нему антитела);
- Т-клетки (выполняющие функцию регулятора клеточного иммунитета);
- NК- клетки (разрушающие отмеченные антителами чужеродные структуры).
Однако, помимо регуляции иммунного ответа, Т-лимфоциты способны выполнять эффекторную функцию, разрушая опухолевые, мутировавшие и чужеродные клетки, участвовать в формировании иммунологической памяти, распознавать антигены и индуцировать иммунные реакции.
Справочно. Важной особенностью T-клеток является их способность реагировать только на презентированные антигены. На одном T-лимфоците находится только один рецептор к одному конкретному антигену. Это обеспечивает отсутствие реакции T-клеток на собственные аутоантигены организма.
Разнообразие функций Т-лимфоцитов обусловлено наличием в них субпопуляций, представленных Т-хелперами, Т-киллерами и Т-супрессорами.
Субпопуляция клеток, их стадия дифференцирования (развития), степень зрелости и т.д. определяется при помощи специальных кластеров дифференцировки, обозначаемых как СD. Наиболее значимыми являются СD3, СD4 и СD8:
- СD3 находится на всех зрелых T-лимфоцитах, он способствует передаче сигнала от рецептора к цитоплазме. Это важный маркер функционирования лимфоцитов.
- СD8 – это маркер цитотоксических T-клеток.
- СD4 является маркером T-хелперов и рецептором к ВИЧ (вирус иммунодефицита человека)
Т-хелперы
Около половины Т-лимфоцитов имеют антиген CD4, то есть являются Т-хелперами. Это помощники, стимулирующие процесс секреции антител В-лимфоцитами, стимулируют работу моноцитов, тучных клеток и предшественников Т-киллеров к «включению» в иммунную реакцию.
Справочно. Функция хелперов осуществляется за счёт синтеза цитокинов (информационных молекул, регулирующих взаимодействие между клетками).
В зависимости от продуцируемого цитокина, их разделяют на:
- T-хелперные клетки 1-го класса (продуцируют интерлейкин-2 и гамма-интерферон, обеспечивая гуморальный иммунный ответ на вирусы, бактерии, опухоли и трансплантанты).
- T-хелперные клетки 2-го класса (секретируют интерлейкины-4,-5,-10,-13 и отвечают за образование IgЕ, а также иммунного ответа, направленного на внеклеточные бактерии).
Т-хелперы 1-го и 2-го типа всегда взаимодействуют антагонистически, то есть повышенная активность первого типа угнетает функцию второго типа и наоборот.
Работа хелперов обеспечивает взаимодействие между всеми клетками иммунитета, определяя какой тип иммунного ответа будет преобладать (клеточный либо гуморальный).
Важно. Нарушение работы клеток-помощников, а именно недостаточность их функции, наблюдается у больных с приобретённым иммунодефицитом. Т-хелперы являются основной мишенью ВИЧ. В результате их гибели нарушается иммунная реакция организма на стимуляцию антигенов, что приводит к развитию тяжёлых инфекций, росту онкологических новообразований и летальному исходу.
Т-киллеры
Это так называемые T-эффекторы (цитотоксические клетки) или клетки убийцы. Такое название обусловлено их способностью уничтожать клетки-мишени. Осуществляя лизирование (ли́зис (от греч. λύσις — разделение) — растворение клеток и их систем) мишеней, переносящих чужеродный антиген или мутировавший аутоантиген (трансплантанты, опухолевые клетки), они обеспечивают реакции противоопухолевой защиты, трансплантационного и противовирусного иммунитета, а также аутоиммунные реакции.
Т-киллеры при помощи собственных МНС-молекул распознают чужеродный антиген. Связываясь с ним на поверхности клетки, они продуцируют перфорин (цитотоксический белок).
После лизирования клетки «агрессора» Т-киллеры остаются жизнеспособными и продолжают циркулировать в крови, разрушая чужеродные антигены.
Т-киллеры составляют до 25-ти процентов от всех Т-лимфоциотов.
Справочно. Помимо обеспечения реакций нормального иммунного ответа, Т-эффекторы могут участвовать в реакциях антителозависимой клеточной цитотоксичности, способствуя развитию гиперчувствительности второго типа (цитотоксической).
Это может проявляться лекарственными аллергиями и различными аутоиммунными заболеваниями (системные заболевания соединительной ткани, гемолитическая анемия аутоиммунного характера, злокачественная миастения, аутоиммунные тиреоидиты, и т.д.).
Подобным механизмом действия обладают некоторые лекарственные средства, способные запускать процессы некроза опухолевых клеток.
Важно. Препараты с цитотоксическим действием используют в химиотерапии онкологических заболеваний.
Например, к таким медикаментам относится Хлорбутин. Это средство применяют для лечения хронического лимфолейкоза, лимфогранулематоза и рака яичников.
Т-супрессоры и клетки памяти
Супрессоры подавляют функцию хелперов и В-лимфоцитарного звена. Однако современная классификация не выносит супрессоры в отдельную субпопуляцию. Поскольку доказано, что решающую роль в угнетении иммунной реакции играют апоптоз и специфические цитокины.
Помимо основных T-лимфоцитов, в организме человека существуют потомки клеток, контактировавших с антигеном и имеющих к нему рецепторы. Это клетки обеспечивающие иммунологическую память. Они способны в течение от десяти до 15 лет сохранять память об антигене, передавая её другим клеткам.
Справочно. Благодаря клеткам памяти обеспечивается быстрый иммунный ответ при повторном попадании «агрессора» в организм.
Нулевые лимфоциты
К ним относят лимфоциты, не имеющие T и B маркеров. Они составляют до 10% от всей популяции лимфоцитов. К ним относят NК-клетки (естественные киллеры) и K-клетки (киллерные).
Справочно. Основным отличием NK-клеток от T-киллеров является способность уничтожать не сенсибиллизированные клетки-мишени.
K-клетки отвечают за антителозависимую клеточную цитотоксичность. Они отражают взаимодействия гуморального и клеточного звеньев иммунитета, а также выступают в качестве «наводчиков» эффекторных (выполняющих функцию – в данном случае уничтожение) клеток на мишень.
NК- клетки обеспечивают контроль за качеством клеток и участвуют в формировании противовирусного иммунитета, обеспечиваютзащиту от роста опухолей и размножения мутировавших (дефектных) клеток.
Диагностика клеточного иммунитета
Диагностика T- и B-лимфоцитарного звена позволяет оценить состояние клеточного иммунитета. Базовое исследование с определением процентного содержания Т-, В- и нулевых клеток проводится с целью выявления первичных или вторичных иммунодефицитов, а также при контроле иммуностимулирующего лечения.
Исследование основных популяций при помощи маркеров CD3, 8, 19, 16+5б, а также соотношение между хелперами и киллерами, позволяет комплексно оценить иммунный статус. Для исследования используют венозную кровь.
Диагностика проводится при выявлении и контроле течения:
- аутоиммунных заболеваний (увеличено содержание CD3, CD4 хелперов);
- лимфолейкозов (повышено количество Т-лимфоцитов CD3);
- злокачественных новообразований (увеличено количество NK);
- ВИЧ (CD3, CD8);
- хронических инфекций, аллергических реакций, бронхиальной астмы и т.д.
Справочно. В зависимости от результатов анализа пациенту может быть рекомендована консультация иммунолога, гематолога, аллерголога, онколога или инфекциониста. С дальнейшим лечением у профильного специалиста по основному заболеванию.
Источник