Антиген распознающие рецепторы в и т лимфоцитов
Оглавление темы “Селезенка. Лимфатические узлы. Стадии иммунного ответа. Формы иммунного ответа. Воспаление. Механизмы, контролирующие иммунную систему.”:
1. Селезенка. Функции селезенки. Лимфатические узлы. Функции лимфатических узлов.
2. Мукозно-ассоциированная лимфоидная ткань. Лимфоидная ткань слизистых оболочек.
3. Стадии иммунного ответа. Формы иммунного ответа. Воспаление. Ранний защитный воспалительный ответ.
4. Представление антигена. Распознавание антигена. Взаимодействие Т-хелперов ( Тh1 ) с антигенпредставляющими клетками.
5. Активация Т- и В-лимфоцитов в иммунном ответе. Активация лимфоцитов. Формы специфического иммунного ответа.
6. Клеточный иммунный ответ. Гуморальный иммунный ответ. Защитные функции иммуноглобулинов ( антител ).
7. Иммуноглобулин G ( IgG ). Иммуноглобулин М ( IgM ). Функции иммуноглобулинов G и М.
8. Иммуноглобулин A ( IgA ). иммуноглобулин Е ( IgE ). Функции иммуноглобулинов А и Е.
9. Формы специфического иммунного ответа. Иммунологическая память как вид имунного ответа.
10. Иммунологическая толерантность. Механизмы, контролирующие иммунную систему. Гормональный контроль имумнной системы.
11. Цитокиновый контроль имунной системы. Местное действие цитокинов. Механизм действия цитокинов на иммунитет.
Представление антигена. Распознавание антигена. Взаимодействие Т-хелперов ( Тh1 ) с антигенпредставляющими клетками.
В случае неэффективности раннего защитного ответа и факторов врожденного иммунитета в организме накапливаются микроорганизмы, содержащие чужеродные антигены. Контакт этих антигенов с клетками иммунной системы приводит к развитию специфического иммунного ответа, который начинается с этапа представления и распознавания антигена.
Растворимые антигены в нативной форме связываются антителами и антигенраспознающими иммуноглобулиновыми рецепторами В-клеток.
Т-лимфоциты своими антигенраспознающими Т-клеточными рецепторами связывают короткие пептидные фрагменты белковых антигенов в комплексах с собственными молекулами главного комплекса гистосовместимости I или II классов на мембранах антигенпредставляющих клеток.
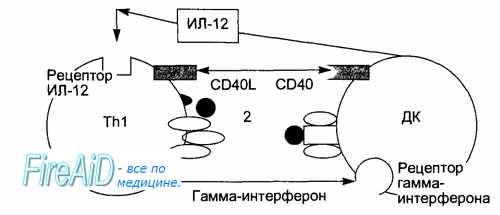
Рис. 8.8. Взаимодействие Т-хелперов (Тh1) с антигенпредставляющими дендритными клетками (ДК) опосредовано цитокинами (ИЛ-12, гамма-интерферон) и кости-мулирующими молекулами (CD40, CD40L).
В центре «иммунологического синапса» находятся: Т-клеточный антиген распознающий рецептор (1) и распознаваемый им комплекс антигенного пептида с молекулой главного комплекса гистосовместимости (2).
Молекулы главного комплекса гистосовместимости на поверхности лейкоцитов человека, получили название «человеческие лейкоцитарные антигены» (Human Leukocyte Antigens — HLA). Молекулы главного комплекса гистосовместимости I класса присутствуют на поверхности всех типов клеток, кроме эритроцитов и клеток трофобласта. Молекулы главного комплекса гистосовместимости II класса находятся на поверхности антигенпредставляющих клеток: дендритных клеток, макрофагов, В-лимфоцитов.
Антигенпредставляющие клетки играют важную роль на начальном (пусковом) этапе специфического иммунного ответа:
1) макрофаги, как правило, представляют антигены бактериального происхождения — продукты захвата и внутриклеточной переработки ими бактерий,
2) В-лимфоциты представляют микробные антигены, антигены токсинов, связанные их поверхностными иммуноглобулиновыми рецепторами,
3) наиболее универсальными антигенпредставляющими клетками являются дендритные клетки, которые необходимы для запуска первичного иммунного ответа, представляют многие, в том числе опухолевые, антигены.
После захвата чужеродного белка — антигена этими клетками и его разложения до коротких пептидов внутри клеток происходит комплексирова-ние отдельных молекул главного комплекса гистосовместимости с конкретными пептидами. Такие комплексы транспортируются на поверхность антигенпредставляющих клеток (рис. 8.8).
При встрече антигенпредставляющей клетки с Т-лимфоцитом, несущим на своей поверхности подходящий по структуре антигенраспознающий рецептор, замыкается лиганд-рецепторная связь, т. е. происходит распознавание антигена.
CD4+ T-лимфоциты способны распознавать антигенные пептиды в комплексах с собственными молекулами главного комплекса гистосовместимости II класса, a CD8+ Т-лимфоциты — в комплексах с собственными молекулами главного комплекса гистосовместимости I класса. Связывание антигена Т-клеточным рецептором служит сигналом усиления пролиферации данного Т-лимфоцита с последующей ускоренной дифференцировкой и активацией его клеток-потомков. В результате формируется клон Т-лим-фоцитов, способных при встрече с тем же антигеном быстро активироваться для участия в удалении патогенного агента.
– Также рекомендуем “Активация Т- и В-лимфоцитов в иммунном ответе. Активация лимфоцитов. Формы специфического иммунного ответа.”
Источник
РЕЦЕПТОРЫ ЛИМФОЦИТОВ
ГЛАВНЫЙ КОМПЛЕКС ГИСТОСОВМЕСТИМОСТИ
·Особенности представления антигенов В- и Т-лимфоцитам. Понятие о В- и Т-эпитопах в структуре антигенов.
·Антигенраспознающие рецепторы В-лимфоцитов: базисные рецепторы и их перестройка в ходе иммунного ответа.
·Основная категория антигенраспознающих рецепторов Т-лимфоцитов. Строение, сходство и различия с рецепторами В-лимфоцитов. Принцип двойного распознавания антигенов Т-лимфоцитами.
·Механизмы усиления антигенного сигнала (понятие о рецепторных комплексах В- и Т-лимфоцитов).
·Молекулярные и субмолекулярные основы клонированности В- и Т-лимфоцитов.
·Главный комплекс гистосовместимости (МНС/HLA): гены и их продукты. Этимология акронима «HLA». Иммунологические функции основных классов МНС.
·MHС и антигенная индивидуальность. Генетические основы МНС-полиморфизма. МНС-полиморфизм как основа для отторжения аллогенных тканей. HLA-фенотип и патология.
·Молекулы МНС/HLA-I. Принцип строения, подклассы, структурный (аллельный) полиморфизм, тканевая локализация, иммунологическая функция.
·МолекулыМНС/HLA-II. Принцип строения, подклассы, структурный (аллельный) полиморфизм, распространение в организме, иммунологическая функция.
·Понятие об МНС/HLA-рестрикции иммунного ответа (двойное распознавание антигенов). Молекулярные основы избирательного взаимодействия CD4 и СD8 Т-лимфоцитов c антигенами, представляемыми молекулами МНС-I и MHC-II. «Профессиональные» и «непрофессиональные» антигенпредставляющие клетки.
·Процессинг и презентация антигенов Т-лимфоцитам. Особенности МНС-I и МНС-II зависимого представления антигенов. Понятие об антигенных пептидах, представляемых молекулами МНС (МНС/HLA-пептиды).
·МНС-зависимая регуляция иммунного ответа. Связь с экспрессией молекул МНС и МНС-рестрикцией иммунных реакций. Понятие об Ir-генах.
Рецепторы В-лимфоцитов (BCR1)
Иммуноглобулины (антитела) не только секретируются во внешнюю среду, но входят в состав плазматической мембраны В-лимфоцитов. В этом случае они функционируют как рецепторы, которые распознают антигены и запускают активацию клеток. До контакта с антигеном (наивные В-лимфоциты) преобладающим изотипом мембранных иммуноглобулинов является IgM (mIgM)2. В отличие от сывороточной (пентамерной) формы, mIgM представляет собой мономер, снабженный дополнительным гидрофобным доменом, который обеспечивает заякоривание на плазматической мембране3. По ходу иммунного ответа происходит смена изотипа рецепторов на IgG, IgA и IgE. Это совпадает с переключением класса секретируемых антител: после короткого IgM-всплеска начинают доминировать IgG-антитела. При повторном контакте с антигеном IgG-антитела преобладают с самого начала, отражая перестройку рецепторов в клетках памяти. Специфичность рецепторов каждой клетки одинакова, совпадая со специфичностью секретируемых антител. Это связано с унификацией и уникальностью генов, детерминирующих синтез иммуноглобулинов дискретными клонами лимфоцитов.
Рекогносцировочная функция иммуноглобулиновых рецепторов получает развитие благодаря трасляции антигенного сигнала внутрь клетки. В этом участвуют две вспомогательных молекулы, контактирующие с mIg – CD79a и CD79b4. Их цитоплазматические фрагменты ассоциированы с внутриклеточными ферментами (тирозинкиназами), активация которых запускает каскадный процесс, ведущий к поэтапному изменению экспрессии генов, т.е. к реакциям, характерным для рецепторзависимой стимуляции любых клеток. Здесь это выражается в пролиферации и дифференицировке наивного В-лимфоцита в клетки-эффекторы (антителопродуцирующие плазмоциты) и клетки памяти.
Рецепторы Т-лимфоцитов (TCR1)
Мембранные структуры Т-лимфоцитов, распознающие антигены, имеют много общего с иммуноглобулинами и, следовательно, с рецепторами В-лимфоцитов. Рецептор большинства (более 95%) Т-лимфоцитов представляет гетеродимер, состоящий из двух пептидных (точнее гликопептидных) цепей – α и β (рис. 1). Они скреплены дисульфидной связью и имеют м. м. 40-50кДа. Каждая из цепей состоит из двух функционально различных участков – вариабельного ((Vα, Vβ) и константного (Сα, Сβ). Вариабельные участки оформлены в виде доменов, которые образуют антигенсвязывающий центр TCR. Это означает, что они клоноспецифичны, т.е. отличаются у Т-лимфоцитов, реагирующих на разные антигены.
Небольшая фракция Т-лимфоцитов располагает рецепторами типа γ/δ. По своему устройству они аналогичны α/β рецепторам, но отличаются по первичной структуре и имеют ряд функциональных особенностей. Их вариабельность гораздо ниже (ограниченная клоноспецифичность), они распознают антигены в комплексе с «неклассическими» (не МНС) антигенпредставляющими молекулами (например, CD1) или даже свободные антигены. В качестве антигенных детерминант могут выступать производные липидов, гликолипидов и других непептидных соединений. γ/δ-клетки имеют тенденцию к локализации в определенных анатомических зонах, прежде всего в слизистых оболочках. Закономерности и значение их реакций стали исследоваться недавно.
Так же, как у антител, структурная индивидуальность (клоноспецифичность) вариабельных доменов (Vα и Vβ) сконцентрирована в трех гипервариабельных участках – CDR1-CDR3 (от англ. Complementarity Determining Regions). Именно из их комбинации образуется «ловушка» для связывания антигена. Константные фрагменты (Сα, Сβ) обеспечивают фиксацию TCR на клеточной мембране и функциональные контакты с медиаторными (транслирующими антигенный сигнал) молекулами.
Домены TCR аналогичны иммуноглобулиновым доменам. Для них характерна глобулярная конформация с укладкой пептидной цепи (70- 110 аминокислот) в виде антипараллельной β-складчатой структуры, скрепленной дисульфидной связью. Известно много молекул, которые содержат элементы, сходные с вариабельными или константными доменами иммуноглобулинов. Обычно это мембранные гликопротеины, выполняющие различные функции внутри и за пределами иммунной системы (рецепторы, молекулы контактного взаимодействия и пр.) Они объединены в «суперсемейство иммуноглобулинов», а их гены ( имеющие эволюционное родство) – в «суперсемейство иммуноглобулиновых генов».
В отличие от рецепторов В-лимфоцитов, TCR не секретируются во внешнюю среду и не меняются в процессе иммуногенеза (отсутствие изотипии, постоянная аффинность). Но главной особенностью является механизм распознавания антигенов: мишенью для Т-лимфоцитов служат антигены, связанные с поверхностью собственных клеток; свободные антигены не воспринимаются. Информация о структурной чужеродности для Т-лимфоцитов формируется при участии мембранных молекул, “специализирующихся” на представлении (презентации) антигенов. Они относятся к системе главного комплекса гистосовместимости – MHC (от англ. Major Histocompatibility Complex) и экспрессируются на поверхности антигенпредставляющих клеток, “прихватывая” фрагменты антигенов. Не меняясь в классическом смысле, понятие “антиген” для Т-лимфоцитов является более сложным, чем для В-клеток, реагирующих на свободные антигены. Полноценный Т-антиген представляет комплекс антигенного пептида (Т-эпитопа) и молекулы МНС. Только такая комбинация из “чужого” и “своего” воспринимается рецепторами Т-клеток. Это означает, что TCR обладает двойной специфичностью, или двойным распознаванием. Говорят также, что Т-лимфоциты рестриктированы по МНС, так как их реакции напрямую зависят от продуктов МНС-генов (лат. restrictio – ограничение). МНС-рестрикция нацеливает Т-лимфоциты на клетки, ставшие чужеродными и потенциально опасными для организма, устраняя (или по крайней мере сокращая) вероятность случайной атаки.
Восприняв информацию об антигене, TCR не может самостоятельно
превратить ее в сигнал, активирующий клетку. Для этого требуются вспомогательные (костимулирующие) молекулы. Наиболее тесной является связь между TCR и комплексом из четырех трансмембранных полипептидов (g, d, e и x), собирательно обозначаемых как CD31. Они контактируют с С-участками TCR, улавливая конформационные изменения, вызываемые связыванием антигена МНС-пептида). Растормаживая активационный каскад, СD3-комплекс содействует трансляции антигенного сигнала внутрь клетки, наполняя его функциональным содержанием.
Цитоплазматические концы молекул CD3-комплекса связаны с тирозинкиназами, инициирующими.эстафетное фосфорилирование-дефосфорилирование внутриклеточных белков, в том числе регуляторов транскрпции генов, поддерживающих активационный процесс. Это один из стандартных механизмов рецепторзависимой стимуляции клеток. Он характерен для большинства костимулирующих и рецепторных молекул Т- , В-лимфоцитов и других клеток иммунной системы.
Формирование активационного сигнала зависит от прочности связи между TCR и МНС-презентируемым антигеном. В ее укреплении существенную роль играют корецепторы, прежде всего молекулы CD4 и CD8, альтернативно представленные на двух основных категориях зрелых Т-клеток (см. лекция 1). Они обладают сродством к молекулам МНС, многократно повышая эффективность антигенной стимуляции Т-лимфоцитов антигеном (см. рис. 2).
Кроме стабилизации физических контактов, CD4 и CD8 участвовуют в формировании активационного сигнала, т.е. обладают костимулирующей активностью. Это происходит благодаря связи их цитоплазматических фрагментов с тирозинкиназой.
Кроме CD4 и CD8, которые взаимодействуют с антигенпрезентирующими молекулами, фиксация Т-лимфоцитов на вспомогательных клетках и клетках-мишенях усиливается адгезивными молекулами (молекулами контактного межклеточного взаимодействия). Их действие физически дистанцировано от TCR, хотя костимулирующий эффект может быть значительным (см. “Индукция иммунного ответа”).
Источник
Презентация
антигена, кооперация иммунокомпетентных клеток
Презентация
(представление антигена T-лимфоцитам)
осуществляется в результате поглощения антигена
антигенпрезентирующей клеткой (АПК), расщепления
его внутри клетки ферментами, связывания
образующихся антигенных пептидов с молекулами MHC
(“загрузка“ антигенных пептидов в желобки
собственных молекул MHC I, II класса) и выхода их на
поверхность клетки для представления (presentation) T-лимфоцитам.
Антигенраспознающий В-клеточный | |
Антигенраспознающий | |
Антигенпрезентирующая, | |
Дендритные | |
T-лимфоциты (тимусзависимые лимфоциты) | |
T-хелперы | |
Цитотоксические | |
NK-клетки (normal | |
B-лимфоциты | |
B-лимфоциты | |
| В иммунном ответе клетки взаимодействуют при межклеточном контакте мембранами и с помощью цитокинов. Различают следующие молекулы межклеточной адгезии: селектины, муциноподобные адрессины сосудов, интегрины и молекулы из суперсемейства иммуноглобулинов. | |
| Селектины – молекулы (рецепторы) поверхности лимфоцитов, нейтрофилов, моноцитов, эозинофилов, взаимодействующие с лигандами (муциноподобными молекулами адрессинов CD34, GlyCAM-1 и MAdCAM-1) эндотелия сосудов. Участвуют в остановке клеток для их миграции через эндотелий. Интегрины – молекулы поверхности T-лимфоцитов, моноцитов, макрофагов, дендритных клеток, нейтрофилов, взаимодействующие с молекулами клеточной адгезии, фрагментами комплемента или с компонентами внеклеточного матрикса. Суперсемейство иммуноглобулинов представлено молекулами сходными (по доменам) с иммуноглобулинами: молекулы МНС I и II классов, T-клеточный рецептор, молекулы CD2, CD3, CD4, CD8, ICAM, VCAM и некоторые Fc-рецепторы. | |
Источник